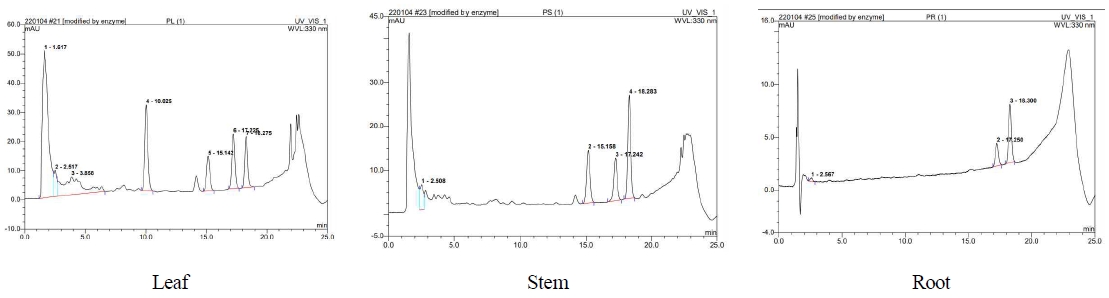
자주색 참마의 부위에 따른 항산화 활성
Abstract
This study evaluated the phenolic acid composition and antioxidant activities of extracts obtained from different parts (leaf, stem, and root) of purple yam (Dioscorea alata) to assess their potential as functional food resources. Five phenolic acids—gallic acid, caffeic acid, coumaric acid, ferulic acid, and sinapic acid—were analyzed quantitatively using ultra-high performance liquid chromatography. Significant differences in phenolic acid composition were observed among the plant parts (p<0.001). The leaf and stem extracts contained higher levels of major phenolic acids compared to the root extract, while coumaric acid was not detected in the root. The total phenolic and total flavonoid contents were highest in the leaf extract, whereas the total anthocyanin content was highest in the root extract. The antioxidant activities evaluated by DPPH and ABTS radical scavenging assays showed that the leaf extract exhibited the lowest IC₅₀ values, indicating the strongest antioxidant activity, followed by the stem and root extracts (p<0.001). The antioxidant activities were strongly correlated with the total phenolic content (p<0.01). These results suggest that the leaves and stems of Dioscorea alata, commonly regarded as agricultural by-products, are valuable sources of natural antioxidants with potential applications in food and functional materials.
Keywords:
antioxidant activity, phenolic acids, purple yam, Dioscorea alata서 론
활성산소종(reactive oxygen species, ROS)은 생체 내에서 산화 반응을 유도하여 세포 손상을 일으키며, 흡연, 과도한 스트레스, 과음 등의 요인에 의해 과도하게 생성될 수 있다(Maxwell SR 1995; Kim MJ 등 2012). 이러한 산화적 스트레스는 동맥경화, 당뇨병, 뇌졸중 및 종양 생성 등 다양한 만성 질환의 주요 원인으로 보고되고 있다(Gupta RK 등 2014). 이에 따라 활성산소종으로부터 생체를 보호할 수 있는 항산화제에 대한 연구가 지속적으로 이루어지고 있으며(Choi JS 등 2019), 최근에는 식품에 존재하는 천연 항산화 물질이 체내 산화적 손상을 완화할 수 있다는 연구 결과가 보고되면서 천연 항산화제에 대한 관심이 증가하고 있다(Choi JY 등 2015; Byun EB 등 2020).
마과(Dioscoreaceae)에 속하는 식물은 여러 해살이 덩굴식물로, 형태에 따라 단마, 장마, 부채마, 둥근마 등으로 다양하게 분류된다(Ahn JH 등 2005; Kim MK & Lee KK 2013). 마는 건강 기능성이 알려지면서 생마 소비 시장이 확대되고 있으며, 기능성 식품 소재로서의 활용 가능성에 대한 관심도 함께 증가하고 있다(Lee DS & Park YM 2013). 마는 탄수화물(전분, 당류 및 식이섬유), 단백질, 미네랄, 비타민을 비롯한 다양한 영양 성분을 함유하고 있을 뿐만 아니라(Darkwa K 등 2019), 면역 증진, 항산화, 노화 방지 등 다양한 생리활성 효과가 보고된 약용 가치가 높은 식물이다(Xie JH 등 2010; Ju Y 등 2014; Ma F 등 2017).
자주색 참마(Dioscorea alata)는 덩이뿌리 채소로 열대 둥근마 또는 물참마로 불리며, 자주색 또는 붉은색을 띠는 마과(Dioscoreaceae) 식물이다. 주로 중국을 비롯한 열대 및 아열대 지역에 널리 분포되어 있으며, mucin, choline, allantoin 등 다양한 영양 및 기능성 성분과 생리활성 물질을 함유하고 있다(Kwon JB 등 2010; Fang Z 등 2011; Zhang J 등 2018; Liu X 등 2019; Srivichai S & Hongsprahas P 2020). 특히 자주색 참마에는 높은 항산화 활성을 나타내는 안토시아닌이 풍부하게 함유되어 있으며(Moriya C 등 2015), cyanidin 계열을 기반으로 한 cyanidin-3-glucoside 및 cyanidin-3-6-sinapoylgentiobioside 등이 주요 안토시아닌으로 보고되었다(Srivichai S & Hongsprahas P 2020).
한편, 마의 뿌리는 식품 및 약용 소재로 널리 활용되고 있으나, 잎과 줄기는 대부분 소각되거나 폐기되어 환경오염의 원인이 되고 있다(Kim MJ 등 2021). 그러나 일부 선행연구에 따르면 마의 잎은 생체 내에서 우수한 항산화 및 항염증 활성을 나타냄에도 불구하고(Das A 등 2014; Omodamiro OD 2015), 뿌리에 비해 상대적으로 연구가 미흡한 실정이다.
최근 농업 및 식품 산업에서는 부산물로 발생하는 식물성 자원의 활용 가능성을 재조명하여, 고부가가치 기능성 식품 소재로 활용하고자 하는 연구가 활발히 진행되고 있다(Kim MJ 등 2021). 이에 본 연구에서는 자주색 참마의 잎, 줄기 및 뿌리 부위별 항산화 활성을 비교·분석하여 부위에 따른 기능적 특성을 규명하고, 자주색 참마 부산물인 잎과 줄기의 활용 가능성을 제시하기 위한 기초 자료를 제공하고자 하였다.
재료 및 방법
1. 실험 재료 및 시약
본 연구에서 사용된 자주색 참마의 잎, 줄기, 뿌리는 충청남도 논산에서 2021년에 수확한 것을 구입하여 실험에 사용하였다. 자주색 참마의 뿌리는 세척 후 껍질을 제거하였으며, 잎과 줄기는 세척하였다. 손질한 원물은 동결건조(MCFD 8508, Ilshin Bio Base, Yangju, Korea)하고 건조된 원물은 분쇄기(HR2056, Philips, Seoul, Korea)로 분쇄하여 초저온냉동고(New Brunswick Scientific Co., Edison, NY, USA)에 보관하여 사용하였다. 본 연구에서 사용된 시약은 Folin & Ciocalteu’s phenol reagent, 2,2-azino-bis diammonium salt, gallic acid, rutin, potassium persulfate 등이 사용되었다. 모든 시약은 Sigma-Aldrich Chemical Co., Junsei chemical Co. 등의 1급 시약을 사용하였다.
2. 시료 추출
자주색 참마의 잎, 줄기, 뿌리의 항산화 활성 측정을 위해 추출용매는 70% ethanol을 사용하였다. 동결건조된 시료들은 각각 20 g씩 삼각 플라스크에 담아 20배의 용매를 가하고, 25℃의 항온진탕기(SI-900R, JEJIO TECH, Gimpo, Korea)에서 125 rpm, 24시간 상온교반 추출을 3회 반복하여 추출액을 얻었다. 추출액은 회전식 진공 증발·농축기(NVC-2100, EYELA, Tokyo, Japan)로 농축하였다. 농축액은 동결건조하여 시료로 사용하였으며, —40℃에서 보관하며 사용하였다. 추출 수율은 추출 전후의 시료 중량을 측정하여 계산하였다.
3. UPLC Phenolic Acid 정량분석
자주색 참마 부위별 시료 0.1 g에 2.6 M NaOH 6 mL를 가한 후, 초음파 추출기(Power sonic 410, Hwashin Technology Co., Yeongcheon, Korea)를 이용하여 15분간 초음파 추출하였다. 이후 페놀산을 함유한 식물 세포벽 성분의 분해를 유도하기 위해 25℃에서 200 rpm으로 설정된 항온진탕기에서 20시간 반응시켰다. 반응이 완료된 추출물은 25℃에서 3,000 rpm으로 5분간 원심분리하였으며, 상층액 2 mL에 35% HCl 0.5 mL를 첨가한 후 30분간 냉장 보관하여 산 가수분해를 진행하였다. 분석 전 시료는 PTFE syringe filter(13 mm, 0.2 μm; Tokyo, Japan)로 여과하였다. Phenolic acid 분석은 UPLC(Ultimate 3000, Dionex, Idstein, Germany)를 이용하여 수행하였다. 분리를 위해 XTerra MS C18 column(125 Å, 5 μm, 3.9 mm × 150 mm, Waters, Japan)을 사용하였으며, column 온도는 30℃로 유지하였다. 검출은 photodiode array detector(Ultimate 3000 PDA detector, Dionex, Idstein, Germany)를 사용하였다. 이동상으로는 A용매로 0.1% formic acid가 함유된 증류수, B용매로 0.1% formic acid가 함유된 메탄올을 사용하였다. 초기 이동상 조건은 A용매 85%, B용매 15%로 설정하여 안정화시킨 후 분석을 시작하였으며, 총 분석 시간은 12.5분으로 하였다. 유속은 0.8 mL/min, 주입량은 1.0 μL로 설정하였다. 정량분석을 위한 표준물질로는 gallic acid, caffeic acid, coumaric acid, ferulic acid 및 sinapic acid를 사용하였다. Gallic acid는 220 nm에서, caffeic acid, coumaric acid, ferulic acid 및 sinapic acid는 330 nm에서 흡광도를 측정하여 정량분석하였다.
4. 총 폴리페놀 함량
총폴리페놀 함량은 Swain T & Hillis WE(1959)의 Folin-Ciocalteu법에 준하여 측정하였다. 시료액 150 μL에 증류수 2.4 mL, 2 N Folin-ciocalteau 용액 50 μL을 가하여 3분간 반응시켰다. 반응시킨 용액에 1 N sodium carbonate 300 μL을 가하여 교반한 뒤, 암소에서 2시간 동안 방치시켜 UV/VIS 분광광도계(T60UV, PG Instruments, Wibtoft, England)에서 흡광도 725 nm로 측정하였다. 표준물질은 gallic acid를 사용하여 계산하였으며, 실험은 3회 반복하여 평균값과 표준편차를 구하였다.
5. 총 플라보노이드 함량
총 플라보노이드 함량은 Davis 변법(Chang CC 등 2002)에 준하여 측정하였다. 시료액 1 mL에 90% diethylenglycol 10 mL, 1 N NaOH 1 mL를 가하여 교반한 뒤, 37℃의 water bath에서 1시간 반응시켰다. 반응시킨 용액은 흡광도 420 nm에서 측정하였다. 표준물질은 rutin을 이용하여 계산하였으며, 실험은 3회 반복하여 평균값과 표준편차를 구하였다.
6. 총 안토시아닌 함량
총 안토시아닌 함량은 pH differential method에 준하여 측정하였다. 시료액 0.5 mL에 0.025 M potassium chloride buffer(pH 1.0)와 0.4 M sodium acetate buffer(pH 4.5)를 각각 가하여 최종부피를 1 mL로 제조하여 흡광도 510 nm와 700 nm에서 각각의 반응액을 측정하였다. 총 안토시아닌 함량은 cyanidin-3-glucoside의 몰 흡광계수(ε=26,900 M-1cm-1)를 이용하고, 다음과 같은 식으로 산출하였다.
- A (absorbance value) = (A510 nm — A700 nm) at pH 1.0 — (A510 nm — A700 nm) at pH 4.5
- MW (molecular weight of cyanidin-3-glucoside) — 449.2
- D (dilution factor) — dilution ratio of sample
- ε (cyanidin-3-glucoside molar absorbance) = 26,900 M-1cm-1
- V = final volume of sample
7. DPPH Radical 소거 활성
DPPH radical 소거 활성은 Blois MS(1958) 방법에 준하여 측정하였다. DPPH radical 소거 활성은 항산화 물질이 DPPH 라디칼과 반응하여 보라색이 노란색으로 탈색되는 원리를 이용한 방법이다(Bondet V 등 1997). 시료액 900 μL에 DPPH solution 300 μL를 가하여 교반한 후, 30분간 암소에서 방치시켜 517 nm에서 흡광도를 측정하였다. 시료를 첨가하지 않은 대조군의 흡광도를 이용하여, 다음과 같은 식을 활용하여 백분율로 나타내어 IC50을 구하였다. 실험은 3회 반복하였으며, 평균값과 표준편차를 나타내었다.
8. ABTS Radical 소거 활성
ABTS radical 소거 활성은 Re R(1999)의 방법을 변형하여 측정하였다. ABTS radical 소거 활성은 ABTS 자유라디칼이 항산화 물질에 의해 제거되면서 청록색이 탈색되는 원리를 기반으로 한다(Kim YD 등 2009). 7 mM ABTS와 2.45 mM potassium persulfate를 혼합하여 16시간 동안 암소에서 반응시켜 ABTS radical을 생성시켰다. 라디칼이 생성된 ABTS는 PBS buffer로 734 nm에서 흡광도 값이 0.70±0.02가 되도록 희석하였다. 시료액 100 μL에 ABTS+ solution 900 μL를 첨가하여 734 nm에서 흡광도를 측정하였다. 다음과 같은 식을 활용하여 백분율로 나타내어 IC50을 구하였다. 실험은 3회 반복하였으며, 평균값과 표준편차를 나타내었다.
9. 환원력(Reducing Power)
환원력은 Yildirin A(2001)의 방법에 준하여 실험을 진행하였다. 시료액 2.5 mL에 0.2 M sodium phosphate buffer(pH 6.6) 2.5 mL를 가한 후, 1% potassium ferricyanide 2.5 mL를 가하였다. 혼합물은 20분간 50℃ water bath에서 반응시키고, 10% TCA 2.5 mL를 첨가하였다. 혼합물의 상등액 5 mL와 증류수 5 mL를 혼합한 뒤, 0.1% ferric chloride 1 mL를 첨가하고 700 nm에서 흡광도를 측정하였다. 값은 흡광도(O.D.)로 나타내었으며, 실험은 3회 반복하여 평균값과 표준편차를 구하였다.
10. 통계처리
모든 실험의 통계분석은 SPSS statistics(ver. 25, IBM Co., Armonk, NY, USA)를 이용하였으며, 평균과 표준편차를 나타내었다. 각 샘플 사이의 유의성 확인을 위해 일원배치분산분석(One-way ANOVA)를 실시하였다. 유의수준 5%에서 유의성이 나타날 경우 다중범위검정(Duncan’s multiple range test)를 실시하여 사후검증을 실시하였다. 자주색 참마의 부위별 상관관계는 상관분석을 통하여 Pearson 계수로 통계적 유의성을 검증하였다.
결과 및 고찰
1. 추출 수율
자주색 참마의 부위별 추출 수율은 Table 1과 같다. 70% 에탄올을 이용하여 추출을 진행하였으며, 잎 추출물이 22.2%, 줄기 추출물이 20.2%, 뿌리 추출물이 11.1%로 잎의 추출 수율이 가장 높았다. 맹그로브 연구에서도 잎, 줄기, 열매 중 잎 추출물의 추출 수율이 가장 높게 나타나 본 연구와 유사한 경향을 보였다(Rahmawati SI 등 2019). 이는 잎은 줄기나 뿌리보다 세포벽이 약한 조직이기 때문에 화합물의 추출이 용이하여 나타난 결과로 보여진다(Rahmawati SI 등 2019).
2. UPLC를 이용한 페놀산 정량분석
자주색 참마 부위별 추출물의 페놀산 5종 gallic acid, caffeic acid, coumaric acid, ferulic acid, sinapic acid 함량은 Table 2와 Fig. 1에 나타내었다. Gallic acid 함량은 줄기 6.03 mg/g에서 가장 높게 나타났으며, 잎 5.04 mg/g, 뿌리 0.22 mg/g 순으로 유의적인 차이를 보였다(p<0.001). Caffeic acid 함량 또한 잎 0.70 mg/g이 가장 높았고, 줄기 0.39 mg/g, 뿌리 0.11 mg/g 순으로 감소하여 부위 간 유의적인 차이가 확인되었다(p<0.001). Coumaric acid는 잎과 줄기에서 각각 0.47 mg/g 및 0.51 mg/g로 검출되었으나, 뿌리에서는 검출되지 않아 부위별 조성 차이가 뚜렷하게 나타났다(p<0.001). Ferulic acid의 경우 잎 1.17 mg/g에서 가장 높은 함량을 보였으며, 줄기 0.70 mg/g, 뿌리 0.16 mg/g 순으로 유의적인 감소 경향을 나타냈다(p<0.001). Sinapic acid 함량은 줄기 0.85 mg/g에서 가장 높았고, 잎 0.58 mg/g, 뿌리 0.25 mg/g 순으로 나타나 부위별 유의적인 차이를 보였다(p<0.001). 이와 같이 자주색 참마의 페놀산 조성은 부위에 따라 뚜렷한 차이를 나타냈으며, 특히 잎과 줄기에서 주요 페놀산이 상대적으로 높은 함량으로 분포함을 확인하였다. 본 연구에서 잎과 줄기에 다량 분포한 gallic acid와 caffeic acid는 기존 연구에서 DPPH 자유라디칼 소거능이 가장 우수한 페놀산으로 보고된 바 있으며, ferulic acid와 sinapic acid 또한 항산화 활성을 나타내는 성분으로 알려져 있다(Karamać M 등 2005). 반면, coumaric acid 계열은 상대적으로 낮은 라디칼 소거능을 보이는 페놀산으로 보고되었으며, 본 연구에서 뿌리 부위에서 검출되지 않은 결과는 이러한 특성과 일관된 경향을 나타낸다(Karamać M 등 2005).
3. 총 폴리페놀 함량
자주색 참마의 부위별 총 폴리페놀 함량은 Table 3과 같다. 총 폴리페놀 함량 측정은 채소, 과일의 기능적 품질성분을 지표로 검정하며 널리 이용되는 방법이다(Sato M 등 1996). 페놀화합물은 천연 식물성 화합물로 hydroxyl기를 가지고 있으며, 활성산소로 생성된 산화를 억제시키는 항암, 항산화, 항균 등의 생리활성 기능을 지닌 것으로 보고되었다(Nozaki K 1986; Nakatani N 1990). 페놀성 화합물에는 phenol류, phenolic acid류, 플라보노이드류 등이 있다(Huang MT 등 1992). 식물성 천연물의 추출물에는 여러 가지 물질이 함유되어 있으며, 그 중 폴리페놀을 측정하는데 주로 사용되는 방법으로는 gallic acid의 함량을 비색법으로 측정하는 법이 있다(Lee EH 등 2021).
자주색 참마의 잎, 줄기, 뿌리 추출물의 총 폴리페놀 함량은 각각 187.67 mg GAE/g, 147.60 mg GAE/g, 24.11 mg GAE/g으로 잎 추출물이 가장 높은 함량을 나타내었다(p<0.001). Sembiring EN 등(2018)의 연구는 피버넛의 부위별 항산화를 측정하였다. 잎, 뿌리, 줄기의 폴리페놀 함량은 각각 146.64 mg GAE/g, 144.42 mg GAE/g, 89.81 mg GAE/g을 나타내었으며, 잎 추출물에서 가장 높은 페놀함량을 보였다. 식물에 널리 존재하는 페놀이 식물 조직에서 균일하게 분포되지 않아 나타난 결과로 보여지며(Naczk M & Shahidi F 2004), 이는 같은 종 내에서 유전적 요인, 환경 조건 및 성장 단계 때문에 발생할 수 있다고 보고되었다(Cheynie V 2005).
4. 총 플라보노이드 함량
자주색 참마의 부위별 총 플라보노이드 함량은 Table 3과 같다. 플라보노이드는 채소, 곡물 및 과실류 등에 풍부하게 함유되어 있으며, 노란색, 담황색을 나타낸다(Hetog MGL 등 1993). 페놀성 화합물 중 하나로 2개의 방향성 고리 구조와 15개의 탄소를 포함하는 구조를 지닌다(Böhm H 등 1998).
자주색 참마 잎의 총 플라보노이드 함량은 121.94 mg RE/g으로 가장 높은 함량을 보였으며, 줄기, 뿌리는 각각 81.87 mg RE/g, 16.24 mg RE/g으로 나타났다(p<0.001). 이러한 결과는 플라보노이드가 페놀성 화합물의 일종으로 총 폴리페놀 함량과 유사한 경향을 나타낸 것으로 보인다. Makorei SI 등(2020)의 연구에서 자색고구마도 줄기와 뿌리보다 잎에서 높은 플라보노이드 함량을 나타내었다.
5. 총 안토시아닌 함량
자주색 참마의 부위별 총 안토시아닌 함량은 Table 3과 같다. 안토시아닌은 자색, 청색, 적색 등을 나타내는 천연 색소 성분으로 과일 및 채소에 폭넓게 분포되어 있다(Kim HJ 등 2015). 안토시아닌은 모두 안토시아니딘 배당체로 안토시아니딘은 flavylium의 기본구조에 수산기 또는 메톡실기가 치환되어있는 구조를 지닌다(Choi SJ 2010). 이러한 안토시아닌은 2차 대산물로 항산화 작용, 항염증 및 항암 활성 등의 효능을 지닌다고 보고되었다(Tsuta T 1996; Ryu SN 등 2000; Hwang YP 등 2011).
자주색 참마의 잎, 줄기, 뿌리 추출물의 총 안토시아닌 함량은 각각 2.56 mg/100 g, 22.93 mg/100 g, 231.56 mg/100 g으로 뿌리 추출물이 가장 높은 함량을 보였다. 자주색 참마 뿌리의 자주색은 식용 색소로 사용되며, 다양한 안토시아닌이 함유되어 있다고 보고되었다(Moriya C 등 2015). 본 연구에서는 자주색 참마의 뿌리 외에도 잎과 줄기에서 안토시아닌 함량을 확인할 수 있었으며, 향후 자주색 참마의 잎과 줄기의 안토시아닌 연구가 추가적으로 필요하다고 생각된다.
6. 항산화 활성
DPPH 및 ABTS radical 소거 활성은 항산화 활성을 평가하기 위해 보편적으로 사용되는 분석 방법이다. 자주색 참마의 잎, 줄기, 뿌리의 DPPH 및 ABTS radical 소거 활성은 Table 4와 같으며, 라디칼 50% 저해하는 데 필요한 농도(IC₅₀)로 나타내었다. 잎, 줄기, 뿌리의 DPPH IC50은 각각 13.12, 25.00, 125.25 μg/mL이며, ABTS IC50은 각각 80.80, 95.77, 637.99 μg/mL로 나타났다. Choi HY 등(2009)은 연근 부위별로 잎, 줄기, 뿌리에 대한 항산화 활성을 연구하였다. 80% 에탄올에서 추출한 잎, 줄기, 뿌리 추출물은 1000 μg/mL에서 DPPH는 각각 66%, 27%, 10%의 활성을 보였으며, ABTS 활성은 각각 25%, 11%, 3%로 나타나 잎에서 가장 높은 활성을 보였다(Choi HY 등 2009). 또한 Bae MJ 등(2019)은 식물 부위별 폴리페놀 함량 차이가 항산화 활성에 영향을 미친다고 보고하였으며, 본 연구에서 잎 추출물이 가장 우수한 DPPH 및 ABTS radical 소거 활성을 보인 결과와 일치하는 경향을 나타낸다.
환원력(reducing power)은 ferric-ferricyanide 혼합물이 항산화 물질에 의해 ferrous 형태로 환원되는 정도를 흡광도로 측정하는 방법으로, 항산화 물질의 전자공여능을 평가하는 지표이다(Sa YJ 등 2010). 자주색 참마 부위별 환원력은 Table 4에 나타내었으며, 모든 시료에서 농도가 증가함에 따라 환원력이 증가하는 경향을 보였다. 특히 잎 추출물은 모든 농도 조건(1,000∼50 μg/mL)에서 줄기 및 뿌리 추출물에 비해 유의적으로 높은 흡광도 값을 나타내어 가장 우수한 환원력을 보였다(p<0.001).
7. 상관관계
자주색 참마의 부위별 추출물의 총 폴리페놀, 총 플라보노이드, 총 안토시아닌 함량과 항산화 활성을 측정한 실험 결과들의 상관관계는 Table 5와 같다. 총 폴리페놀 함량과 총 플라보노이드, 환원력은 각각 r=0.763(p<0.05), r=0.975(p<0.01)로 유의적인 양의 상관관계를 보였으며, 총 안토시아닌은 r=—0.964(p<0.01)로 유의적인 음의 상관관계를 나타내었다. 총 폴리페놀의 함량이 높아질수록 전자공여능의 IC50 값은 낮아지면서 높은 항산화 활성을 보였으며, 총 폴리페놀과 DPPH, ABTS 활성은 각각 r=—0.985(p<0.01), r=—0.973(p<0.01)로 높은 음의 상관관계를 나타내었다. 이러한 결과는 자주색 참마의 잎, 줄기 및 뿌리 추출물에서 나타나는 항산화 활성이 총 폴리페놀 함량과 밀접한 관련이 있음을 시사하며, 페놀성 화합물이 항산화 활성에 주요하게 기여하는 성분으로 작용했을 가능성을 보여준다. 특히 총 플라보노이드 및 총 안토시아닌 함량보다 총 폴리페놀 함량이 항산화 활성과 더 강한 상관관계를 나타낸 점은, 자주색 참마 추출물의 항산화 활성이 특정 단일 성분보다는 다양한 페놀성 화합물의 복합적인 작용에 기인했을 가능성을 시사한다. DPPH, ABTS 및 환원력은 모두 전자공여 또는 환원 메커니즘을 기반으로 항산화 활성을 평가하는 지표로, 본 연구에서 이들 활성 지표가 총 폴리페놀 함량과 일관되게 높은 상관성을 보인 결과는 페놀성 물질이 자유라디칼 소거 및 환원 반응에 효과적으로 관여했음을 의미한다.

Correlation between the total phenolic contents and antioxidant activities of parts of Dioscorea alata
본 연구는 자주색 참마의 부위별 추출물에 대한 항산화 활성과 페놀성 화합물 함량을 비교하여 기능성 소재로서의 가능성을 평가하였으나, in vitro 분석에 한정되어 실제 생체 내 효능을 직접적으로 반영하지 못한다는 한계가 있다. 향후에는 다양한 용매 조건에 따른 추출 효율 비교, 생리활성 물질의 정밀 분석 및 세포 또는 동물 모델을 이용한 생체 내 효능 검증 연구가 수행될 필요가 있을 것으로 판단된다.
요 약
본 연구에서는 자주색 참마(Dioscorea alata)의 잎, 줄기 및 뿌리 부위별 추출물의 페놀성 화합물 조성 및 항산화 활성을 비교·분석하여 부위별 활용 가능성을 평가하고자 하였다. 70% 에탄올을 이용한 추출 결과, 잎 추출물이 22.2%로 가장 높은 추출 수율을 보였으며, 줄기(20.2%), 뿌리(11.1%) 순으로 나타났다.
UPLC를 이용한 페놀산 정량분석 결과, gallic acid, caffeic acid, coumaric acid, ferulic acid, sinapic acid의 함량은 부위에 따라 유의적인 차이를 보였다(p<0.001). Gallic acid와 sinapic acid는 줄기에서 가장 높았으며, caffeic acid와 ferulic acid는 잎에서 높은 함량을 나타냈다. Coumaric acid는 잎과 줄기에서만 검출되었고, 뿌리에서는 검출되지 않았다. 전반적으로 잎과 줄기에서 주요 페놀산이 상대적으로 높은 함량으로 분포하였다.
총 폴리페놀과 총 플라보노이드 함량은 잎 추출물에서 각각 187.67 mg GAE/g, 121.94 mg RE/g으로 가장 높았으며, 줄기, 뿌리 순으로 감소하였다. 반면, 총 안토시아닌 함량은 뿌리 추출물에서 231.56 mg/100 g으로 가장 높게 나타나 부위별 상이한 분포 특성을 보였다.
항산화 활성 평가 결과, DPPH 및 ABTS radical 소거 활성(IC₅₀)은 잎 추출물이 가장 낮은 값을 나타내어 가장 우수한 항산화 활성을 보였으며, 줄기, 뿌리 순으로 감소하였다(p<0.001). 환원력 또한 모든 농도 조건에서 잎 추출물이 가장 높은 흡광도를 나타냈다.
상관관계 분석 결과, 총 폴리페놀 함량은 DPPH(r=—0.985), ABTS(r=—0.973) 및 환원력(r=0.975)과 높은 상관관계를 나타냈으며(p<0.01), 항산화 활성이 총 폴리페놀 함량과 밀접한 관련이 있음을 확인하였다. 이러한 결과는 자주색 참마 추출물의 항산화 활성이 특정 단일 성분보다는 다양한 페놀성 화합물의 복합적인 작용에 기인했을 가능성을 시사한다.
본 연구를 통해 자주색 참마의 잎과 줄기는 높은 페놀성 화합물 함량과 우수한 항산화 활성을 지닌 유용한 천연 자원임을 확인하였으며, 식품 및 기능성 소재로서의 활용 가능성을 제시하였다.
References
-
Ahn JH, Son KH, Sohn HY, Kwon ST (2005) In vitro culture of adventitious roots from Dioscorea nipponica Makino for the production of steroidal saponins. J Plant Biotechnol 32(3): 217-223.
[https://doi.org/10.5010/JPB.2005.32.3.217]

-
Bae MJ, Kim EN, Choi HK, Byun MS, Chung KH, Yoon JA, An JH (2019) Quality characteristics and antioxidant activities of strawberries according to various extraction methods. J Korean Soc Food Sci Nutr 48(7): 728-738.
[https://doi.org/10.3746/jkfn.2019.48.7.728]

-
Blois MS (1958) Antioxidant determinations by the use of a stable free radical. Nature 181: 1199-1200.
[https://doi.org/10.1038/1811199a0]

-
Böhm H, Boeing H, Hempel J, Raab B, Kroke A (1998) Flavonols, flavone and anthocyanins as natural antioxidants of food and their possible role in the prevention of chronic diseases. Z Ernahrungswiss 37(2): 147-163.
[https://doi.org/10.1007/PL00007376]

-
Bondet V, Brand-Williams W, Berset C (1997) Kinetics and mechanisms of antioxidant activity using the DPPH free radical method. LWT-Food Sci Technol 30(6): 609-615.
[https://doi.org/10.1006/fstl.1997.0240]

- Byun EB, Kim MJ, Kim SJ, Oh NS, Park SH, Kim WS, Song HY, Jong FM, Kim K, Byun C (2020) Antioxidant activity and neuroprotective effects of ethanol extracts from the core of Diospyros kaki. Korean J Food Sci Technol 52(1): 60-66.
-
Chang CC, Yang MH, Wen HM, Chern JC (2002) Estimation of total flavonoid content in propolis by two complementary colorimetric methods. J Food Drug Anal 10(3): 178-182.
[https://doi.org/10.38212/2224-6614.2748]

-
Cheynier V (2005) Polyphenols in foods are more complex than often thought. Am J Clin Nutr 81(1): 223S-229S.
[https://doi.org/10.1093/ajcn/81.1.223S]

- Choi HY, Jung K, Shin HS (2009) Antioxidant activity of the various extracts from different parts of lotus (Nelumbo nucifera Gaertner). Food Sci Biotechnol 18(4): 1051-1054.
-
Choi JS, Han SD, Jang TW, Lee SH, Park JH (2019) Antioxidant and anti-inflammatory activity of parts of Rhus javanica L. J Appl Biol Chem 62(2): 195-202.
[https://doi.org/10.3839/jabc.2019.027]

-
Choi JY, Jo MK, Goo YM, Kim HK, Shin JW, Kim DY, Kim HJ, Lee EH, Kim NH, Cho YJ (2015) Antioxidant activities of phenolic compounds from medicinal plants (Hibiscus esculentus, Cirsium japonicum, Zizania latifolia and Kalopanax pictus). Current Research on Agriculture and Life Sciences 33(2): 57-63.
[https://doi.org/10.14518/crals.2015.33.2.010]

- Choi SJ (2010) The difference of anthocyanin pigment composition and color expression in fruit skin of several grape cultivars. J Food Preserv 17(6): 847-852.
-
Darkwa K, Olasanmi B, Asiedu R, Asfaw A (2020) Review of empirical and emerging breeding methods and tools for yam (Dioscorea spp.) improvement: Status and prospects. Plant Breeding 139(3): 474-497.
[https://doi.org/10.1111/pbr.12783]

- Das A, Chaudhuri D, Ghate N, Chatterjee A, Mandal N (2014) Phytochemical analysis, antioxidant and anticancer potential of leaf extracts from edible greater yam, Dioscorea Alata L., from North-East India. Int J Phytopharmacol 5(2): 109-119.
-
Fang Z, Wu D, Yü D, Ye X, Liu D, Chen J (2011) Phenolic compounds in Chinese purple yam and changes during vacuum frying. Food Chem 128(4): 943-948.
[https://doi.org/10.1016/j.foodchem.2011.03.123]

-
Gupta RK, Patel AK, Shah N, Chaudhary AK, Jha UK, Yadav UC, Gupta PK, Pakuwal U (2014) Oxidative stress and antioxidants in disease and cancer: A review. Asian Pac J Cancer Prev 15(11): 4405-4409.
[https://doi.org/10.7314/APJCP.2014.15.11.4405]

-
Hertog MGL, Hollman PCH, Van de Putte B (1993) Content of potentially anticarcinogenic flavonoids of tea infusions, wines, and fruit juice. J Agric Food Chem 41(8): 1242-1246.
[https://doi.org/10.1021/jf00032a015]

-
Huang MT, Ho CT, Lee CY (1992) Phenolic compounds in food. Vol II. pp 2-33. In: Phenolic compounds in food and their effects on health II. Ho CT, Lee CY, Huang MT (eds). Maple Press, New York, NY, USA.
[https://doi.org/10.1021/bk-1992-0507]

-
Hwang YP, Choi JH, Han EH, Kim HG, Wee JH, Jung KO, Jung KH, Kwon KI, Jeong TC, Chung YC, Jeong HG (2011) Purple sweet potato anthocyanins attenuate hepatic lipid accumulation through activating adenosine monophosphate-activated protein kinase in human HepG2 cells and obese mice. Nutr Res 31(12): 896-906.
[https://doi.org/10.1016/j.nutres.2011.09.026]

-
Ju Y, Xue Y, Huang J, Zhai Q, Wang X (2014) Antioxidant Chinese yam polysaccharides and its pro-proliferative effect on endomertial epithelial cells. Int J Biol Macromol 66: 81-85.
[https://doi.org/10.1016/j.ijbiomac.2014.01.070]

- Karamać M, Kosińska A, Pegg RB (2005) Comparison of radical-scavenging activities for selected phenolic acids. Pol J Food Nutr Sci 55(2): 165-170.
-
Kim HJ, Wee JH, Yang EJ (2015) Optimal conditions for anthocyanin extraction from black rice bran and storage stability of anthocyanin extract. J Korean Soc Food Sci Nutr 44(10): 1543-1549.
[https://doi.org/10.3746/jkfn.2015.44.10.1543]

-
Kim MJ, Chu WM, Park EJ (2012) Antioxidant and antigenotoxic effects of shiitake mushrooms affected by different drying methods. J Korean Soc Food Sci Nutr 41(8): 1041-1048.
[https://doi.org/10.3746/jkfn.2012.41.8.1041]

-
Kim MJ, Son SY, Jeon SG, Kim JG, Lee CH (2021) Metabolite profiling of Dioscorea (Yam) leaves to identify bioactive compounds reveals their potential as renewable resources. Plants 10(8): 1751.
[https://doi.org/10.3390/plants10081751]

- Kim MK, Lee KK (2013) Screening of physiological activities of Dioscurea japonica extracts. J Kor Soc Cosmetol 19(3): 509-515.
-
Kim YD, Ko WJ, Koh KS, Jeon YJ, Kim SH (2009) Composition of flavonoids and antioxidative activity from juice of Jeju native citrus fruits during maturation. Korean J Nutr 42(3): 278-290.
[https://doi.org/10.4163/kjn.2009.42.3.278]

-
Lee DS, Park YM (2013) Optimization of curing treatment and storage temperature of Chinese yam. Hort Sci Technol 31(3): 289-298.
[https://doi.org/10.7235/hort.2013.12195]

-
Lee EH, Park HJ, Kang IK, Cho YJ (2021) Functional properties of newly bred ‘Summer Prince’ apples. Hortic Sci Technol 39(4): 530-545.
[https://doi.org/10.7235/HORT.20210048]

-
Liu X, Lu K, Yu J, Copeland L, Wang S, Wang S (2019) Effect of purple yam flour substitution for wheat flour on in vitro starch digestibility of wheat bread. Food Chem 284: 118-124.
[https://doi.org/10.1016/j.foodchem.2019.01.025]

-
Ma F, Zhang Y, Liu N, Zhang J, Tan G, Kannan B, Liu X, Bell AE (2017) Rheological properties of polysaccharides from Dioscorea opposite Thunb. Food Chem 227: 64-72.
[https://doi.org/10.1016/j.foodchem.2017.01.072]

-
Makori SI, Mu TH, Sun HN (2020) Total polyphenol content, antioxidant activity, and individual phenolic composition of different edible parts of 4 sweet potato cultivars. Nat Prod Commun 15(7): 1-12.
[https://doi.org/10.1177/1934578X20936931]

-
Maxwell SRJ (1995) Prospects for the use of antioxidant therapies. Drugs 49(3): 345-356.
[https://doi.org/10.2165/00003495-199549030-00003]

-
Moriya C, Hosoya T, Agawa S, Sugiyama Y, Kozone I, Shin-ya K, Terahara N, Kumazawa S (2015) New acylated anthocyanins from purple yam and their antioxidant activity. Biosci Biotechnol Biochem 79(9): 1484-1492.
[https://doi.org/10.1080/09168451.2015.1027652]

-
Naczk M, Shahidi F (2004) Extraction and analysis of phenolics in food. J Chromatogr A 1054(1-2): 95-111.
[https://doi.org/10.1016/S0021-9673(04)01409-8]

-
Nakatani N (1990) Recent advances in the study on natural antioxidants. Nippon Shokuhin Kogyo Gakkaishi 37(7): 569-576.
[https://doi.org/10.3136/nskkk1962.37.7_569]

- Nozaki K (1986) Current aspect and future condition of phytogenic antioxidants. Fragrance J 6: 99-106.
- Omodamiro OD (2015) Anti-inflammatory and diuretic activities ethanol extract of Dioscorea bulbifera leaf. American Journal of Drug Delivery and Therapeutics 2(1): 29-38.
-
Rahmawati SI, Izzati FN, Hapsari Y, Septiana E, Rachman F, Bustanussalam, Simanjuntak P (2019) Endophytic microbes and antioxidant activities of secondary metabolites from mangroves Avicennia marina and Xylocarpus granatum. Earth Environ Sci 278: 012065.
[https://doi.org/10.1088/1755-1315/278/1/012065]

-
Re R, Pellegrini N, Proteggente A, Pannala A, Yang M, Rice-Evans C (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radic Biol Med 26(9-10): 1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]

- Ryu SN, Han SJ, Park SZ, Kim HY (2000) Antioxidative activity and varietal difference of cyanidin 3-glucoside and peonidin 3-glucoside contents in pigmented rice. Korean J Crop Sci 45(4): 257-260.
- Sa YJ, Kim J, Kim MO, Jeong HJ, Yu CY, Park DS, Kim MJ (2010) Comparative study of electron donating ability, reducing power, antimicrobial activity and inhibition of α glucosidase by Sorghum bicolor extracts. Korean J Food Sci Technol 42(5): 598-604.
-
Sato M, Ramarathnam N, Suzuki Y, Ohkubo T, Takeuchi M, Ochi H (1996) Varietal differences in the phenolic content and superoxide radical scavenging potential of wines from different sources. J Agric Food Chem 44(1): 37-41.
[https://doi.org/10.1021/jf950190a]

-
Sembiring EN, Elya B, Sauriasari R (2018) Phytochemical screening, total flavonoid and total phenolic content and antioxidant activity of different parts of Caesalpinia bonduc (L.) Roxb. Pharmacogn J 10(1): 123-127.
[https://doi.org/10.5530/pj.2018.1.22]

-
Srivichai S, Hongsprabhas P (2020) Profiling anthocyanins in Thai purple yams (Dioscorea alata L.). Int J Food Sci 2020: 1594291.
[https://doi.org/10.1155/2020/1594291]

-
Swain T, Hillis WE (1959) The phenolic constituents of Prunus domestica. I.: The quantitative analysis of phenolic constituents. J Sci Food Agric 10(1): 63-68.
[https://doi.org/10.1002/jsfa.2740100110]

-
Tsuda T, Shiga K, Ohshima K, Kawakishi S, Osawa T (1996) Inhibition of lipid peroxidation and the active oxygen radical scavenging effect of anthocyanin pigments isolated from Phaseolus vulgaris L. Biochem Pharmacol 52(7): 1033-1039.
[https://doi.org/10.1016/0006-2952(96)00421-2]

-
Xie JH, Xie MY, Nie SP, Shen MY, Wang YX, Li C (2010) Isolation, chemical composition and antioxidant activities of a water-soluble polysaccharide from Cyclocarya paliurus (Batal.) Iljinskaja. Food Chem 119(4): 1626-1632.
[https://doi.org/10.1016/j.foodchem.2009.09.055]

-
Yıldırım A, Mavi A, Kara AA (2001) Determination of antioxidant and antimicrobial activities of Rumex crispus L. extracts. J Agric Food Chem 49(8): 4083-4089.
[https://doi.org/10.1021/jf0103572]

-
Zhang J, Tian H, Zhan P, Du F, Zong A, Xu T (2018) Isolation and identification of phenolic compounds in Chinese purple yam and evaluation of antioxidant activity. LWT-Food Sci Technol 96: 161-165.
[https://doi.org/10.1016/j.lwt.2018.05.019]