생강 또는 표고버섯 함유 꼬막 초절임이 RBL-2H3 세포에서 IgE 매개 알레르기 반응에 미치는 영향


Abstract
This study evaluated the quality changes and allergen-reducing effects of pickled ark shell (Scapharca subcrenata) containing ginger (PASG) and pickled ark shell containing shiitake mushroom (PASSM). During the storage period, the pH of both pickling solutions increased until day 4 and then stabilized, while the salinity decreased until day 2 and remained constant thereafter. The sugar content decreased after adding of boiled ark shell meat (BAS). In IgE-sensitized RBL-2H3 cells, raw ark shell meat (RAS) showed a significantly higher β-hexosaminidase release than the IgE-only control group and the IgE plus antigen (DNP-HSA) positive control group, indicating its allergenic potential. On the other hand, BAS showed significantly lower β-hexosaminidase release than RAS. PASG and PASSM significantly suppressed the secretion of β-hexosaminidase and tumor necrosis factor-α (TNF-α) compared to BAS, and the β-hexosaminidase level reached similar values to those of the control group. These effects were attributed to the combined allergen-reducing actions of boiling, vinegar, ginger, and shiitake mushroom. Therefore, pickled ark shell containing ginger or shiitake mushrooms has potential as a functional food that can alleviate allergic responses.
Keywords:
allergy reduction, ginger, Scapharca subcrenata, shiitake mushroom, RBL-2H3 cells서 론
알레르기(allergy) 반응은 인체의 면역체계가 알레르겐(allergen) 또는 항원(antibody) 등과 같은 특정 물질을 해로운 인자로 잘못 인식하여 과도하게 반응하는 면역학적 현상이다(Chung MJ 등 2021). 알레르기 반응 시 면역 시스템은 해당 항원에 특이적인 Immunoglobulin E(IgE) 항체를 생성하며, 동일 항원에 재노출될 경우 비만세포에서 β-hexosaminidase, histamine, interleukin-4(IL-4), IL-13, tumor necrosis factor-α(TNF-α) 등이 분비된다. 이러한 물질들은 눈물, 가려움, 발진, 콧물, 재채기 등의 증상을 유발하며, 심한 경우 호흡곤란, 급성 저혈압, 아나필락시스(anaphylaxis)와 같은 중증 알레르기 반응으로 이어질 수 있다(Sicherer SH & Sampson HA 2018; Chung MJ 등 2020).
비만세포(mast cell)는 고친화성 IgE 수용체(FcεRI)를 세포 표면에 발현하고 있으며, IgE 항체가 FcεRI에 결합한 상태에서 항원(알레르겐)이 침입하면 IgE–FcεRI 복합체의 교차결합(cross-linking)이 일어나면, 비만세포는 탈과립(degranulation) 과정을 통해 β-hexosaminidase, histamine 및 다양한 cytokine 등의 염증 매개물질을 방출하여 알레르기 증상이 나타난다(Sicherer SH & Sampson HA 2018; Chung MJ 등 2020). RBL-2H3 세포는 rat basophilic leukemia 세포주로, FcεRI를 발현하고 있어 IgE 매개 탈과립 반응을 정량적으로 분석할 수 있으므로 세포 수준 기전을 연구하는 대표적인 in vitro 모델로 활용되고 있다. 그리고 IgE로 감작된 RBL-2H3 세포에서 항원(알레르겐)이 침입한 후 β-hexosaminidase 방출, histamine 분비, cytokine 방출 등은 알레르기 지표 측정에 널리 사용된다(Chung MJ 등 2013).
새꼬막(Scapharca subcrenata)은 대표적인 꼬막류(참꼬막, 새꼬막, 피꼬막) 중 하나로서 돌조개목(Arcoida), 돌조개과(Arcidae), 피조개속(Scapharca)에 속한다(Choi SS 등 2023). 우리나라에서는 연근해 어업 및 해면 양식업을 통해 생산되고 있다(Choi SS 등 2023).꼬막은 고단백질, 저지방 식품이며 필수 아미노산, 무기질 및 비타민이 풍부한 것으로 보고되어 있다(Park CK 2000).
트로포미오신(tropomyosin)은 조개류와 갑각류에 존재하는 주요 알레르기 유발 단백질로, 열에 안정하며 고도로 보존된 IgE 결합 에피토프를 가지기 때문에 알레르기 반응을 유발한다(Fujinoki M 등 2006; Fedoseeva VN 등 2009; Lopata AL 등 2016; Chung MJ 등 2021). 트로포미오신과 IgE가 결합하면 비만세포가 활성화되어 β-hexosaminidase, histamine, cytokine 등 분비가 촉진된다(Fujinoki M 등 2006; Lopata AL 등 2016; Chung MJ 등 2021).
트로포미오신은 열과 산에 비교적 안정적이라 가열이나 식초 처리만으로 완전 비활성화가 어렵지만, 특정 열처리 조건에서 알레르기 항원성이 일부 감소될 수 있음이 보고되었다(Kamath SD 등 2013; Faber MA 등 2017). 폴리페놀 화합물인 quercetin, chlorogenic acid와 트로포미오신의 공변결합으로 단백질 구조가 변성되어 항알레르기 효과가 있으며, 표고버섯 균사체에도 항알레르기 효과가 있다고 보고되었다(Bae MJ & Ye EJ 2007; Ge X 등 2024). 자외선 조사를 통한 비타민 D2의 함량이 증가된 표고버섯 추출물은 대식세포에서 염증성 cytokine의 분비와 유전자 발현을 억제시키고, RBL-2H3 세포에서 histamine 및 cytokine의 분비를 억제함으로써 항염증 작용 및 알레르기 질환 관련 반응을 완화하는 데 활용될 수 있다고 보고하였다(Hwang MS 등 2022). 생강에 함유된 천연 플라보노이드인 kaempferol은 알레르기가 유발된 RBL-2H3 세포에서 β-hexosaminidase 및 cytokine 생성을 억제하였고, 생강 추출물도 항알레르기 효과가 알려져 있다(Gong JH 등 2012; Chung MJ 등 2020).
따라서 본 연구는 알레르겐인 꼬막 단백질의 비활성화를 목표로 생강과 표고버섯을 첨가해 꼬막 초절임을 제조하고, 그 품질 변화와 알레르기 유발성 저감을 평가하였다.
재료 및 방법
1. 꼬막 초절임 제조
본 연구에 사용된 꼬막은 새꼬막으로 생꼬막살과 자숙 꼬막살은 ㈜벌교꼬막(Boseong, Korea)으로부터 제공받았다. 2배 사과식초(Ottogi, Anyang, Korea), 설탕(Cheiljedang, Seoul, Korea), 소금(Cheiljedang, Seoul, Korea), 월계수 잎(Gomaps, Sydney, Australia), 파(Gwangju, Korea), 마늘(Gwangju, Korea), 양파(Gwangju, Korea), 통후추(Gwangju, Korea), 생강(Gwangju, Korea) 그리고 표고버섯(Gwangju, Korea)은 광주광역시 남구 대형 마트에서 구매하여 사용하였다. 세척 한 생강은 건조하였고, 표고버섯은 건조한 것을 구입하여 건조한 시료를 분쇄기(SHMF-3250S, Hanil, Seoul, Korea)로 분쇄하여 사용하였다.
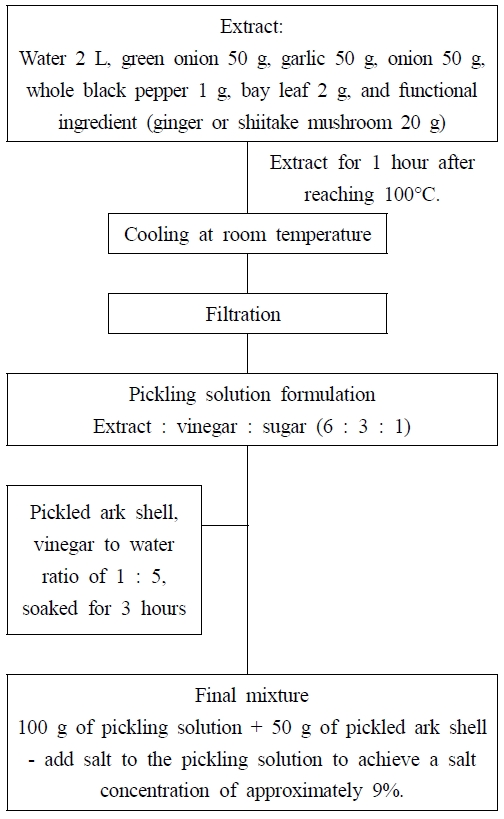
꼬막 초절임 제조 과정은 Fig. 1과 같다. 즉, 물 2 L, 파 50 g, 마늘 50 g, 양파 50 g, 통후추 1 g, 월계수 2 g 그리고 기능성 원료인 생강 또는 표고버섯20 g을 혼합하여 100℃에 도달한 후 1시간 동안 추출하였다. 추출물은 실온에서 냉각한 뒤 커피 여과지를 사용하여 여과하였고, 초절임 제조에 사용하였다. 또한 2배 사과식초와 물을 1:5 비율로 혼합한 희석 식초액에 꼬막살을 1회 3시간 침지하여 준비하였다. 초절임액은 추출물과 2배 사과식초, 설탕을 6:3:1의 비율로 혼합하여 제조하였으며, 초절임액 100 g에 초절임 꼬막살 50 g을 담아 실험에 사용하였다. 소금의 양은 시판되는 초절임 꼬막인 Parsons Pickles Pickled Cockles(Leslie A. Parsons & Sons(Burry Port) Ltd., Burry Port, UK)의 초절임액을 근거하여 초절임액의 염도가 9% 정도가 되도록 첨가하였다. 생강 또는 표고버섯이 함유된 꼬막살 초절임은 각각 생강 함유 꼬막 초절임(pickled ark shell containing ginger)과 표고버섯 함유 꼬막 초절임(pickled ark shell containing shiitake mushroom)으로 명명하였고, 초절임에 함유된 꼬막살에 동량의 증류수를 넣고 분쇄 후 원심분리하여 얻은 상층액을 각각 PASG와 PASSM이라고 하였다. 생꼬막살(raw ark shell meat)과 자숙꼬막살(boiled ark shell meat)도 동량의 증류수를 넣어 분쇄 후 원심분리하여 얻은 상층액을 RAS와 BAS이라 하였다.
2. 꼬막 초절임액의 pH, 염도 및 당도 측정
꼬막 초절임액의 pH는 pH meter(Orion 420A, Thermo Scientific, Waltham, MA, USA)를 사용하여 측정하였다. 염도는 디지털 염도계(Digital Salt Refractometer, PAL-30S, Atago, Tokyo, Japan)를 사용하여 측정하였고, 당도는 디지털 당도계(Digital Brix Refractometer, PAL-3, Atago, Tokyo, Japan)를 사용하여 측정하였다. 모든 실험은 3회 반복으로 측정하였으며, 그 평균값을 구하였다.
3. RBL-2H3 세포 배양
RBL-2H3 세포(rat basophilic leukemia cells)는 한국세포주은행(Korean Cell Line Bank, Seoul, Korea)에서 분양받아 사용하였다. 세포는 Dulbecco’s Modified Eagle Medium(DMEM; WelGene Co., Daegu, Korea)에 10% fetal bovine serum(FBS; WelGene Co., Daegu, Korea)과 1% penicillin/streptomycin(PEST; WelGene Co., Daegu, Korea)을 첨가한 배양액에서 배양하였다. 모든 세포는 37℃, 5% CO2, 습도가 유지되는 배양기(BB 15, ThermoFisher Scientific, Waltham, MA, USA)에서 배양하였다. 세포 밀도가 약 80%에 도달하면 phosphate-buffered saline(PBS, pH 7.4; WelGene Co., Daegu, Korea)으로 세포층을 세척한 후 trypsin-EDTA(×1; WelGene Co., Daegu, Korea) 용액을 처리하여 부착 세포를 분리하고, 새로운 배양 접시에 옮겨 계대 배양하였다. 배양액은 약 2일 간격으로 교환하였다.
4. 시료 처리
RBL-2H3 세포를 24-well plate에 well 당 5 × 105 cells의 밀도로 접종하여 48시간 동안 배양하였다. 이후 배지를 FBS이 포함되지 않은 serum-free medium(SFM)으로 교체하고, 2시간 동안 추가 배양하였다. 이후 250 ng/mL의 dinitrophenyl-immunoglobulin E(DNP-IgE; Sigma-Aldrich Co., St Louis, MO, USA)가 포함된 배지로 교환하여 24시간 동안 배양하였다. 배양이 완료된 세포는 Siraganian buffer 1(119 mM NaCl, 5 mM KCl, 0.4 mM MgCl2, 25 mM PIPES, pH 7.2)로 한 차례 세척한 뒤, Siraganian buffer 2(119 mM NaCl, 5 mM KCl, 1 mM CaCl2, 0.4 mM MgCl2, 25 mM PIPES, 5.6 mM glucose, 0.1% bovine serum albumin, pH 7.2)로 교체하고 10분간 배양하였다. 이후, 알레르기 반응 조건에서 RAS 및 BAS의 영향을 평가하기 위해 SFM으로 RAS 및 BAS를 100배 희석한 배지를 교체하고 2시간 동안 배양하였다. 그 다음, 10 μg/mL의 dinitropheny-human serum albumin(DNP-HSA; Sigma-Aldrich Co., St Louis, MO, USA)이 포함된 SFM으로 배지를 교환하여 2시간 동안 추가 배양하였다. 그다음에 세포는 얼음 위에서 10분간 냉각시켜 반응을 정지시켰다. 시료의 알레르겐(allergen) 활성을 평가하기 위해 DNP-HSA(항원) 대신 RAS, BAS, PASG, PASSM 시료를 각각 100배 및 250배로 희석하여 동일한 조건에서 세포에 처리하였다. 배양액은 회수하여 β-hexosaminidase 분비량 분석을 위해 35 μL를 사용하였으며, 잔여 배양액은 5,000 rpm에서 10분간 원심분리하였다. 상층액은 —20℃에서 보관하였고, 이후 cytokine 분석용으로 사용하였다.
5. 세포 생존율 측정
세포 생존율은 Chung MJ 등(2020)의 방법을 일부 변형한 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide(MTT; Sigma-Aldrich Co., St Louis, MO, USA) 방법으로 측정하였다. 시료의 세포독성은 β-hexosaminidase 분비량 측정과 동일한 조건에서 측정하였고, 시료 처리 후 배양 시간은 24시간으로 하였다. 시료 처리 시간이 완료되면 각 well에 배양액 부피의 1/10에 해당하는 5 mg/mL 농도의 MTT 용액을 첨가하고, 37℃에서 4시간 동안 배양하였다. 반응 종료 후 배지를 조심스럽게 제거한 후 실온에서 약 30분간 건조시켰다. 이후, dimethyl sulfoxide(DMSO; Sigma‑Aldrich Co., St Louis, MO, USA)를 첨가하여 형성된 formazan을 용해하였으며, 생성된 용액의 흡광도는 UV/Visible spectrophotometer(Ultrospec 3000, Pharmacia Biotech, Uppsala, Sweden)로 570 nm에서 측정하였다. DMSO를 공시료(blank)로 사용하였고, 세포 생존율은 다음 식과 같이 계산하였다.
6. β-Hexosaminidase 분비량 측정
β-Hexosaminidase 활성은 96-well plate에서 측정하였다. 각 e-tube에 시료 처리에서 언급한 상층액 35 μL와 기질 완충용액(0.1 M sodium citrate, pH 4.5에 용해된 2 mM 4-p-nitrophenyl-N-acetyl-β-D-glucosaminide) 35 μL를 혼합한 뒤, 37℃에서 1시간 동안 반응시켰다. 반응 후, 0.1 M Na2CO3/NaHCO3(pH 10.0) 200 μL를 첨가하여 반응을 정지시키고, 생성된 p-nitrophenol의 흡광도를 405 nm 파장에서 측정하였다.
7. TNF-α 함량 측정
세포 배양 상층액 내 rat TNF-α의 함량은 ELISA kit(Abcam, Cambridge, MA, USA)를 이용하여 제조사의 지침에 따라 측정하였다. 흡광도는 microplate reader(AMR-100, Allsheng Co., Ltd, Hangzhou, China)를 사용하여 450 nm 파장에서 측정하였다.
8. 통계처리
모든 실험 결과는 평균(mean)±표준편차(standard deviation; SD)로 나타내었다. 실험군 간의 평균 차이는 일원분산분석(one-way ANOVA)을 실시하여 검정하였으며, 사후 검정은 Duncan’s multiple range test를 이용하였다. 통계적 유의성은 p<0.05 수준에서 판단하였고, 모든 분석은 SPSS 통계 프로그램(version 27.0, IBM Corp., Armonk, NY, USA)을 사용하여 수행하였다.
결과 및 고찰
1. 저장 기간 중 꼬막 초절임액의 pH, 염도 및 당도 변화
생강 함유 꼬막 초절임액 및 표고버섯 함유 꼬막 초절임액의 pH, 염도, 당도 변화를 자숙 꼬막살 첨가 전(BPS), 첨가 후 1, 2, 3, 4, 5일 및 2주차에 측정한 결과는 Fig. 2과 같다.
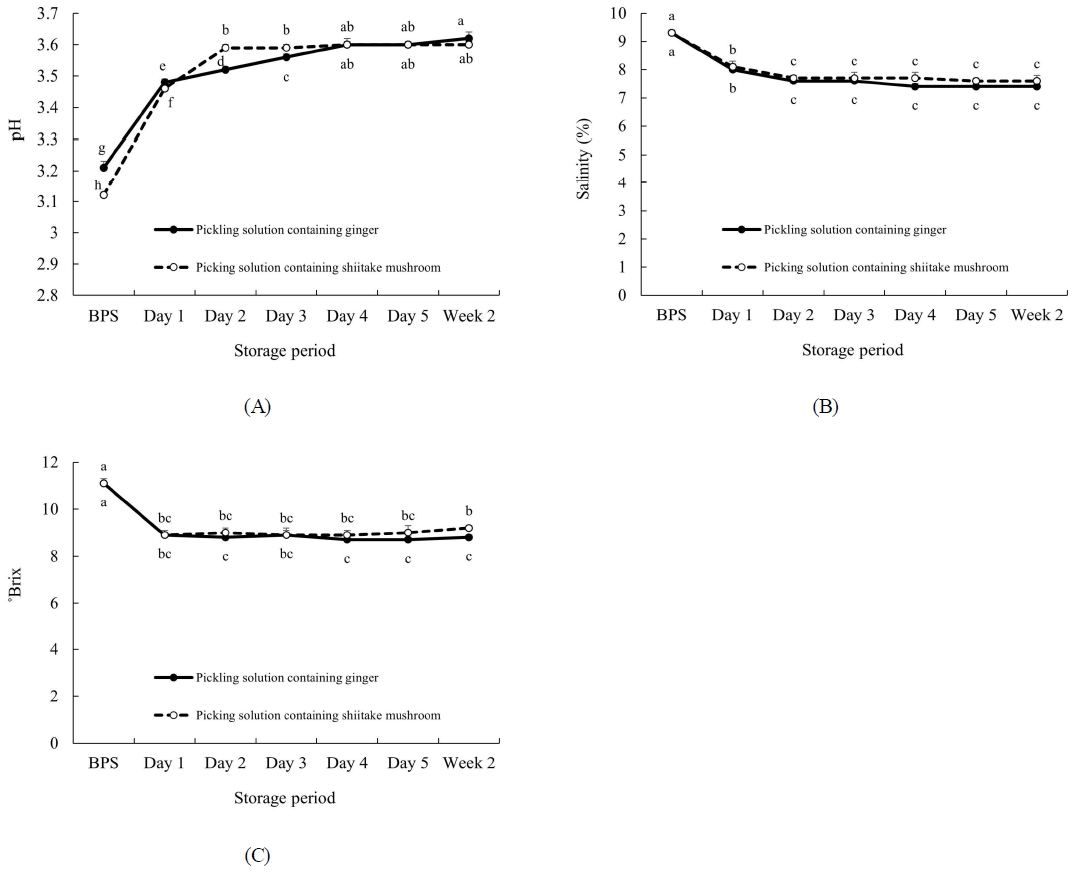
pH (A), salinity (B), and °Brix (C) of pickling solution containing ginger or shiitake mushroom for pickled ark shell. BPS, picking solution before addition of boiled ark shell meat. Day 1∼5 and week 2 indicate the storage period of the picking solution after the addition of boiled ark shell meat. Values are expressed as mean±S.D. (n=3). Means followed by different letters within the same sample are significantly different (p<0.05) according to Duncan’s multiple range test.
두 초절임액의 pH는 저장 기간이 증가할수록 4일까지 상승하는 경향을 보였으며, 자숙 꼬막살 첨가 전(BPS)과 1일까지는 생강 함유 초절임액의 pH가 표고버섯 함유 초절임액보다 유의적으로 높았고, 2일과 3일에는 표고버섯 함유 초절임액의 pH(2일 3.59±0.01, 3일 3.59±0.01)가 생강 함유 초절임액의 pH(2일 3.52±0.01, 3일 3.56±0.01)보다 높았다. 그러나 4일 이후에는 두 초절임액 간 유의적 차이가 나타나지 않았다(Fig. 2A).
염도는 생강 함유 초절임액(BPS 9.3±0.1%, 1일 8.0±0.2%, 2일 7.6±0.2%)과 표고버섯 함유 초절임액(BPS 9.3±0.1%, 1일 8.1±0.2%, 2일 7.7±0.1%) 모두 저장 2일까지 감소하였으며, 전 기간 동안 두 시료 간의 유의적인 차이는 없었다(Fig. 2B).
당도는 자숙 꼬막살 첨가 1일 후 생강 함유 초절임액(BPS 11.1±0.2 °brix, 1일 8.9±0.1 °brix)과 표고버섯 함유 초절임액(BPS 11.1±0.2 °brix, 1일 8.9±0.2 °brix) 모두 자숙 꼬막살 첨가 전과 비교하여 유의적으로 감소하였으나 이후 일정하게 유지되었다. 저장 5일까지는 두 초절임액 간 차이가 없었으나, 2주차에는 표고버섯 함유 초절임액(9.2±0.1 °brix)의 당도가 생강 함유 초절임액(8.8±0.1 °brix)보다 높았다(Fig. 2C).
Kim MH & Han YS(2016)는 저장 기간 동안 양하 피클의 pH가 첨가된 간장 농도가 높을수록 pH 변동이 적었으며, 저장 초기 15일까지는 급격히 pH가 감소하다가 45일 이후 서서히 증가하는 경향을 보였다고 하였다. 이는 간장의 유리 아미노산이 완충 작용을 하여 pH 변화를 완만하게 만든 것이라 하였다. 본 연구에서는 꼬막 초절임액의 pH 변화 역시 꼬막의 유리 아미노산이 완충 작용을 하여 4일까지 pH가 상승하고 이후에는 완만한 변화를 보였을 것으로 추정된다.
한편, Kim JN 등(2015)은 저장 기간 동안 맛나지의 pH가 감소하는 반면, 전통 방법으로 제조한 맛나지는 염도와 당도가 증가하였으나 가열 처리한 맛나지는 염도와 당도가 감소하는 경향을 보고했으며, 본 연구의 꼬막 초절임액도 염도와 당도가 감소하는 유사한 경향을 나타내었다. 저장 중 염도와 당도가 낮아진 이유는 초절임액에 포함된 당과 소금이 자숙 꼬막 조직 내로 침투했기 때문으로 추정된다. 배추 절임 시간이 증가함에 따라 염의 침투 속도가 점차 완만해지는 현상이 보고되었으며(Kim JM 등 1987; Kim HJ 등 2018), 본 연구에서도 시간이 지남에 따라 당과 소금의 자숙 꼬막 내 침투 속도가 완만해져 염도와 당도의 변화가 미비한 것으로 사료된다. 실제로 염도는 저장 3일차부터, 당도는 2일차부터 거의 변화가 없었다. 한편, pH가 상승하는 이유는 초절임액 내 식초 성분이 자숙 꼬막 조직에 침투한 결과로 보인다. 이러한 pH 상승은 식초 내 산이 꼬막살 내부로 확산되면서 발생하는 것으로 사료된다.
2. IgE-처리 RBL-2H3 세포 및 IgE-Antigen 복합체로 알레르기가 유도된 RBL-2H3 세포에서 생꼬막살과 자숙 꼬막살이 β-Hexosaminidase 분비에 미치는 영향
IgE를 처리한 RBL-2H3 세포 및 IgE-antigen 복합체로 알레르기를 유도한 RBL-2H3 세포에 생꼬막살(raw ark shell meat)과 자숙꼬막살(boiled ark shell meat)을 각각 동량의 증류수로 균질화하고 원심분리하여 얻은 상층액(RAS, BAS)을 배지로 100배 희석하여 처리한 후 세포 생존율과 β-hexosaminidase 분비에 미치는 영향을 확인하였다(Fig. 3A, 3B, Fig. 4). RAS와 BAS 모두 세포 생존율에 영향을 미치지 않았다(Fig. 3A, 3B).
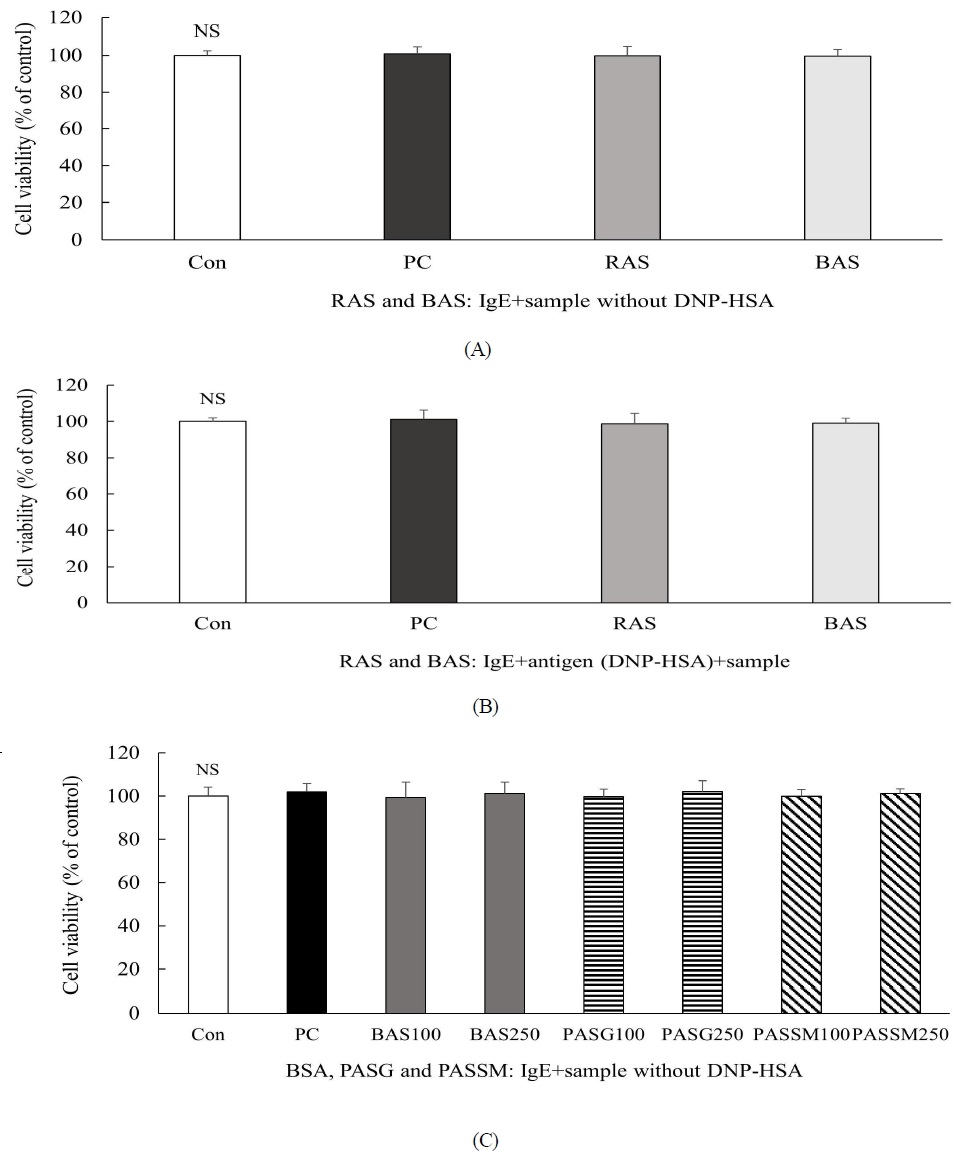
Cytotoxic effects of raw and boiled ark shell meat (RAS, BAS) and pickled ark shell containing ginger (PASG) or shiitake mushroom (PASSM) on IgE-treated and IgE-antigen (DNP-HSA) complex-stimulated RBL-2H3 cells. Con (control), without DNP-HSA and sample; PC (positive control), IgE + DNP-HSA. The values are expressed as mean±S.D. (n=3); NS, not significantly different from each other (p<0.05) as determined by Duncan’s multiple range test. The samples in (C) were diluted 100 times and 250 times, respectively. The samples in (A, B) were diluted 100 times.
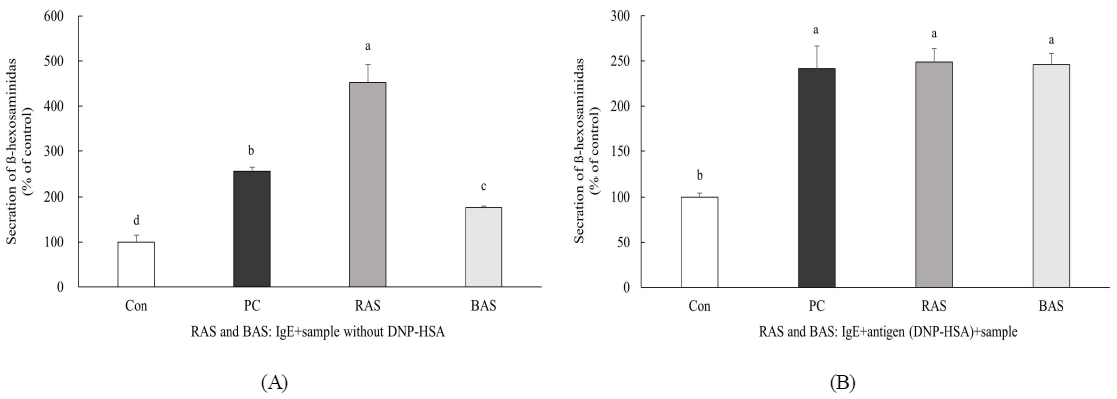
Effect of raw and boiled ark shell meat (RAS, BAS) on β-hexosaminidase release in IgE-treated RBL-2H3 cells (A) and IgE-antigen (DNP-HSA) complex-stimulated RBL-2H3 cells (B). Con (control), without DNP-HSA and sample; PC (positive control), IgE + DNP-HSA. Values are expressed as mean±S.D. (n=3). Means followed by different letters are significantly different (p<0.05) according to Duncan’s multiple range test. The samples were diluted 100 times.
RBL-2H3 세포에서 꼬막살이 알레르겐으로 작용할 가능성을 평가하기 위해 IgE만 처리한 세포에 DNP-HSA 대신 RAS를 처리한 결과(452.9±39.2%), 대조군(Con, antigen과 시료 무처리군 100.0±15.2%)과 양성 대조군(PC, IgE-antigen 복합체 처리군 255±9.2%)에 비해 β-hexosaminidase 분비량이 유의적으로 증가하였다(Fig. 4A). 이는 생꼬막살 단백질이 알레르겐으로 강하게 작용함을 의미한다. 반면 BAS 처리군의 β-hexosaminidase 분비는 PC보다 유의적으로 낮았으나, 대조군(IgE만 처리)보다는 높았다. 따라서 자숙 과정은 꼬막 내 알레르겐의 활성 일부를 불활성화시키지만, 완전한 저감화에는 이르지 못함을 알 수 있었다.
한편, IgE-antigen 복합체로 알레르기를 유도한 세포에서 RAS와 BAS 처리는 β-hexosaminidase 분비에 유의한 영향을 주지 않았다(Fig. 4B).
근육 단백질인 트로포미오신(tropomyosin)은 꼬막의 주요 알레르겐으로 알려져 있으며(Fujinoki M 등 2006; Lopata AL 등 2016; Chung MJ 등 2021), 높은 열 안정성과 보존된 IgE 결합 에피토프(IgE-binding epitopes)를 가지고 있다. 따라서 트로포미오신이 함유된 식품이 체내로 흡수될 경우 IgE와 결합하여 알레르기 반응을 유발할 수 있다(Lopata AL 등 2016; Chung MJ 등 2021).
Kamath SD 등(2013)은 갑각류와 홍합 등에서 트로포미오신이 확인되었으며, 생(raw) 시료와 가열(heat-treated) 시료 간 트로포미오신의 단백질 형태가 다름을 보고하였다. 즉, 가열 처리는 트로포미오신 단백질 구조를 변성시켜 검출 형태에 영향을 주지만, 그 알레르겐성을 완전히 제거하지는 못한다고 하였다.
본 연구에서는 자숙 과정에 의해 트로포미오신 및 관련 알레르겐 단백질이 부분적으로 변성되어 β-hexosaminidase 분비가 감소하였으나, 알레르기 반응성을 완전히 억제하지는 못하였다는 것을 확인하였다. 따라서 기존의 자숙 처리만으로는 완전히 억제되지 않는 꼬막의 알레르기 반응을 효과적으로 저감시키기 위해, 항알레르기 활성을 가진 천연 소재를 첨가한 초절임 꼬막 제품을 개발하였다.
3. IgE-처리 RBL-2H3 세포에서 생강 함유 꼬막 초절임 및 표고버섯 함유 꼬막 초절임이 β-Hexosaminidase 분비에 미치는 영향
자숙 꼬막살을 이용하여 생강 또는 표고버섯을 함유한 꼬막 초절임을 제조한 후, 이들의 알레르기 저감화 효과를 평가하기 위해 IgE로 감작된 RBL-2H3 세포에 처리하였다. 제조된 초절임에서 꼬막을 분리한 뒤, 동량의 증류수를 가하여 균질화하고 원심분리하여 얻은 상층액을 시료로 사용하였다. 생강 함유 꼬막 초절임과 표고버섯 함유 꼬막 초절임은 각각 PASG와 PASSM으로 명명하였으며, 자숙 꼬막 시료(BAS)와 비교하였다. BAS, PASG, PASSM을 각각 배지로 100배 및 250배 희석하여 세포에 처리한 결과, 모든 시료 처리군에서 세포 생존율이 대조군과 비교하여 유의적 차이가 없어 세포독성이 나타나지 않았다는 것을 알 수 있었다(Fig. 3C).
IgE로 감작된 RBL-2H3 세포에서의 β-hexosaminidase 분비 측정 결과, 100배 희석 처리군에서 PASG100(108.8±10.2%) 및 PASSM100(108.8±6.9%) 처리군은 BAS100(173±9.3%)처리군에 비해 현저히 낮은 탈과립 반응을 보였다(Fig. 5). BAS의 경우 100배 희석 처리보다 250배 희석 처리에서 β-hexosaminidase 분비가 다소 감소하였으나, PASG와 PASSM은 두 농도 모두에서 IgE만 처리한 대조군 수준으로 분비가 감소하였다.
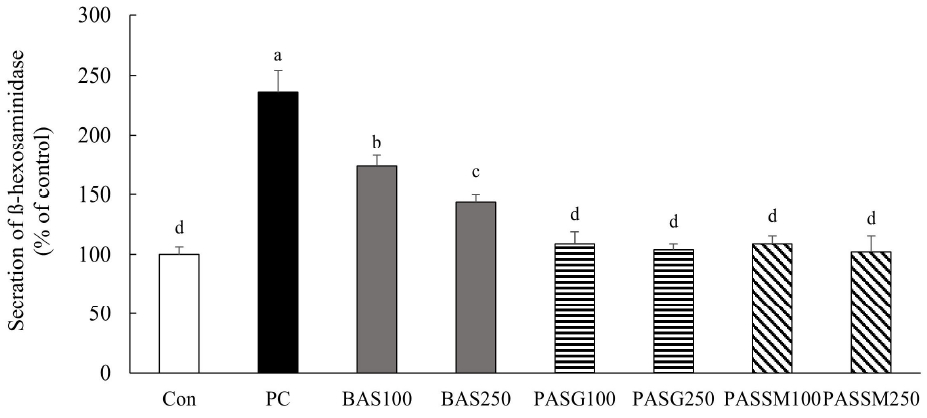
Effect of pickled ark shell containing ginger (PASG) or shiitake mushroom (PASSM) on β-hexosaminidase release in IgE-treated RBL-2H3 cells. Con (control), without DNP-HSA and sample; PC (positive control), IgE + DNP-HSA; BAS, boiled ark shell meat. Values are expressed as mean±S.D. (n=3). Means followed by different letters are significantly different (p<0.05) according to Duncan’s multiple range test. The samples were diluted 100 times and 250 times, respectively.
이 결과는 초절임 과정에 포함된 식초, 생강, 표고버섯 등이 꼬막 내 알레르겐 단백질의 활성 또는 안정성을 억제하여 알레르기 반응을 저감시켰음을 시사하였다. Chung MJ 등(2021)은 자숙 꼬막을 식초 함유 초절임액에 침지할 경우 β-hexosaminidase 분비가 감소하며, 이는 식초가 알레르겐 단백질 일부를 불활성화시킨 결과라고 보고하였다. 본 연구에서도 유사하게, 식초 기반 초절임 과정이 알레르겐 활성을 완화시키는 데 기여한 것으로 보인다.
표고버섯에는 β-glucan이 풍부하게 함유되어 있으며, 이는 대식세포 등 면역세포를 활성화 또는 조절하여 면역 반응을 증진시키는 것으로 알려져 있다(Roszczyk A 등 2022). 또한, 표고버섯에서 추출한 비타민 D2는 대식세포에서 염증성 사이토카인의 분비와 유전자 발현을 억제하고, 비만세포에서는 histamine과 cytokine 분비를 저해하여 염증 및 알레르기 반응을 완화하는 항염증 및 항알레르기 효과가 보고되었다(Hwang MS 등 2022). 생강의 주요 활성 성분인 kaempferol은 항알레르기 효과를 가지며, 특히 알레르기 매개체의 분비와 염증 반응을 억제하는 것으로 알려져 있다(Gong JH 등 2012).따라서 β-glucan, 비타민 D2 및 kaempferol 등 천연 항알레르기 성분이 꼬막 초절임의 알레르기 저감 효과에 기여하였을 것으로 사료된다.
선행연구에 따르면, 생강 추출물은 IgE-antigen 복합체로 유도된 RBL-2H3 세포에서 β-hexosaminidase 방출을 유의적으로 억제하였으며, 이들 추출물에 함유된 플라보노이드 화합물은 사이토카인(IL-4, IL-13, TNF-α) 생성을 감소시키는 항알레르기 활성을 보였다(Chung MJ 등 2020). 표고버섯 균사체 추출물 또한 IL-4 생성 억제 및 β-hexosaminidase 저해 효과를 나타내어 알레르기 반응을 완화한다고 보고되었다(Bae MJ & Ye EJ 2007). 또한 Ge X 등(2024)은 새우의 주요 알레르겐인 트로포미오신을 폴리페놀 화합물(quercetin, chlorogenic acid)과 공변결합(covalent conjugation)시켜 단백질 구조를 변성함으로써 β-hexosaminidase 및 히스타민 방출을 감소시킬 수 있음을 보고하였다. 이는 본 연구에서 생강 및 표고버섯의 폴리페놀 성분이 꼬막 내 알레르겐 단백질과 상호작용하여 구조적 변화를 유도했을 가능성을 뒷받침한다.
결과적으로, 생강 함유 꼬막 초절임(PASG) 및 표고버섯 함유 꼬막 초절임(PASSM)은 IgE-처리 RBL-2H3 세포에서 β-hexosaminidase 분비량을 대조군 수준으로 감소시켰다. 이는 자숙 과정에 따른 알레르겐 변성뿐 아니라, 초절임액 내 식초와 천연 항알레르기 물질(생강, 표고버섯)의 복합 작용에 의한 것으로 해석된다. 따라서 생강 및 표고버섯 함유 꼬막 초절임은 알레르기 반응을 효과적으로 완화하는 식품으로 활용될 가능성을 보여주었다.
4. IgE-처리 RBL-2H3 세포에서 생강 함유 꼬막 초절임 및 표고버섯 함유 꼬막 초절임이 TNF-α 분비에 미치는 영향
IgE로 감작된 RBL-2H3 세포에 BAS, PASG, PASSM을 각각 100배 및 250배로 희석하여 처리한 후 TNF-α 분비량을 측정한 결과는 Fig. 6에 나타내었다. BAS의 경우 250배 희석 시료(29.4±0.9 pg/mL)에서 TNF-α 분비량이 100배 희석군(34.9±0.5 pg/mL)보다 감소하였으나, PASG와 PASSM 처리군에서는 두 희석 농도 간 유의적인 차이가 나타나지 않았다. 100배 희석군에서 BAS, PASG 그리고 PASSM 처리군의 TNF-α 함량은 각각 34.9±0.5, 23.9±2.7 그리고 24.4±2.6 pg/mL 이었다. PASG와 PASSM 처리군 모두 BAS에 비해 TNF-α 분비량이 현저히 낮게 나타나 알레르기 저감화 효과를 확인할 수 있었다.
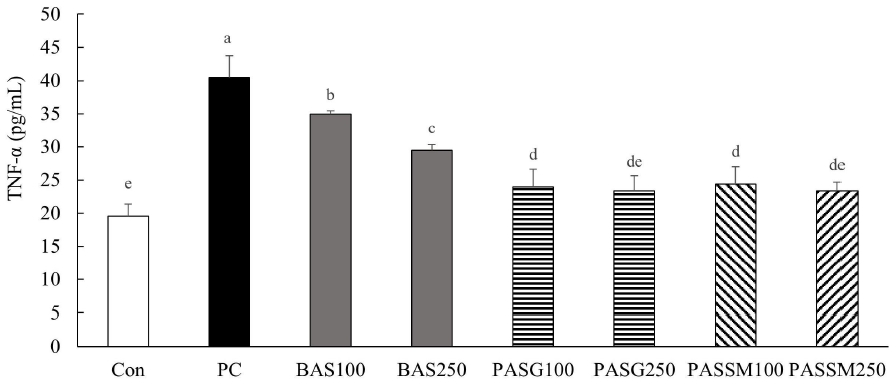
Effect of pickled ark shell containing ginger (PASG) or shiitake mushroom (PASSM) on TNF-α release in IgE-treated RBL-2H3 cells. Con (control), without DNP-HSA and sample; PC (positive control), IgE + DNP-HSA; BAS, boiled ark shell. Values are expressed as mean±S.D. (n=3). Means followed by different letters are significantly different (p<0.05) according to Duncan’s multiple range test. The samples were diluted 100 times and 250 times, respectively.
TNF-α는 비만세포 활성화 및 알레르기 염증 반응의 주요 매개 인자로, 그 분비 억제는 항알레르기 작용의 중요한 지표로 활용된다(Hide I 등 1997). Hide I 등(1997)은 항히스타민제인 azelastine이 RBL-2H3 세포에서 IgE/항원 자극 또는 이온작용제(ionomycin)에 의해 유도된 TNF-α 방출을 효과적으로 억제한다고 보고하였다. Chung MJ 등(2020)은 생강에 함유된 플라보노이드가 IgE-antigen 복합체로 유도된 알레르기 RBL-2H3 세포에서 과생성되는 TNF-α를 현저히 억제한다고 보고하였다. 본 연구에서도 생강 및 표고버섯 함유 꼬막 초절임(PASG, PASSM)이 TNF-α 분비량을 유의적으로 감소시킨 것은 자숙 처리와 더불어 초절임액 내 식초의 작용 및 생강과 표고버섯의 항알레르기 성분(플라보노이드 및 폴리페놀 등)에 기인한 것으로 판단된다.
결과적으로, 생강 함유 꼬막 초절임 및 표고버섯 함유 꼬막 초절임은 IgE-처리 RBL-2H3 세포에서 β-hexosaminidase와 TNF-α 분비를 모두 유의적으로 억제하였다. 이는 두 시료 모두 자숙 꼬막보다 높은 알레르기 저감화 효과를 나타내었으며, 알레르기 반응을 완화할 수 있는 알레르기 저감화 기능성 꼬막 식품으로의 개발 가능성을 보여 주었다.
요 약
이 연구는 생강 또는 표고버섯을 첨가하여 제조한 꼬막 초절임의 품질 변화와 알레르기 유발성 저감 효과를 평가하였다. 저장 기간 동안 두 초절임액의 pH는 4일째까지 증가한 후 안정화되었으며, 염도는 2일까지 감소한 뒤 일정하게 유지되었다. 자숙 꼬막살을 첨가한 후에는 당 함량이 감소하였다. IgE로 감작된 RBL-2H3 세포에서 생꼬막살(RAS)은 β-hexosaminidase 분비량이 IgE만 처리한 대조군과 IgE와 항원(DNP-HSA) 처리 양성 대조군보다 유의적으로 높아 알레르기 유발성을 나타낸 반면, 자숙 꼬막살(BAS)은 RAS보다 β-hexosaminidase 분비량이 유의적으로 낮았다. 생강 함유 꼬막 초절임(PASG)과 표고버섯 함유 꼬막 초절임(PASSM)은 BAS에 비해 β-hexosaminidase와 TNF-α의 분비량이 유의적으로 억제되었고, β-hexosaminidase는 대조군과 유사한 수준에 도달하였다. 이러한 효과는 자숙, 식초, 생강, 표고버섯의 복합적인 알레르기 유발성 저감 효과에 기인하는 것으로 판단된다. 따라서 생강 또는 표고버섯을 첨가한 꼬막 초절임은 알레르기 반응을 완화시킬 수 있는 기능성 식품으로 활용될 잠재력을 가지고 있는 것으로 판단된다.
Acknowledgments
본 성과물은 중소벤처기업부에서 지원하는 “2020년도 지역특화산업육성+(R&D)-지역스타기업육성 사업(No. S2868121)”의 연구수행으로 인한 결과물임을 밝힙니다.
REFERENCES
-
Bae MJ, Ye EJ (2007) Effect of mycelia extracts from Lentinus edodes mushroom-cultured Lonicera japonica thunberg on anticancer and antiallergy activities. J Korean Soc Food Sci Nutr 36(4): 424-430.
[https://doi.org/10.3746/jkfn.2007.36.4.424]

- Choi SS, Yoo SH, Seo YB, Kim JO, Kwon IJ, Bae SH, Kim GD (2023) Development and verification of and single nucleotide polymorphism markers to determine country of origin of Korean and Chinese Scapharca subcrenata. J Life Sci 33(12): 1025-1035.
-
Chung MJ, Goh Eun, Bae SH, Lee SH, Hur JM, Yoo GS, Kim DS (2021) Effects of powder mixtures containing ark shell on IgE-mediated allergic response in RBL-2H3 cells. Food Sci Preserv 28(6): 837-845.
[https://doi.org/10.11002/kjfp.2021.28.6.837]

-
Chung MJ, Lee SH, Kim DS (2020) Anti-allergic effects of onion, apple, cucumber, ginger, and broccoli mixtures and their bioactive compounds in RBL-2H3 cells. Food Sci Preserv 27(7): 973-983.
[https://doi.org/10.11002/kjfp.2020.27.7.973]

-
Chung MJ, Sohng JK, Choi DJ, Park YI (2013) Inhibitory effect of phloretin and biochanin A on IgE-mediated allergic responses in rat basophilic leukemia RBL-2H3 cells. Life Sci 93(9-11): 401-408.
[https://doi.org/10.1016/j.lfs.2013.07.019]

-
Faber MA, Pascal M, Kharbouchi OE, Sabato V, Hagendorens MM, Decuyper II, Bridts CH, Ebo DG (2017) Shellfish allergens: Tropomyosin and beyond. Allergy 72(6): 842-848.
[https://doi.org/10.1111/all.13115]

- Fedoseeva VN, Kamysheva VA, Fedoskova TG, Nekrasova OV (2009) Myofibrillar protein tropomyosin and allergic cross-reactivity. Patol Fiziol Eksp Ter Jan-Mar(1): 13-18.
-
Fujinoki M, Ueda M, Inoue T, Yasukawa N, lnoue R, Ishimoda-Takagi T (2006) Heterogeneity and tissue specificity of tropomyosin isoforms from four species of bivalves. Comp Biochem Physiol B: Biochem Mol Biol 143(4): 500-506.
[https://doi.org/10.1016/j.cbpb.2006.01.002]

-
Ge X, Ju G, Lv X, Sui, X, Zhang Y, Liang L, Yang Q, Wu W, Lv L (2024) Reducing the allergenicity of tropomyosin in shrimp by covalent conjugation with quercetin and chlorogenic acid. Int J Biol Macromol 262(Pt 2): 130099.
[https://doi.org/10.1016/j.ijbiomac.2024.130099]

-
Gong JH, Shin DK, Han SY, Kim JL, Kang YH (2012) Kaempferol suppresses eosinophil infiltration and airway inflammation in airway epithelial cells and in mice with allergic asthma. J Nutr 142: 47-56.
[https://doi.org/10.3945/jn.111.150748]

-
Hide I, Toriu N, Nuibe T, Inoue A, Hide M, Yamamoto S, Nakata Y (1997) Suppression of TNF-alpha secretion by azelastine in a rat mast (RBL-2H3) cell line: Evidence for differential regulation of TNF-alpha release, transcription, and degranulation. J Immunol 159(6): 2932-2940.
[https://doi.org/10.4049/jimmunol.159.6.2932]

- Hwang MS, Pyo J, Kim HJ, Do SG, Song ID, Kim KM (2022) Anti-inflammatory and anti-allergic effects of Lentinula edodes extract by uv irradiation. J Life Sci 32(5): 368-374.
-
Kamath SD, Rahman AMA, Komoda T, Lopata AL (2013) Impact of heat processing on the detection of the major shellfish allergen tropomyosin in crustaceans and molluscs using specific monoclonal antibodies. Food Chem 141(4): 4031-4039.
[https://doi.org/10.1016/j.foodchem.2013.06.105]

-
Kim HJ, Baik MY, Kim BY (2018) Permeation rate of salt and sugar into cabbage pickles and sensory changes during storage. Food Eng Prog 22(4): 366-373.
[https://doi.org/10.13050/foodengprog.2018.22.4.366]

- Kim JM, Kim IS, Yang HC (1987) Storage of salted Chinese cabbages for Kimchi: I. Physicochemical and microbial changes during salting of Chinese cabbages. J Korean Soc Food Sci Nutr 16(2): 75-82.
-
Kim JN, Park YH, Kim Y, Lee JY, Han GJ (2015) Quality characteristics of Mannaji (boiled beef down in Korean soy sauce) by cooking method during storage period. J East Asian Soc Diet Life 25(5): 850-859.
[https://doi.org/10.17495/easdl.2015.10.25.5.850]

-
Kim MH, Han YS (2016) Quality characteristics of Yangha (Zingiber mioga Rosc) pickle with soy sauce during storage. J East Asian Soc Diet Life 26(3): 260-270.
[https://doi.org/10.17495/easdl.2016.6.26.3.260]

-
Lopata AL, Kleine-Tebbe J, Kamath SD (2016) Allergens and molecular diagnostics of shellfish allergy: Part 22 of the series molecular allergology. Allergo J Int 25(7): 210-218.
[https://doi.org/10.1007/s40629-016-0124-2]

- Park CK (2000) Seasonal variation of proximate composition in ark shell (Scapharca subcrenata) tissues. J Korean Soc Food Sci Nutr 29(1): 10-14.
-
Roszczyk A, Turło J, Zagożdżon R, Kaleta B (2022) Immunomodulatory properties of polysaccharides from Lentinula edodes. Int J Mol Sci 23(16): 8980.
[https://doi.org/10.3390/ijms23168980]

-
Sicherer SH, Sampson HA (2018) Food allergy: A review and update on epidemiology, pathogenesis, diagnosis, prevention, and management. J Allergy Clin Immunol 141(1): 41-58.
[https://doi.org/10.1016/j.jaci.2017.11.003]