시판 분리대두단백의 이화학적 및 기능적 특성
Abstract
This study compared the physicochemical and functional properties of seven commercial soy protein isolates (SPIs) to evaluate their potential applications. The analysis of physicochemical properties revealed that the crude protein contents ranged from 82.87% to 86.90%, below the 90% standard for SPIs. The CH1, CH2, and CH3 samples contained no detectable crude fat but had higher ash contents, with CH1 exhibiting the highest levels of most amino acids. The US1 and US2 samples showed the highest lightness values, appearing closest to white, although the visual differences among the samples were minimal. In the functional property analysis, US1 showed the greatest water absorption capacity, and CH2 showed the highest oil absorption capacity. Also, CH1, CH2, and CH3 showed the greatest foaming capacities. Foam stability was significantly higher in US1 and US2. Emulsifying capacity was high in US1, CH1, CH2, and CH3, with CH2 showing the highest emulsion stability. The least gelation concentration was significantly higher in the SI1 sample than in the other samples. Sodium dodecyl sulfate-polyacrylamide gel electrophoresis (SDS-PAGE) revealed distinct 7S protein bands in CH1, CH2, and CH3, whereas US1, US2, SI1, and SI2 showed weak or undetectable bands. Differential scanning calorimetry (DSC) analysis indicated flat thermograms without thermal transitions for US1, US2, SI1, and SI2, while CH1, CH2, and CH3 exhibited an exothermic peak at 25-30℃. Overall, the findings demonstrated that the physicochemical and functional properties of commercial SPIs vary substantially depending on the origin of the raw material, extraction conditions, and purification methods, underscoring the importance of selecting appropriate SPIs for specific food applications.
Keywords:
Glycine max (L.) Merr., soybean, soy protein, soy protein isolate서 론
최근 지속 가능한 식품 소비에 대한 관심이 증가함에 따라, 식물성 단백질을 기반으로 한 식품 소재의 수요가 전 세계적으로 확대되고 있다(Lee EJ 등 2021). 특히, 식물성 단백질은 동물성 단백질에 비해 포화지방과 콜레스테롤 함량이 낮고, 환경적 지속 가능성이 우수하여 건강 지향 및 친환경 식품 시장에서 핵심 원료로 주목받고 있다(Kim SH 2023; Lee SY 등 2023). 이러한 흐름은 육류 대체식품, 기능성 건강식품, 단백질 보충식 등 다양한 식품 분야에서 식물성 단백질의 활용 확대를 이끌고 있으며, 그중 대두(Glycine max (L.) Merr.)는 높은 단백질 함량과 우수한 아미노산 조성으로 인해 대표적인 식물성 단백질 공급원으로 널리 활용되고 있다(Kim YA 2018; Kim YJ 등 2023).
대두로부터 추출한 분리대두단백(soy protein isolate; SPI)은 대두단백 중에서도 단백질 함량이 90% 이상으로 유화성, 기포성, 겔 형성능 등 우수한 기능적 특성으로 인해 식품산업 전반에 걸쳐 다양한 용도로 사용되고 있다(Park HJ 등 2020; Zheng L 등 2022). 특히 제빵, 육가공품, 단백질 음료, 드레싱, 소스류 등의 소재로 활용도가 높아지고 있으며, 최근에는 비건 및 고단백 식품 개발을 위한 핵심 소재로도 각광받고 있다(Zhang T 등 2021; Meganaharshini M 등 2023). 분리대두단백의 기능적 특성은 제조 과정에 따라 달라질 수 있다. Monteiro SR & Lopes-da-Silva JA(2019)는 탈피·탈지 등 원료 전처리와 가공 공정 조건이 단백질의 구조, 변성 정도, 응집 상태를 변화시켜 기능적 특성에 큰 영향을 미친다고 보고하였으며, Hu Z 등(2023)은 가열이나 알칼리 처리 등의 공정에 따라 분리대두단백의 구조적 특성과 겔 형성력과 같은 특성이 달라질 수 있음을 시사한 바 있다.
한편, 현재 국내에서 사용되는 분리대두단백은 전량 수입에 의존하고 있으며, 관세청 통계에 따르면 주요 수입국은 중국과 미국으로 나타났다(Lee EJ 등 2021; Korea Customs Service 2023). 또한 식물성 단백질 산업을 전략적으로 육성하고 있는 싱가포르 제품이 국내 시장에 유통되고 있는 것으로 확인된다(Pay C & Gianoli A 2024). 수입산 제품에 대한 의존도가 높을 경우 원료 공급 안정성과 산업 경쟁력 유지에 한계가 따를 수 있으며, 이에 따라 국내산 대두를 활용한 분리대두단백 개발의 필요성이 있다. 앞서 언급하였듯이 분리대두단백은 원산지 및 제조 공정에 따라 품질 특성이 달라져 최종 제품 가공적성에도 영향을 미칠 수 있다. 따라서 가공 목적에 적합한 분리대두단백을 선정하기 위해서는 제품별 특성에 대한 체계적인 비교가 필요하다. 그러나 현재 국내에 보고된 분리대두단백 관련 연구는 분리대두단백을 활용한 소시지 제조(Kim HW 등 2009), 분리대두단백 고단백 바의 소비자 기호 분석(Park HJ 등 2020), 분리대두단백 함량에 따른 식물조직단백의 특성 분석(Hwang NK 등 2023) 등 주로 제품 응용 중심으로 이루어지고 있으며 특성 분석에 관한 연구는 미비하다. 이러한 실정에 산업 현장에서는 경험이나 가격 위주로 제품 선정이 이루어지고 있다. 따라서 현재 국내 유통 중인 제품들의 품질 특성과 수준을 파악하는 것은 향후 국산 제품 개발 및 식품 가공 현장에서 활용 시 유용한 기초자료가 될 수 있다. 이에 본 연구에서는 국내에서 유통 중인 수입산 분리대두단백 제품 중 무작위로 선정한 7종(미국산 2종, 싱가포르산 2종, 중국산 3종)을 대상으로 이화학적 및 기능적 특성을 비교·분석하였다.
재료 및 방법
1. 실험재료
본 실험에 사용된 분리대두단백 시료는 국내 온라인 쇼핑몰에서 시판 중인 제품 중 무작위로 7종을 선정하여 구매하였다. 선정된 제품은 원산지에 따라 미국산 2종(US1, US2), 싱가포르산 2종(SI1, SI2), 중국산 3종(CH1, CH2, CH3)으로 분류되었다. 모든 시료는 구입 직후 폴리에틸렌백에 밀봉하여 4℃ 이하에서 냉장 보관하며 분석에 사용하였다.
2. pH 및 일반성분
분리대두단백의 pH 측정을 위해 각 시료를 증류수에 10배 희석하여 300 rpm으로 30 min 동안 교반한 후, 4,000×g로 10 min 동안 원심분리(Combi 508, Hanil, Inc., Gimpo, Korea)하였다. 원심분리 후 시료의 상층액의 pH를 pH meter(Star A211, Thermo Fisher Scientific, Inc., Waltham, MA, USA)를 이용하여 측정하였다. 분리대두단백의 일반성분 분석은 식품공전 일반시험법에 준하여 측정하였다(MFDS 2024). 즉, 수분은 상압가열건조법, 조단백질은 Kjeldahl법에 따라 분석하였으며, 조단백질 함량 산출 시 질소-단백질 환산계수를 국제적으로 정의된 SPI 기준에 따라 6.25로 적용하여 계산하였다(Codex Alimentarius 2019). 조지방은 Soxhlet 추출법, 조회분은 건식회화법에 따라 분석하였으며, 탄수화물은 시료 전체를 100% 기준으로 하고 수분, 조회분, 조단백질, 조지방 함량을 감하여 계산하였다.
3. 구성 아미노산
분리대두단백의 구성 아미노산 분석을 위해 산 안정 계열, 황 함유 계열, 그리고 트립토판으로 구분하여 각각 전처리하였다. 산 안정 계열 아미노산은 시료 50∼300 mg(조단백질 기준 10 mg)에 6 N HCl 10 mL를 첨가하여 110℃에서 22 hr 가수분해하였다. 황 함유 계열 아미노산은 동일한 시료에 과개미산으로 전처리한 후, 6 N HCl 10 mL를 가하여 동일한 조건(110℃, 22 hr)에서 가수분해하였다. 트립토판은 시료에 4.2 N NaOH를 첨가한 후, 질소 치환 하에 110℃에서 20 hr 가수분해하였다. 가수분해물은 Whatman 여과지(No. 1, Cytiva LLC, Maidstone, UK)로 여과한 후, 0.2 M sodium citrate buffer(pH 4.2)를 사용하여 25 mL로 정용하였다. 아미노산 분석은 자동 아미노산 분석기(L-8900, Hitachi, Tokyo, Japan)를 사용하였으며, 이동상으로는 PH1, PH2, PH3, PH4, PH-RG를 사용하였다. 분석에 사용된 컬럼은 Hitachi custom ion exchange column이며, 컬럼 온도는 57℃, 반응 챔버 온도는 135℃로 설정하였다.
4. 색도
색도는 각 시료를 Ø35 × 10 mm의 투명 cell에 가득 담은 후 비색계(UltraScan VIS, Hunterlab, Reston, VA, USA)를 사용하여 반사광 모드에서 명도(lightness, L), 적색도(redness, a), 황색도(yellowness, b), 그리고 색차(ΔE) 값을 측정하였다. 표준 색판으로는 백판(L=98.14, a=0.01, b=0.21)을 사용하였다.
5. 유지흡수력 및 수분흡수력
유지흡수력과 수분흡수력은 Adepeju AB 등(2011)의 방법을 참고하여 측정하였다. 유지흡수력은 대두유 20 mL에 시료 2 g을 첨가한 후, 75 rpm에서 1 hr 동안 교반한 뒤 4,000×g에서 20 min 동안 원심분리하여(Combi 508, Hanil, Inc., Gimpo, Korea) 측정하였다. 상등액을 제거한 후 남은 침전물의 무게를 식 (1)에 대입하여 유지흡수력을 계산하였다. 수분흡수력은 증류수 20 mL에 시료 2 g을 첨가한 후, 75 rpm에서 1 hr 동안 교반하고 4,000×g로 20 min 동안 원심분리하여(Combi 508, Hanil, Inc., Gimpo, Korea) 측정하였다. 분리된 상등액을 제거한 뒤 남은 침전물의 무게를 측정하였으며, 해당 값을 식 (2)에 대입하여 수분흡수력을 계산하였다.
| (1) |
| (2) |
6. 기포형성력 및 기포안정성
분리대두단백의 기포형성력 및 기포안정성은 Jeong MS 등(2021)의 방법을 참고하여 측정하였다. 시료는 증류수를 첨가하여 2% 혼합액으로 제조하였으며, 제조된 혼합액 중 40 mL를 취하여 12,000 rpm에서 2 min 균질화하였다(HG-15A, DAIHAN Scientific Co., Ltd, Wonju, Korea). 기포형성력은 균질화 전 시료의 부피와 균질 직후의 기포 부피를 측정하여 식 (3)에 따라 산출하였다. 기포안정성은 기포 형성 직후부터 2 min 정치한 뒤 형성된 기포 부피와 상온에서 60 min 방치한 후 유지된 기포 부피를 측정하여 식 (4)에 따라 계산하였다.
| (3) |
| (4) |
7. 유화형성력 및 유화안정성
유화형성력 및 유화안정성은 Hu A & Li L(2022)의 방법을 참고하여 측정하였다. 각 시료 1 g에 증류수 100 mL를 가하여 300 rpm에서 3 min 교반하여 혼합액을 제조하였다. 이후 혼합액 30 mL와 대두유 10 mL를 혼합하여 10,000 rpm에서 2 min 균질화한 뒤(HG-15A, DAIHAN Scientific Co., Ltd, Wonju, Korea), 즉시 50 mL 비이커에 옮겨 담아 준비하였다. 유화형성력 측정을 위해, 균질화 직후 비이커 바닥 부근에서 시료 25 μL를 채취하여 SDS 용액(0.04%, w/v) 5 mL와 혼합한 뒤 10 sec 동안 교반하고 분광광도계(Cary 3500, Agilent Technologies, Inc., Santa Clara, CA, USA)를 이용하여 500 nm에서 흡광도를 측정하였다. 유화안정성은 비이커에 담은 혼합액을 상온에서 10 min 방치한 후 동일한 방법으로 시료 25 μL를 채취하여 측정하였다. 유화형성력과 유화안정성은 각각 식 (5), 식 (6)에 따라 계산하였으며, 각 식에서 N은 희석 인자(200), c는 시료 농도(0.01 g/mL), Θ는 대두유의 비율(0.25), A0와 A10은 각각 유화 직후 및 10분 후의 흡광도를 의미한다.
| (5) |
| (6) |
8. 최소 겔 형성 농도
분리대두단백의 최소 겔 형성 농도는 O’Kane FE 등(2004)의 방법을 참고하여 분석하였다. 각 시료를 75 mM potassium phosphate 완충용액(pH 7.6)과 혼합하여 3∼30% 농도의 혼합액으로 제조하였으며, 각 혼합액 3 mL를 유리 바이알에 취하여 90℃의 항온수조(SSB-18, Daihan Scientific, Wonju, Korea)에서 30 min 동안 가열하였다. 가열 직후 시료는 얼음을 채운 수조에서 10 min 방냉한 후, 4℃로 설정된 항온기(DS-16S, Dasol Scientific, Hwaseong, Korea)에서 2 hr 정치하였다. 최소 겔 형성 농도는 바이알을 거꾸로 뒤집었을 때, 시료가 흐르지 않고 형태를 유지하는 가장 낮은 농도로 판단하였다.
9. SDS-PAGE
분리대두단백의 단백질 조성을 확인하기 위해 Liu C 등(2019)의 방법을 일부 변형하여 SDS-PAGE(sodium dodecyl sulfate-polyacrylamide gel electrophoresis)를 실시하였다. 분리대두단백 0.08 g에 0.03 M Tris-HCl 용액 2 mL와 1 M 2-mercaptoethanol(2-ME) 20 μL를 혼합한 후, 11,000×g에서 20 min 동안 원심분리하여 상등액을 분리하였다. 상등액 20 μL에 SDS sample buffer 5 μL를 혼합한 후 90℃에서 3 min 동안 가열하고, gradient SDS-PAGE gel (5∼13%, Bio-Rad Laboratories, Inc., Seoul, Korea)에 10 μL씩 주입하여 전기영동(Hoefer, Inc., CA, USA)을 수행하였다. 겔 염색은 Instant Blue 염색액(Expedeon Ltd., Cambridgeshire, UK)을 사용하였으며, 분자량 6, 17, 28, 35, 43, 56, 70, 95, 130, 170 kDa로 구성된 marker 단백질(Thermo Scientific, Inc., Waltham, MA, USA)을 사용하였다.
10. 시차주사열량(DSC)
분리대두단백의 열적 특성을 확인하기 위해 시차주사열량은 Differential scanning calorimeter(DSC 4000, PerkinElmer, Inc., Waltham, MA, USA)를 이용하여 분석하였다. Stainless pan에 시료와 수분의 중량 비율이 1:2가 되도록 넣고, 밀봉하여 상온에서 수분 평형을 이루도록 2 hr 이상 안정화한 후 측정하였다. 측정 조건은 10℃에서 1 min 정치 후 160℃까지 5℃/min 속도로 가열하면서 반응곡선을 얻어내었다.
11. 통계분석
모든 실험은 3회 이상 반복하여 실시하였다. 실험 결과는 SPSS Statistics(Version 25.0, IBM Corp., Armonk, NY, USA)를 이용하여 평균과 표준편차로 나타내었다. 분리대두단백 시료 간 유의성을 검증하기 위해 분산분석을 실시하였고, 시료별 평균값에 대한 유의성을 Duncan’s multiple range test(p<0.05)를 실시하여 분석하였다.
결과 및 고찰
1. pH 및 일반성분
시판 분리대두단백의 pH 및 일반성분 분석 결과는 Table 1과 같다. 대부분의 시료는 중성 pH 값을 나타내어 식품 가공 시 적용이 용이하고 단백질의 기능성 유지에 유리한 조건으로 판단된다. 다만, CH3 시료는 pH 8.17로 비교적 높은 값을 보였으며, SI1과 SI2는 각각 6.44, 6.41로 다소 낮은 값을 나타내었다(p<0.05). 이는 단백질 추출 pH 및 중화 조건의 차이에 기인한 것으로 사료된다.
일반성분 중 수분함량은 2.42∼5.69%의 범위를 보였으며, CH1의 수분함량은 2.42%로 가장 낮았고 SI1의 수분함량은 5.69%로 가장 높은 값을 보였다(p<0.05). 분말형 제품의 저장 안정성은 수분함량의 영향을 받는 것으로 알려져 있으므로(Abdullah Z 등 2020), 최종 분리대두단백의 수분함량을 고려할 필요가 있을 것으로 판단된다. 탄수화물 함량은 5.67∼8.05%의 범위를 나타내었으며, US2가 가장 높은 값을 보였다(p<0.05). 조지방 함량은 US1이 0.64%로 가장 높았으며(p<0.05), CH1, CH2, 그리고 CH3에서는 조지방이 검출되지 않았다. 이는 탈지 공정의 차이로 인한 결과로, CH1, CH2, 그리고 CH3은 지방 대부분이 제거된 것으로 판단된다. 조회분 함량은 3.32∼4.94% 범위로 SI1 가장 낮은 값을, CH3이 가장 높은 값을 보였다(p<0.05). 조단백질 함량은 CH1이 86.90%로 가장 높았고, CH3는 82.87%로 가장 낮은 수치를 나타내었다(p<0.05). Zhang L 등(2024)의 연구에서도 중국 및 유럽에서 구입한 분리대두단백의 조단백질 함량이 81.97∼86.63%의 범위를 보여 본 연구와 유사한 결과를 보였다. 이러한 결과는 분리대두단백이라는 제품 명칭에도 불구하고, 실제 조성 측면에서 국제적으로 정의된 분리대두단백 기준(90% 이상)에 부합하지 않는 제품이 시중에 유통되고 있음을 시사하며(Codex Alimentarius 2019), 제품 라벨링의 명확성 확보와 표준화 필요성이 있다고 생각되었다. 한편, CH1은 조단백질 함량이 가장 높고 조지방이 검출되지 않아 원료 정제 수준이 높은 것으로 판단되며, 이러한 특성으로 보아 분리대두단백 원료로서의 활용 적합성이 높은 것으로 판단된다.
2. 구성 아미노산
시판 분리대두단백의 구성 아미노산 분석 결과는 Table 2와 같다. 총 아미노산 함량은 CH1이 84.13%로 가장 높은 값을 나타내었다(p<0.05). 모든 시료에서 glutamic acid와 aspartic acid가 주요 아미노산으로 확인되었으며, 다른 아미노산에 비해 높은 함량을 나타내었다. 이는 대두단백의 특성상 주요 아미노산으로 알려진 구성과 일치하는 결과로 Kim KS 등(2003)과 Moon HK 등(2011)의 선행연구와 유사하였다. 필수 아미노산 중 lysine은 높은 함량을 보였으나 cysteine, tryptophan 및 methionine은 상대적으로 낮은 수치를 보여 Cha SH 등(2020)이 보고한 농축대두단백의 아미노산 조성과 일치하는 결과를 보였다. 특히 methionine은 대두단백질에서 일반적으로 결핍되는 제한 아미노산으로, 그 함량은 식품 단백질의 영양적 품질을 평가하는 주요 지표로 활용된다(Moon JY 등 2015). 한편, cysteine은 가열 및 압출 공정 중 이황화 결합(S-S)을 형성하여 단백질 간 결합력과 구조적 안정성을 높이는 데 기여하며, 이는 식물성조직단백(textured vegetable protein; TVP)과 같은 조직형 단백 제품의 섬유상 조직 형성 및 텍스처 개선에 중요한 역할을 할 수 있다(Gao Y 등 2024). 따라서 황 함유 아미노산의 함량은 영양학적 가치뿐 아니라 가공적성 측면에서도 중요한 요소라 할 수 있다. 시판 분리대두단백 중 CH1이 필수 아미노산 함량이 가장 높은 것으로 나타났다(p<0.05). 아미노산 조성은 식품이 인체의 필수 아미노산 요구량을 얼마나 충족시킬 수 있는지를 평가하는 중요한 기준으로, Huang S 등(2018)은 이러한 분석이 식품의 단백질 품질을 판단하는 데 유용하다고 보고하였다. 본 연구에서 시판 분리대두단백은 제품에 따라 아미노산 조성의 차이를 보였으며, 활용 시 이러한 조성을 고려한 선택이 필요함을 시사한다. 이러한 결과는 시판 분리대두단백 간의 영양적 품질 차이를 반영하며, 제품 선택 및 향후 국산 분리대두단백 개발 시 영양적 균형을 고려한 품질 기준 마련의 필요성을 뒷받침하는 근거로 활용될 수 있을 것으로 기대된다.
3. 외관 및 색도
시판 분리대두단백의 외관은 Fig. 1에 제시하였으며, 색도 측정 결과는 Table 3과 같다. 명도(L)는 84.60∼88.72 범위로 나타났으며, US2가 가장 높은 값을 보여 상대적으로 밝은 색을 띠는 것으로 확인되었다. 적색도(a) 및 황색도(b)는 SI1과 SI2에서 가장 높은 값을 나타냈고, US2는 각각 0.49 및 14.09로 가장 낮은 수치를 보였다. 색차(ΔE)도 원산지에 따라 차이를 보였으며, 싱가포르산, 중국산, 미국산 순으로 높은 값을 나타내었다. 육안으로 시료 간 차이는 뚜렷하지 않았으나, 전반적으로 US1과 US2는 명도가 높고 색차가 작아 백색에 가까운 색상을 나타내었다. SI1과 SI2는 명도가 낮고 적색도와 황색도 값이 높아 가공 시 최종 제품의 색상에 영향을 줄 가능성이 있는 것으로 판단된다.

Appearance of commercial soy protein isolate (SPI).1) US1, US2: soy protein isolate from the United States; SI1, SI2: soy protein isolate from Singapore; CH1, CH2, and CH3: soy protein isolate from China.
4. 유지흡수력 및 수분흡수력
시판 분리대두단백의 유지흡수력 및 수분흡수력 측정 결과는 Fig. 2와 같다. 유지흡수력은 단백질의 소수성 아미노산 비율 및 표면 특성에 의해 영향을 받으며, 이는 유화력 및 식감 안정성 등 지질 관련 품질 특성과 밀접하게 관련된다(Jeong MS & Cho SJ 2023). 본 연구에서 유지흡수력은 2.22∼2.82 g/g 범위로 확인되었으며, US2가 가장 낮은 값을 나타내었고 CH2가 가장 높은 값을 보였다(p<0.05). 수분흡수력은 단백질 분자의 구조, 친수성 아미노산의 함량 및 분포, 입자 표면의 물리적 특성 등에 의해 결정되며, 이는 식품 가공 시 겔 형성에 영향을 미쳐 최종 제품의 조직감, 점도 등과 관련되는 중요한 특성이다(Cho SY & Ryu GH 2020). 본 연구에서 수분흡수력은 유지흡수력 비해 시료 간 유의적인 차이를 나타내었다. 분리대두단백의 수분흡수력은 2.58∼7.41 g/g 범위로 나타났으며, US1이 가장 높은 값을 보여 수분 결합력이 우수한 구조적 특성을 지닌 것으로 생각되었다(p<0.05). Zhang L 등(2024)은 시중에서 구입한 분리대두단백의 수분결합력이 3.55∼8.75 g/g의 범위의 값을 보였다고 하였는데 본 연구에서도 이와 유사한 결과를 나타내었다. 일반적으로 유지흡수력과 수분흡수력은 단백질의 구조적 특성에 따라 반비례하는 경향을 보일 수 있으나(Ding M 등 2022) 본 연구에서는 그와 같은 명확한 상관관계는 관찰되지 않았다. 이는 각 제품의 제조 공정, 단백질 구조 변화, 탈지 및 건조 조건 등의 차이에 기인할 수 있으며(Denavi G 등 2009), 이러한 분리대두단백의 기능적 특성은 제품별로 다르게 나타날 수 있음을 보여준다. 분리대두단백의 수분 및 유지흡수력은 대체육 제품에서 육즙 보유력과 결착력, 베이커리 제품에서 반죽의 안정성과 기공 형성 정도 등에 영향을 줄 수 있기 때문에 결과적으로 최종 제품의 식감 및 풍미 형성에 중요한 요인으로 작용할 수 있다(Loveday SM 2019; Zhang T 등 2021). 따라서 대체육이나 베이커리 등에 적용 시 각 제품의 특성에 적합한 원료 선별이 중요하다.
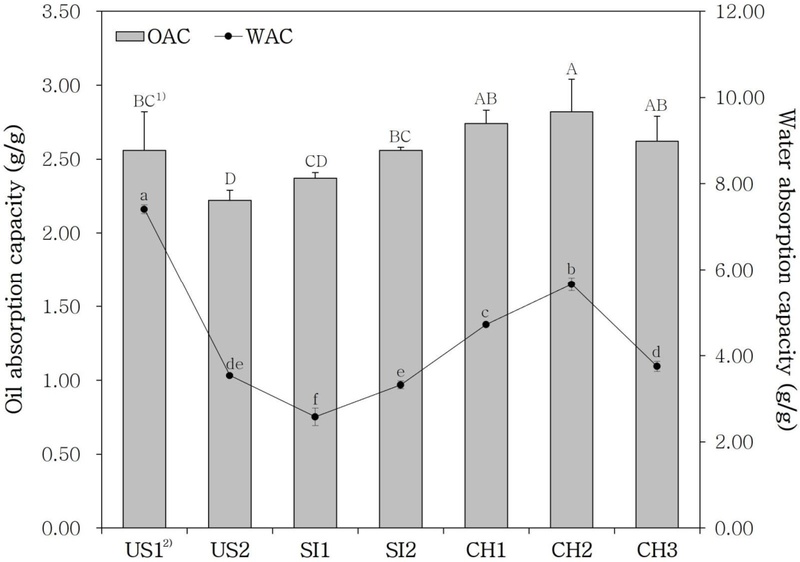
Oil absorption capacity (OAC) and water absorption capacity (WAC) of commercial soy protein isolate (SPI).1) Different capital letters (OAC) and lowercase letters (WAC) indicate significant differences (p<0.05) by Duncan’s multiple range test.2) US1, US2: soy protein isolate from the United States; SI1, SI2: soy protein isolate from Singapore; CH1, CH2, and CH3: soy protein isolate from China.
5. 기포 형성력 및 기포 안정성
시판 분리대두단백의 기포형성력 및 기포안정성 측정 결과는 Fig. 3과 같다. 기포형성력 및 안정성은 베이킹, 디저트, 소스류 등의 식품에서 부드러운 텍스처, 부피 증가, 구조적 일관성 확보에 중요한 영향을 미칠 수 있어, 제품 적용 시 고려되어야 할 주요한 특성이다(Martínez KD 등 2009). 기포형성력은 단백질의 표면활성 및 피막 형성 특성과 밀접하게 관련되어 있으며, 안정한 기포를 형성하기 위해서는 공기 입자를 감싸는 단백질 피막이 충분한 강도를 가져야 하고, 수분 보유력과 기계적 자극에 대한 저항성도 필요하다(Wang MP 등 2019; Li J 등 2022). 시판 분리대두단백 중에서 CH1과 CH2이 유의적으로 우수한 기포형성력을 나타내었다(p<0.05). 기포안정성은 US1과 US2가 다른 제품에 비해 우수한 결과를 보였다(p<0.05). 이러한 결과는 분리대두단백의 원료 특성이나 제조 공정의 차이에서 기인할 수 있으며, 단백질의 구조적 특성, 변성 정도 등의 영향이 복합적으로 작용했을 가능성이 있다(Damodaran S 2005). 따라서 제품 적용 시 최종 제품의 물성에 적합한 기포 특성을 고려하여 분리대두단백을 선택하는 것이 바람직하다. 기포형성력이 우수한 분리대두단백은 혼합 및 교반 과정에서 송기를 효과적으로 포획하여 부피를 팽창시키므로 크림 음료, 무스와 머랭과 같은 디저트에 적합하다고 알려져 있다. 반면, 기포안정성이 우수한 분리대두단백은 형성된 피고가 장시간 붕괴지 않도록 유지하여 점도와 질감을 안정적으로 유지할 수 있으므로 휘핑크림이나 마요네즈와 같은 소스류에 적합한 것으로 보고된 바 있다(Sikora M 등 2008; Cano-Medina A 등 2011; Aghajanzadeh S 등 2024).
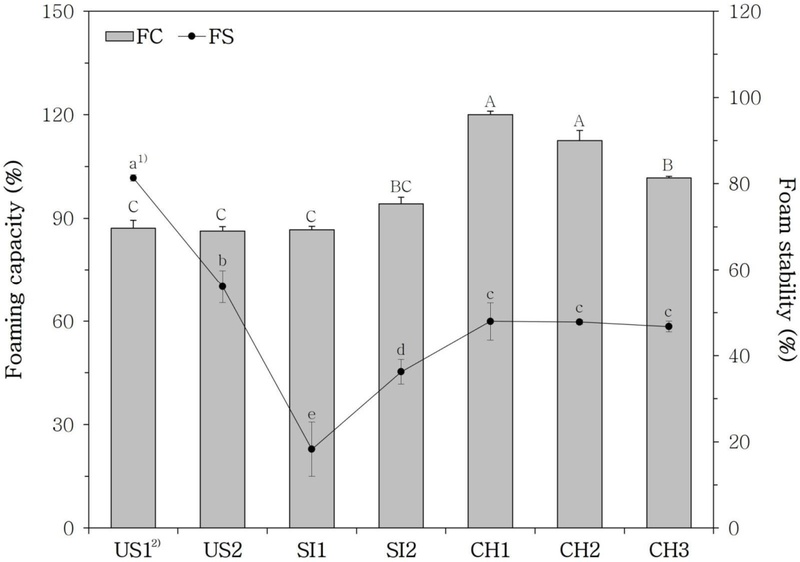
Foaming capacity (FC) and foam stability (FS) of commercial soy protein isolate (SPI).1) Different capital letters (FC) and lowercase letters (FS) indicate significant differences (p<0.05) by Duncan’s multiple range test.2) US1, US2: soy protein isolate from the United States; SI1, SI2: soy protein isolate from Singapore; CH1, CH2, and CH3: soy protein isolate from China.
6. 유화 형성력 및 유화 안정성
시판 분리대두단백의 유화형성력 및 유화안정성 측정 결과는 Fig. 4에 제시하였다. 유화형성력은 서로 섞이지 않는 물과 기름을 균일하게 분산시켜 에멀전을 형성하는 능력을 의미하고, 유화안정성은 형성된 에멀전이 시간 경과 후에도 분리되지 않고 지속적으로 유지되는 능력을 의미하는데 두 특성 모두 분리대두단백의 유화 특성을 평가하는 데 중요한 기준이 될 수 있다(Mozafarpour R 등 2019; Ma KK 등 2022). 본 연구에서 US1과 CH1, CH2, 그리고 CH3은 유의적으로 높은 유화형성력을 보였다(p<0.05). 유화안정성의 경우, CH2가 유의적으로 가장 높은 값을 보였으며, US1은 가장 낮은 값을 나타내었다(p<0.05). 유화안정성은 제품 내 함유된 지방이 소수성 아미노산의 표면 노출을 유도하여 단백질-지질 상호작용에 영향을 줄 수 있다(Tang CH 2017). 일반적으로 유지흡수력이 높을수록 유화형성력 및 안정성이 증가하는 것으로 알려져 있으며(Adiamo OQ 등 2016), 본 연구에서도 유지흡수력이 가장 높았던 CH2가 유화형성력 및 안정성이 우수한 결과를 보였다. 따라서 CH2는 드레싱, 소시지, 아이스크림 등 유화 특성이 요구되는 제품군에 적용하기에 적합한 분리대두단백으로 판단된다.
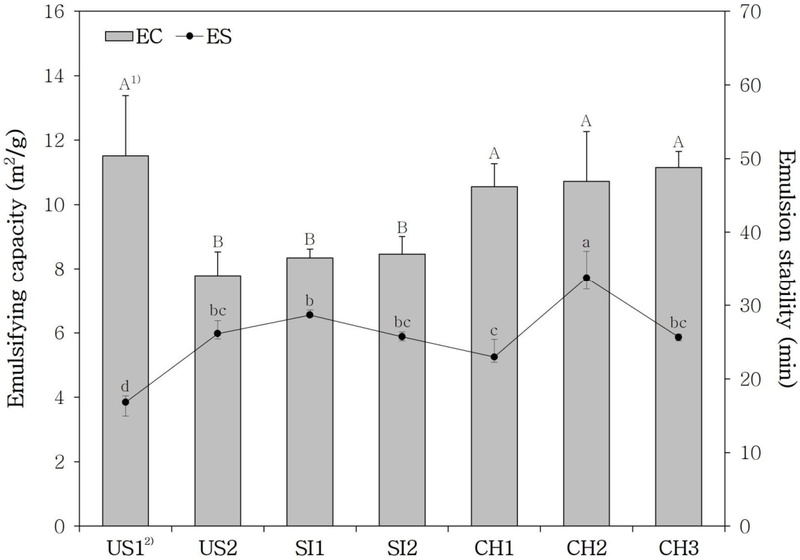
Emulsifying capacity (EC) and emulsion stability (ES) of commercial soy protein isolate (SPI).1) Different capital letters (EC) and lowercase letters (ES) indicate significant differences (p<0.05) by Duncan’s multiple range test.2) US1, US2: soy protein isolate from the United States; SI1, SI2: soy protein isolate from Singapore; CH1, CH2, and CH3: soy protein isolate from China.
7. 최소 겔 형성 농도
시판 분리대두단백의 최소 겔 형성 농도 측정 결과는 Fig. 5와 같다. 최소 겔 형성 농도는 단백질이 겔을 형성하는 데 필요한 최소 농도를 의미하며, 이는 단백질 기반 소재를 활용한 가공 공정의 최적화뿐만 아니라 생산 효율성 및 최종 제품의 텍스처 조절에 있어 중요한 특성으로 작용한다(Webb D 등 2023). 본 연구 결과, SI1과 US2는 다른 시료에 비해 상대적으로 높은 겔 형성 농도를 보였으며, US1은 가장 낮은 값을 나타내었다(p<0.05). 일반적으로 최소 겔 형성 농도가 낮은 분리대두단백은 유화제, 응고제, 저지방 식품 등과 같이 비교적 낮은 농도의 단백질을 사용하는 제품에 적합하며, 반대로 최소 겔 형성 농도가 높은 분리대두단백은 단백질 바, 대체육 등 고농도 단백질이 요구되는 제품에 활용하기에 적합한 것으로 알려져 있다(Zhao H 등 2020; Ma KK 등 2022).
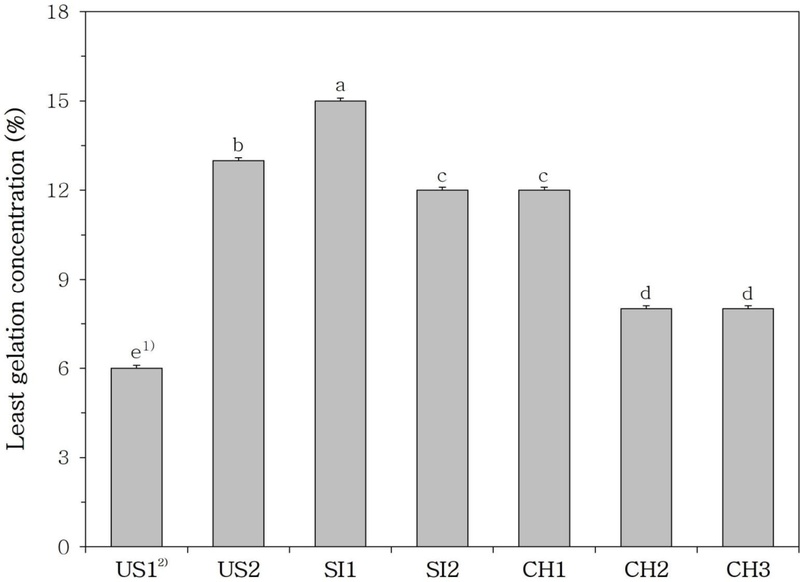
Least gelation concentration of commercial soy protein isolate (SPI).1) Different letters indicate significant differences (p<0.05) by Duncan’s multiple range test.2) US1, US2: soy protein isolate from the United States; SI1, SI2: soy protein isolate from Singapore; CH1, CH2, and CH3: soy protein isolate from China.
8. SDS-PAGE
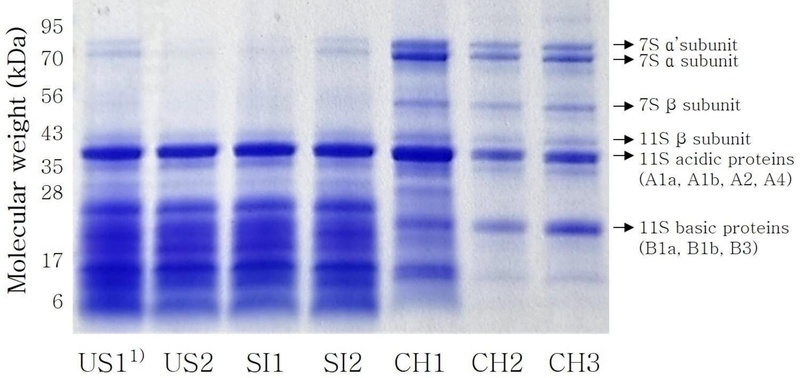
시판 분리대두단백의 SDS-PAGE 전기영동 결과는 Fig. 6에 제시하였다. 대두의 저장단백질은 주로 글로불린 계열로 7S(β-conglycinin)와 11S(glycinin) 글로불린이 약 80%를 차지하며 두 단백질의 복합체 형태로 존재한다(Kim YM 등 2011). 이러한 저장단백질의 조성은 가공 용도 결정에 중요한 요소로 작용한다. 7S 글로불린은 α(67 kDa), α′(71 kDa), β(50 kDa)의 세 가지 서브유닛으로 구성되며, 11S는 약 35 kDa 및 20 kDa의 분자량을 갖는 서브유닛으로 구성된다(Nishinari K 등 2014). CH1, CH2, 그리고 CH3은 7S 및 11S 서브유닛에 해당하는 밴드들이 선명하게 관찰되었다. US1과 US2, SI1과 SI2는 7S에 해당하는 밴드가 매우 희미하게 나타났으며, CH1, CH2, 그리고 CH3과 달리 28 kDa 이하 분자량 영역에서 다수의 미세한 밴드가 관찰되었다. 그럼에도 불구하고, 시판 분리대두단백의 전체적인 저장단백질 구성은 모든 시료에서 유사한 패턴을 보였다. 다만, 7S 및 11S 단백질은 분리대두단백의 가공 적성 및 최종 제품 품질에 영향을 미칠 수 있는 주요 인자로 보고되므로(Liu Y 등 2023), 향후 각 서브유닛의 구성 비율에 대한 정량적 분석이 필요할 것으로 판단된다.
9. 시차주사열량(DSC)
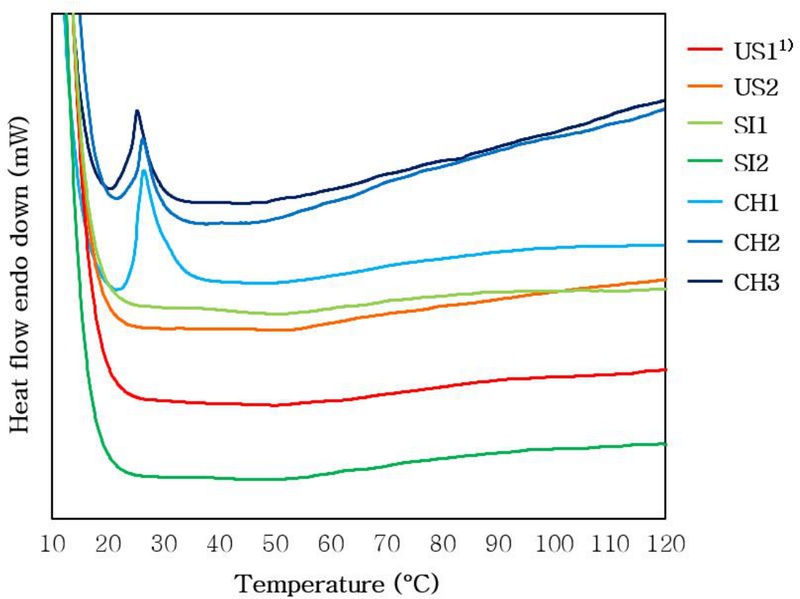
시차주사열량법(DSC)은 단백질의 열변성을 평가하는 데 사용되며 일반적으로 변성 시작 온도(To), 피크 온도(Tp), 엔탈피 변화(ΔH)를 통해 열전이 특성을 분석한다. 그러나 열곡선에서 뚜렷한 피크가 관찰되지 않는 경우, 시료가 이미 과변성되어 열에 의한 단백질 구조 변화가 유도되지 않은 것을 의미한다(Li S 등 2014). 시판 분리대두단백의 DSC 측정 결과는 Fig. 7에 제시하였다. 대두단백의 주요 열전이 반응이 대부분 120℃ 이하에서 나타나는 점을 고려하여, 본 연구에서는 DSC 결과를 120℃까지 그래프로 제시하였다(Hua Y 등 2005; Ahmed J 등 2006). DSC 분석 결과, US1과 US2, SI1과 SI2는 분석 구간 전반에 걸쳐 열전이 반응 없이 플랫한 열곡선을 나타내었다. 반면, CH1, CH2, 그리고 CH3은 공통적으로 25∼30℃ 구간에서 발열 피크를 나타내었다. 일반적으로 대두 단백질의 열변성 반응에서 70∼80℃ 구간의 흡열 피크는 7S(β-conglycinin), 90∼100℃ 구간의 피크는 11S(glycinin) 단백질의 열변성에 해당하는 것으로 알려져 있다(Ryan M 등 2008). 25∼30℃ 구간은 일반적인 단백질 열변성 범위와는 상이한 온도 구간으로 이러한 저온 발열반응은 단백질의 열변성보다 시료 내 흡습된 수분의 초기 탈리 또는 수분과 결합된 단백질 구조의 부분적인 재배열 등으로 인해 발생하였을 가능성이 높다(Rawel HM 등 2002). 따라서 본 연구에서 25∼30℃ 구간에서 관찰된 발열 피크는 수분과 단백질의 상호작용에 의해 유도된 비정형적 열반응으로 사료된다. 이러한 발열 특성은 제조 공정 및 조성 차이에 기인할 가능성이 있다. 특히 원료의 품종, 탈지 방식, 열처리 등 제조 과정의 차이가 단백질 구조에 영향을 줄 수 있다. 따라서 CH1, CH2, 그리고 CH3은 다른 원산지 제품과는 상이한 제조 공정에 따라 제조된 것으로 사료된다. 또한 시판 분리대두단백은 제조 공정 과정에서 상당한 수준의 단백질 변성이 이루어져 7S 및 11S 단백질의 열변성에 해당하는 명확한 열전이 피크가 관찰되지 않은 것으로 판단된다.
요 약
본 연구는 시판 중인 분리대두단백 7종의 이화학적 및 기능적 특성을 비교 분석하였다. 분석 결과, 모든 시료의 조단백질 함량은 82.87∼86.90%의 범위로 분리단백 기준(90%)에 미치지 못하는 수준으로 나타났다. CH1, CH2, 그리고 CH3은 조지방이 검출되지 않았으나 조회분 함량이 높았다. CH1이 대부분의 구성 아미노산 함량에서 높은 값을 보였다. 색차 측정 결과, US1과 US2의 명도가 가장 높아 백색에 가까웠으나, 육안으로는 시료 간 차이가 뚜렷하지 않았다. 기능적 특성에서는 US1이 가장 높은 수분흡수력을 보였고, 유지흡수력은 CH2가 가장 높은 값을 나타내었다. 기포형성력은 CH1, CH2, 그리고 CH3가 높았으며, 기포 안정성은 US1과 US2가 유의적으로 높았다. 유화형성력은 US1, CH1, CH2, 그리고 CH3가 높은 값을 보였고, 유화안정성은 CH2가 가장 높은 값을 나타내었다. 최소 겔 형성 농도는 SI1이 유의적으로 가장 높은 값을 나타내었다. SDS-PAGE 분석에서는 CH1, CH2, 그리고 CH3가 뚜렷한 7S 단백질 밴드를 나타낸 반면, US1과 US2, SI1과 SI2는 일부 밴드가 미약하였다. DSC 분석 결과, US1과 US2, SI1과 SI2는 분석 구간 전반에 걸쳐 열전이 반응 없이 플랫한 열곡선을 나타내었으나 CH1, CH2, 그리고 CH3은 25∼30℃ 구간에서 발열 피크를 나타내었다. 본 연구는 원료 품종, 추출·정제·건조 등 세부적인 제조 공정 요소를 규명하지 못한 한계가 있으나, 시판 분리대두단백의 기능적 특성 간 유의한 차이가 확인하였다. 이러한 기능적 특성 차이에 따라 선별적 접근과 맞춤형 식품 적용이 요구됨을 보여준다. 특히 국내에서 소비되는 분리대두단백이 전량 수입에 의존하고 있는 현실은 식품산업의 안정성과 지속 가능성 측면에서 잠재적인 제약이 있다. 이에 따라 국산 대두를 활용한 분리대두단백의 개발은 식품 소재의 자급률 향상뿐만 아니라, 다양한 응용 제품에 적합한 소재 확보 측면에서도 중요한 과제로 부상하고 있다. 아울러 현재까지는 시판 중인 수입산 분리대두단백의 품질 특성에 대한 체계적인 정보가 부족하여 산업 현장에서 분리대두단백 적용 시 제품 간 비교 및 평가가 어려운 상황이기에 기능적 특성 기반의 품질 평가를 실시할 필요가 있다고 생각하였다. 따라서 시판 제품의 이화학적 및 기능적 특성을 기반으로 식품 가공 현장에서 분리대두단백의 적용 방향을 제시하고, 향후 국산 분리대두단백 개발하는 데 기초자료로 활용될 수 있을 것으로 기대된다.
Acknowledgments
본 연구는 농촌진흥청 국립식량과학원 연구사업(과제번호: PJ017480012024)의 지원에 의해 이루어진 것임. 본 연구는 2024년도 농촌진흥청 국립식량과학원 전문연구원 과정 지원사업에 의해 이루어진 것임.
REFERENCES
-
Abdullah Z, Taip FS, Kamal SMM, Rahman RZA (2020) Nonlinear model-based inferential control of moisture content of spray dried coconut milk. Foods 9(9): 1177.
[https://doi.org/10.3390/foods9091177]

- Adepeju AB, Gbadamosi SO, Adeniran AH, Omobuwajo TO (2011) Functional and pasting characteristics of breadfruit (Artocarpus altilis) flours. Afr J Food Sci 5(9): 529-535.
-
Adiamo OQ, Gbadamosi OS, Abiose SH (2016) Functional properties and protein digestibility of protein concentrates and isolates produced from Kariya (Hildergadia bateri) seed. J Food Process Preserv 40(5): 979-989.
[https://doi.org/10.1111/jfpp.12678]

-
Aghajanzadeh S, Sultana A, Mohammad Ziaiifar A, Khalloufi S (2024) Formation of pores and bubbles and their impacts on the quality attributes of processed foods: A review. Food Res Int 188: 114494.
[https://doi.org/10.1016/j.foodres.2024.114494]

-
Ahmed J, Ramaswamy HS, Alli I (2006) Thermorheological characteristics of soybean protein isolate. J Food Sci 71(3): E158-E163.
[https://doi.org/10.1111/j.1365-2621.2006.tb15629.x]

-
Cano-Medina A, Jiménez-Islas H, Dendooven L, Herrera RP, González-Alatorre G, Escamilla-Silva EM (2011) Emulsifying and foaming capacity and emulsion and foam stability of sesame protein concentrates. Food Res Int 44(3): 684-692.
[https://doi.org/10.1016/j.foodres.2010.12.015]

- Cha SH, Shin KO, Han KS (2020) Studies on the characteristics of concentrated soy protein. Korean J Food Sci Technol 52(5): 459-466.
- Cho SY, Ryu GH (2020) Effects of mushroom composition on the quality characteristics of extruded meat analog. Korean J Food Sci Technol 52(4): 357-362.
- Codex Alimentarius (2019) General Standard for Soy Protein Products (CXS 175-1989). https://www.fao.org, (accessed on 17. 6. 2024).
-
Damodaran S (2005) Protein stabilization of emulsions and foams. J Food Sci 70(3): R54-R66.
[https://doi.org/10.1111/j.1365-2621.2005.tb07150.x]

-
Denavi G, Tapia-Blácido DR, Añón MC, Sobral PJA, Mauri AN, Menegalli FC (2009) Effects of drying conditions on some physical properties of soy protein films. J Food Eng 90(3): 341-349.
[https://doi.org/10.1016/j.jfoodeng.2008.07.001]

-
Ding M, Huang Z, Jin Z, Zhou C, Wu J, Zhao D, Shan K, Ke W, Zhang M, Nian Y, Li C (2022) The effect of fat content in food matrix on the structure, rheological properties and digestive properties of protein. Food Hydrocoll 126: 107464.
[https://doi.org/10.1016/j.foodhyd.2021.107464]

-
Gao Y, Lian W, Zhang H, Zhu Y, Huang Y, Liu L, Zhu X (2024) Mechanism of L-cysteine-induced fibrous structural changes of soybean protein at different high-moisture extrusion zones. Int J Biol Macromol 268(Pt 1): 131621.
[https://doi.org/10.1016/j.ijbiomac.2024.131621]

-
Hu A, Li L (2022) Effects of ultrasound pretreatment on functional property, antioxidant activity, and digestibility of soy protein isolate nanofibrils. Ultrason Sonochem 90: 106193.
[https://doi.org/10.1016/j.ultsonch.2022.106193]

-
Hu Z, Wang Y, Ma Z, Cheng T, Guo Z, Zhou L, Wang Z (2023) Impacts of industrial modification on the structure and gel features of soy protein isolate and its composite gel with myofibrillar protein. Foods 12(10): 1982.
[https://doi.org/10.3390/foods12101982]

-
Hua Y, Cui SW, Wang Q, Mine Y, Poysa V (2005) Heat induced gelling properties of soy protein isolates prepared from different defatted soybean flours. Food Res Int 38(4): 377-385.
[https://doi.org/10.1016/j.foodres.2004.10.006]

-
Huang S, Wang LM, Sivendiran T, Bohrer BM (2018) Amino acid concentration of high protein food products and an overview of the current methods used to determine protein quality. Crit Rev Food Sci Nutr 58(15): 2673-2678.
[https://doi.org/10.1080/10408398.2017.1396202]

-
Hwang NK, Gu BJ, Ryu GH (2023) Physicochemical properties of low-moisture extruded meat analog by replacing isolated soy with mung bean protein. J Korean Soc Food Sci Nutr 52(8): 836-843.
[https://doi.org/10.3746/jkfn.2023.52.8.836]

-
Jeong MS, Cho SJ (2023) Evaluation of quality characteristics of soybean protein isolate from cold-pressed soybean meal. J Korean Soc Food Sci Nutr 52(7): 716-721.
[https://doi.org/10.3746/jkfn.2023.52.7.716]

-
Jeong MS, Lee SD, Cho SJ (2021) Effect of three defatting solvents on the techno-functional properties of an edible insect (Gryllus bimaculatus) protein concentrate. Molecules 26(17): 5307.
[https://doi.org/10.3390/molecules26175307]

-
Kim HW, Choi JH, Choi YS, Han DJ, Kim HY, Lee MA, Shim SY, Kim CJ (2009) Effects of wheat fiber and isolated soy protein on the quality characteristics of frankfurter-type sausages. Food Sci Anim Resour 29(4): 475-481.
[https://doi.org/10.5851/kosfa.2009.29.4.475]

- Kim KS, Kim MJ, Lee KA, Kwon DY (2003) Physico-chemical properties of Korean traditional soybeans. Korean J Food Sci Technol 35(3): 335-341.
-
Kim SH (2023) Development of card news as an educational material for the proper use of plant-based milk alternatives reflecting adult consumption characteristics through focus group interview. Journal of Home Economics Education Research 35(1): 53-72.
[https://doi.org/10.19031/jkheea.2023.3.35.1.53]

- Kim YA (2018) Soy protein: A high-quality, plant-based protein. Food Sci Ind 51(4): 270-277.
-
Kim YJ, Cha JY, Kim JH, Kim TK, Park MK, Lee JH, Choi YS (2023) Future prospects of meat protein alternative food in food tech industry. Food Sci Ind 56(3): 186-197.
[https://doi.org/10.23093/FSI.2023.56.3.186]

-
Kim YM, Lee JY, Yoon UH, Choi SB, Ha SH, Lim SH (2011) New design of rice seed storage proteins. J Plant Biotechnol 38(4): 263-271.
[https://doi.org/10.5010/JPB.2011.38.4.263]

- Korea Customs Service (2023) Import and Export Trade Statistics. https://tradedata.go.kr, (accessed on 17. 6. 2024).
- Lee EJ, Lee JY, Hong GP (2021) Current status and development strategies of domestic plant-based meat alternative food market. Food Sci Anim Resour Ind 10(1): 61-70.
- Lee SY, Kim JH, Hur SJ (2023) Current status and technologies of alternative foods in Korea and abroad. Food Sci Anim Resour Ind 12(1): 59-72.
-
Li J, Yang X, Swallah MS, Fu H, Ji L, Meng X, Yu H, Lyu B (2022) Soy protein isolate: An overview on foaming properties and air-liquid interface. Int J Food Sci Technol 57: 188-200.
[https://doi.org/10.1111/ijfs.15390]

-
Li S, Wei Y, Fang Y, Zhang W, Zhang B (2014) DSC study on the thermal properties of soybean protein isolates/corn starch mixture. J Therm Anal Calorim 115: 1633-1638.
[https://doi.org/10.1007/s10973-013-3433-4]

-
Liu C, Damodaran S, Heinonen M (2019) Effects of microbial transglutaminase treatment on physiochemical properties and emulsifying functionality of faba bean protein isolate. LWT 99: 396-403.
[https://doi.org/10.1016/j.lwt.2018.10.003]

-
Liu Y, Huang ZH, Hu ZX, Yu Z, An HZ (2023) Texture and rehydration properties of texturised soy protein: Analysis based on soybean 7S and 11S proteins. Int J Food Sci Technol 58(1): 323-333.
[https://doi.org/10.1111/ijfs.15787]

-
Loveday SM (2019) Food proteins: Technological, nutritional, and sustainability attributes of traditional and emerging proteins. Annu Rev Food Sci Technol 10: 311-339.
[https://doi.org/10.1146/annurev-food-032818-121128]

-
Ma KK, Grossmann L, Nolden AA, McClements DJ, Kinchla AJ (2022) Functional and physical properties of commercial pulse proteins compared to soy derived protein. Future Foods 6: 100155.
[https://doi.org/10.1016/j.fufo.2022.100155]

-
Martínez KD, Sánchez CC, Rodríguez Patino JM, Pilosof AMR (2009) Interfacial and foaming properties of soy protein and their hydrolysates. Food Hydrocoll 23(8): 2149-2157.
[https://doi.org/10.1016/j.foodhyd.2009.03.015]

-
Meganaharshini M, Sudhakar V, Bharathi ND, Deepak S (2023) Review on recent trends in the application of protein concentrates and isolates-A food industry perspective. Food Humanity 1: 308-325.
[https://doi.org/10.1016/j.foohum.2023.05.022]

- MFDS (2024) Analytical Method of General Composition. Korea Food Code Notification No. 2024-71. https://various.foodsafetykorea.go.kr, (accessed on 14. 11. 2024).
-
Monteiro SR, Lopes-da-Silva JA (2019) Critical evaluation of the functionality of soy protein isolates obtained from different raw materials. Eur Food Res Technol 245: 199-212.
[https://doi.org/10.1007/s00217-018-3153-x]

- Moon HK, Lee SW, Moon JN, Kim DH, Yoon WJ, Kim GY (2011) Quality characteristics of various beans in distribution. J East Asian Soc Diet Life 21(2): 215-221.
-
Moon JY, Kwon SW, Hong SB, Seok SJ, Kim JS, Kim SJ (2015) Characteristics and functional analysis of Bacillus strains from the fermented soybean products, Cheonggukjang. Korean J Microbiol 51(3): 300-307.
[https://doi.org/10.7845/kjm.2015.5044]

-
Mozafarpour R, Koocheki A, Milani E, Varidi M (2019) Extruded soy protein as a novel emulsifier: Structure, interfacial activity and emulsifying property. Food Hydrocoll 93: 361-373.
[https://doi.org/10.1016/j.foodhyd.2019.02.036]

-
Nishinari K, Fang Y, Guo S, Phillips GO (2014) Soy proteins: A review on composition, aggregation and emulsification. Food Hydrocoll 39: 301-318.
[https://doi.org/10.1016/j.foodhyd.2014.01.013]

-
O’Kane FE, Happe RP, Vereijken JM, Gruppen H, van Boekel MAJS (2004) Characterization of pea vicilin. 2. Consequences of compositional heterogeneity on heat-induced gelation behavior. J Agric Food Chem 52(10): 3, 149-3, 154.
[https://doi.org/10.1021/jf035105a]

-
Park CS, Seo MS, Jung SY (2023) Effects of aronia powder on the quality characteristics of texturized vegetable protein using defatted soy flour. Korean J Food Sci Technol 55(3): 252-257.
[https://doi.org/10.9721/KJFST.2023.55.3.252]

-
Park HJ, Oh HI, Yang JY, Oh JE, Kang NE, Cho MS (2020) A study on the consumer’s preference and purchasing behavior of high-protein bars with soy protein isolate. J Korean Soc Food Sci Nutr 49(3): 270-278.
[https://doi.org/10.3746/jkfn.2020.49.3.270]

-
Pay C, Gianoli A (2024) Securing the future: Analysing the protein transition in Singapore. Cities 150: 105072.
[https://doi.org/10.1016/j.cities.2024.105072]

-
Rawel HM, Czajka D, Rohn S, Kroll J (2002) Interactions of different phenolic acids and flavonoids with soy proteins. Int J Biol Macromol 30(3-4): 137-150.
[https://doi.org/10.1016/S0141-8130(02)00016-8]

-
Ryan M, McEvoy E, Duignan S, Crowley C, Fenelon M, O’Callaghan DM, FitzGerald RJ (2008) Thermal stability of soy protein isolate and hydrolysate ingredients. Food Chem 108(2): 503-510.
[https://doi.org/10.1016/j.foodchem.2007.11.001]

-
Sikora M, Badrie N, Deisingh AK, Kowalski S (2008) Sauces and dressings: A review of properties and applications. Crit Rev Food Sci Nutr 48(1): 50-77.
[https://doi.org/10.1080/10408390601079934]

-
Tang CH (2017) Emulsifying properties of soy proteins: A critical review with emphasis on the role of conformational flexibility. Crit Rev Food Sci Nutr 57(12): 2636-2679.
[https://doi.org/10.1080/10408398.2015.1067594]

-
Wang MP, Chen XW, Guo J, Yang J, Wang JM, Yang XQ (2019) Stabilization of foam and emulsion by subcritical water-treated soy protein: Effect of aggregation state. Food Hydrocoll 87: 619-628.
[https://doi.org/10.1016/j.foodhyd.2018.08.047]

-
Webb D, Dogan H, Li Y, Alavi S (2023) Physico-chemical properties and texturization of pea, wheat and soy proteins using extrusion and their application in plant-based meat. Foods 12(8): 1586.
[https://doi.org/10.3390/foods12081586]

-
Zhang L, Li Q, Zhang W, Bakalis S, Luo Y, Lametsch R (2024) Different source of commercial soy protein isolates: structural compositional, and physicochemical characteristics in relation to protein functionalitis. Food Chem 433: 137315.
[https://doi.org/10.1016/j.foodchem.2023.137315]

-
Zhang T, Dou W, Zhang X, Zhao Y, Zhang Y, Jiang L, Sui X (2021) The development history and recent updates on soy protein-based meat alternatives. Trends Food Sci Technol 109: 702-710.
[https://doi.org/10.1016/j.tifs.2021.01.060]

-
Zhao H, Shen C, Wu Z, Zhang Z, Xu C (2020) Comparison of wheat, soybean, rice, and pea protein properties for effective applications in food products. J Food Biochem 44(4): e13157.
[https://doi.org/10.1111/jfbc.13157]

-
Zheng L, Regenstein JM, Zhou L, Wang Z (2022) Soy protein isolates: A review of their composition, aggregation, and gelation. Compr Rev Food Sci Food Saf 21(2): 1940-1957.
[https://doi.org/10.1111/1541-4337.12925]