
Tyrosinase 하향조절을 통한 대두(Glycine max (L.) Merr) 추출물의 멜라닌 생성 억제 효과
Abstract
To investigate the molecular mechanisms underlying the antimelanogenic effects of Glycine max (L.) Merr ethanol extract (GEE), 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT) assays, melanin content measurement, reverse transcription-polymerase chain reaction (RT-PCR), and cellular tyrosinase activity assays were performed using B16F10 melanoma cell models. Treatment with GEE at concentrations of 10, 50, 100, 200, and 400 μg/mL significantly inhibited melanin synthesis in a dose-dependent manner by 46.69%, 44.42%, 27.90%, 19.37%, and —3.15%, respectively, in B16F10 cells stimulated with 3-isobutyl-1-methylxanthine (IBMX). Furthermore, treatment with GEE downregulated tyrosinase gene expression and reduced cellular tyrosinase activity to 80.42%, 78.13%, 67.26%, 64.25%, and 40.46%, respectively, compared to the control. Specifically, GEE treatment at 400 μg/mL effectively suppressed melanogenesis by decreasing tyrosinase expression and directly inhibiting tyrosinase enzymatic activity in the B16F10 cells. Therefore, GEE may be a promising natural whitening agent with potential applications in skin health and for the prevention of pigmentation related disorders.
Keywords:
Glycine max (L.) Merr, soybean, melanogenesis, melanin, tyrosinase서 론
멜라닌(melanin)은 주로 사람의 피부, 머리카락 및 눈 등에 존재하고 있으며, 외부 환경으로부터 피부조직을 보호하는 역할을 한다(Lee EJ 등 2023). 이러한 멜라닌은 피부의 가장 바깥쪽인 표피의 기저층(basal layer)에 위치하고 있는 멜라닌 세포(melanocyte)에서 합성되며, 세포소기관인 멜라닌 소체(melanosome)에서 합성이 이루어진다(Circu ML & Aw TY 2010). 이 멜라닌 소체는 수상돌기를 통하여 인접한 각질형성세포(keratinocyte)에 멜라닌을 전달하고, 각질형성세포가 표피로 점차 이동하면서 멜라닌이 피부로 나타내게 된다(Dorsky RI 등 2000). 피부에서 적절한 멜라닌 함량은 자외선에 의한 피부 손상을 보호하며 더 나아가 피부암 발생의 위험을 낮추는 것으로 알려져 있지만(Videira IF 등 2013), 과잉 생산된 멜라닌이 피부에 축적될 경우에는 오히려 기미, 주근깨 및 피부 반점 등을 포함한 피부암 및 세포 사멸과 같은 질병을 유발할 수 있다(Yoon JW 등 2013).
멜라닌 형성과 관련하여 잘 알려져 있는 효소로는 tyrosinase, TRP-1(tyrosinase-related protein-1) 및 TRP-2 (tyrosinase-related protein-2) 등이 있으며 이 중에서도 특히 멜라닌 형성의 주효소인 tyrosinase는 멜라닌 생합성의 초기 반응에 관여하는 속도제한 효소로서 tyrosinase의 발현과 함량 및 활성에 의해 멜라닌 양이 결정되며, tyrosine을 기질로 하여 DOPA(3,4-dihydroxylphenylalanine)로 전환하는 tyrosine hydroxylase 활성과 DOPA를 DOPA-quinone으로 산화하는 DOPA oxidase 활성을 모두 가지고 있다(Kim KY & Lee NK 2014). 이에 따라 최근 의료 및 화장품 산업에서 멜라닌 생성의 주요 효소인 tyrosinase 활성을 억제하는 것에 초점을 맞추고 있다(Pillaiyar T 등 2017; Pillaiyar T 등 2018).
현재까지 알려진 tyrosinase의 억제제로 사용할 수 있는 미백 물질은 ascorbic acid, kojic acid, azelaic acid 및 hydroquinone 등이 활발하게 사용되었지만, 이러한 합성 미백 소재는 대부분 알레르기 반응을 포함한 피부에 대한 안전성과 제품의 제형 안정성 등의 문제로 인하여 제한된 양만 사용하고 있으며(Imokawa G & Mishima Y 1982; Ando S 등 1993; Masuda M 등 1996), 미백 소재로 사용하기에 제한성을 가진다(Kim KY & Lee NK 2014). 또한, tyrosinase의 직접적인 소거 작용을 하는 기전만 알려져 있을 뿐 tyrosinase의 번역 단계, 발현 수준에서 저해 활성을 가지는 천연 소재에 관한 연구는 미약한 수준이다(Choung MG 등 2013). 따라서 알레르기와 같은 피부에 대한 예민 반응과 같은 한계점을 극복하기 위해 보다 부작용이 없으며, 효과적으로 tyrosinase를 조절하여 멜라닌 생성 억제 효과를 가지는 천연 소재에 관한 연구가 요구되고 있다.
대두(Glycine max (L.) Merr)는 필수아미노산의 함량이 높은 고단백 식품으로서, 우리나라를 비롯하여 동남아시아 국가 등에서 오랫동안 사용된 중요 식물 자원이다(Yoo KM 2011). 대두는 두부, 두유, 콩나물, 콩기름 및 콩가루 등으로 가공하거나 대두를 발효시켜 만든 된장, 청국장 및 간장 등으로 이용하고 있다(Xu B 등 2010; Chen KI 등 2012). 오랫동안 사용되어 온 만큼 대두의 항산화(Shukla S 등 2016), 항암(Sundaram MK 등 2018), 항고혈압(Vallabha VS & Tiku PK 2014) 및 항염(Yusof HM 등 2019) 활성 등 여러 생물학적 활성이 입증되었다. 이 밖에도 대두의 뿌리(Soares AR 등 2011) 및 파이토케미컬 성분인 글리세올린이 가지는 미백 활성에 관한 연구가 진행되었다(Lee YS 2010). 그러나 대두 추출물의 미백 등과 관련한 미용기능성 분야에 대한 연구는 미비한 실정이다.
따라서 본 연구에서는 대두 추출물의 미백 활성과 그 작용기전 규명을 통해 향후 천연 미백 소재로서의 적합성에 대해 조사하고자 하였다.
재료 및 방법
1. 실험재료 및 시약
본 연구에서는 대두 추출물의 미백 효능 및 기전을 확인하기 위해 thiazolul blue tetrazolium bromide(MTT), 3-isobutyl-1-methylxanthine(IBMX), potassium chloride, trizma base, acetic acid, L-DOPA 및 bovine serum albumin(BSA)를 Sigma-Aldrich(St. Louis, MO, USA)에서 구입하였고, dimethyl sulfoxide(DMSO) 및 isopropanol은 Junsei chemical Co., Ltd. (Tokyo, Japan)에서 구매하였으며, 94.5% ethanol은 Daejung (Seoul, Korea)에서 구매하여 사용하였다. RNase-free water, Maxime PCR Premix(i-Taq), DNA maker 및 ethidium bromide는 iNtRON Biotechnology, Inc.(Seongnam, Korea)에서 구매하였고, CycleScript RT-PreMix와 RT-PCR 분석에 사용한 모든 primer는 Bioneer corporation(Daegeon, Korea)에서 구매하였다. Ethylenediaminetetraacetic acid(EDTA), agarose, Triton X-100 및 protein assay dye 시약은 Bio-rad Laboratories, Inc. (Hercules, CA, USA)에서 구매하였고, TrizolⓇ 및 chloroform은 Thermo Fisher Scientific Inc.(Waltham, MA, USA)에서 구매하였다. 본 실험에 사용된 세포는 B16F10 세포를 배양하기 위한 Dulbecco’s modified Eagle’s medium(DMEM), fetal bovine serum(FBS), penicillin-streptomycin, trypsine-ethylenediaminetetraacetic acid(trypsin-EDTA) 및 phosphate-buffered saline(PBS)은 Welgene Inc.(Daegu, Korea)에서 구입하였다.
2. 대두 Ethanol 추출물 제조
본 연구에서는 대두 ethanol 추출물을 파이토알렉신(Gimhae, Korea)에서 제공받아 사용하였다. 제공받은 대두 ethanol 추출물은 카트리지 5 μm 폴리프로필렌 필터(SYP05-25, TOP-Filter tech, Dagjeon, Korea)로 여과시킨 후 3 hr 동안 환류 추출(MS-DM609, MISUNG Scitific, Yangju, Korea) 후 동결 건조하여 —80℃에서 추후 실험을 진행할 때까지 보관하였다. 보관해 둔 추출물은 DMSO를 용매로 하여 실험할 농도로 희석해 실험에 사용하였다. 제조한 대두 ethanol 추출물은 GEE(Glycine max (L.) Merr ethanol extract)로 명명하였다.
3. B16F10 세포 배양
본 연구에서 사용된 B16F10 세포는 KCLB(Korean cell line bank, No. 80008, Seoul, Korea)에서 분양받았다. B16F10 세포는 10% FBS 및 1% penicillin-streptomycin를 혼합한 DMEM을 사용하여 37℃, 5% CO2로 설정한 조건에서 배양하였다.
4. 세포독성 평가
GEE 처리에 의한 B16F10 세포의 독성을 조사하기 위해 B16F10 세포를 12-well plate에 분주하여 24 hr 동안 37℃, 5% CO2 조건에서 배양하였으며, GEE를 농도별로 처리한 후 같은 조건에서 24 hr 동안 배양하였다. 그 후 MTT 시약을 배지에 섞은 MTT-DMEM을 0.5 mL씩 분주하여, 1 hr 동안 반응시킨 후 배지를 제거하고 각 well마다 DMSO를 첨가하여 생성된 formazan을 용해시키고, 96-well plate에 분주해 microplate reader(VersaMax: Molecular Devices, Sunnyvale, CA, USA)를 이용해 570 nm에서 흡광도를 측정하였다. 결과는 세 번 반복한 측정값의 평균으로 표시하였으며, 세포 생존율은 아래의 식을 사용하여 계산하였다.
5. B16F10 세포에서의 멜라닌 생성 억제 측정
B16F10 세포에서 GEE 처리에 의한 멜라닌 생성을 억제 활성을 평가하여 미백 기능성을 확인하고자 하였다. 0.5 mM 농도의 IBMX를 처리하여 멜라닌 생성을 유도하였으며, GEE를 각각 10, 50, 100, 200 및 400 μg/mL의 농도로 120 hr 동안 처리하였다. 그 후 세포 외 멜라닌 함량을 측정하기 위하여 배지를 200 μL씩 96-well plate에 분주하여 microplate reader(VersaMax: Molecular Devices, Sunnyvale, CA, USA)를 이용해 405 nm에서 흡광도를 측정하였다. 또한, 세포 내 멜라닌 함량을 측정하기 위하여 trypsine-EDTA 200 μL씩 처리하여 멜라닌과 세포를 용해시켜 세포 용해물을 수집하였다. 수집한 세포 용해물을 5 min 동안 원심분리 후 상등액을 제거하고, 9:1 비율로 제조한 1N NaOH-DMSO로 용해시켜 100℃에서 10 min 동안 가열하였다. 가열 후 200 μL씩 96-well plate에 분주하여 405 nm에서 흡광도를 측정하였다. 총 멜라닌 함량은 세포 외의 멜라닌 함량과 세포 내의 멜라닌 함량을 평균으로 산출하였으며, 멜라닌 함량은 IBMX만 단독처리한 control 그룹을 100%로 하여 비교 분석하였다.
6. RT-PCR(Reverse Transcription-Polymerase Chain Reaction)에 의한 mRNA 발현 분석
GEE 처리가 멜라닌 생성에 관여하는 효소인 tyrosinase, TRP-1 및 TRP-2의 유전자 수준에 영향을 미치는지를 확인하기 위해 RT-PCR 분석을 수행하였다. B16F10 세포에 GEE를 10, 50, 100, 200 및 400 μg/mL의 농도로 처리하고 0.5 mM 농도의 IBMX를 120 hr 동안 처리하여 멜라닌 생성을 유도하였다. 120 hr 동안 처리 후 TrizolⓇ 시약을 600 μL에 처리·용해하여 획득한 용해물에 chloroform 100 μL를 첨가한 후 15 sec 동안 혼합시켰으며, 혼합물을 25℃에서 3 min 동안 정치시킨 후 4℃, 12,000 RCF, 15 min 조건에서 원심분리하였다. 원심분리 후 획득한 상등액은 isopropanol을 200 μL 첨가한 후 재현탁하여 25℃에서 10 min 동안 정치시켰다. 그 후 4℃, 12,000×g 조건으로 10 min 동안 원심분리하여 획득한 RNA 침전물을 75% ethanol 300 μL를 첨가하여 세척 후 4℃, 7,500×g, 5 min 조건에서 원심분리하였으며, 상등액은 제거하여 RNA 침전물을 건조시켜 RNase-free water를 첨가하여 용해시켰다. 분리된 RNA는 biodrop spectrophotometer (Biodrop, Cambridge, UK)를 이용하여 정량화하였고, CycleScript RT PreMix를 사용하여 48℃, 12 cycle 조건에서 cDNA를 합성하였다. 합성된 cDNA는 thermal cycler(Bio-Rad, Berkeley, CA, USA)를 사용하여 RT-PCR 분석을 수행하였으며, 멜라닌 생성에 관여하는 유전자인 tyrosinase, TRP-1 및 TRP-2의 mRNA 발현 수준은 1.5% agarose gel을 사용해 전기영동을 실시하여 유전자 발현 수준을 분석하였다. 본 실험에서는 대조군으로 β-actin과 GAPDH가 사용되었으며, 멜라닌 생성에 관여하는 유전자 tyrosinase, TRP-1 및 TRP-2의 primer sequences는 Table 1에 나타내었다.
7. B16F10 세포 내 Tyrosinase 활성 측정
멜라닌 생성에 관여하는 효소 중 핵심 효소인 tyrosinase의 활성을 B16F10 세포 내에서 측정하고자 GEE가 세포 내 tyrosinase 활성에 어떠한 영향을 미치는지를 분석하였다. 배양된 B16F10 세포를 1% triton X-100을 함유한 PBS에 처리하여 얼음 위에서 5 min 동안 정치한 뒤, 세포를 scrapper로 긁어 수확하였다. 수확한 세포는 4℃에서 20 min 동안 원심분리하여 상등액만 수집하였다. 그 후 상등액은 Bradford 시약을 통해 정량하였고 상등액은 0.1 M phosphate buffer에 용해시킨 L-DOPA와 37℃에서 2 hr 동안 반응시켜 micro-plate reader(VersaMax: Molecular Devices, Sunnyvale, CA, USA)를 이용해 475 nm에서 세포 내 tyrosinase의 활성을 측정하였다.
8. 통계분석
모든 결과 값은 평균±표준편차로 표시하였으며, 데이터의 통계처리는 SPSS software(Ver. 18, Statistical package for the social sciences Inc., Chicago, IL, USA)를 이용하여 분석하였다. 그룹 간의 유의성 평가는 일원 배치 분산분석 (one-way ANOVA)을 이용하였고, 사후 검증은 Student’s t-test 방법을 사용하여 유의성 차이를 검증하였다(*p<0.05, **p<0.01 및 ***p<0.001).
결과 및 고찰
1. B16F10 세포에서의 GEE 처리에 의한 세포 생존율 평가
B16F10 세포에 GEE를 처리하였을 때 세포 생존율에 미치는 영향을 확인하기 위하여 MTT 분석을 통해 확인하였다(Fig. 1). MTT 분석은 세포 생존율을 측정하는 방법으로, 담황색 기질인 MTT가 살아있는 대사가 활발한 세포의 미토콘드리아 내의 redoxase의 효소 작용으로 인해 환원되어 보라색의 formazan을 생성하는데, 이를 용해액으로 용해시킨 후 살아있는 세포의 수를 측정하는 방법이다(Kim YE 등 2009). DMSO만 처리한 세포를 대조군으로 하여 100%로 보고 비교하였을 경우, GEE를 10, 50, 100, 200, 400 및 800 μg/mL의 농도로 처리하였을 때, 99.12%, 104.52%, 103.82%, 106.60%, 95.91% 그리고 90.49%를 나타내었다. 따라서 추후 진행된 실험에서는 유의적 차이가 나타나지 않는 농도인 10, 50, 100, 200 및 400 μg/mL의 농도만을 선택하여 실험을 진행하였다.
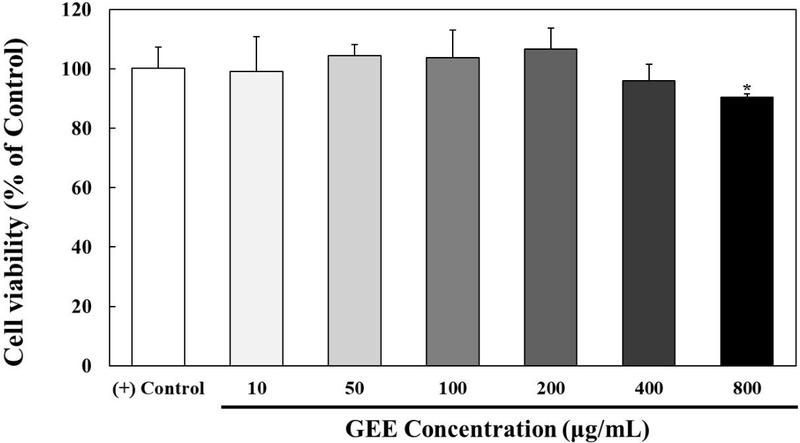
Effect of GEE treatment on the viability of B16F10 cells.B16F10 cells were incubated with 10, 50, 100, 200, 400, and 800 μg/mL for 24 hr. Subsequent experiments were progressed within the concentration range that no significant difference in cell viability. Different corresponding letters indicate significant differences by Student’s t-test (* p<0.05).(+) Control: DMSO-treated for 24 hr in B16F10 cells.GEE: Glycine max (L.) Merr ethanol extract.
2. B16F10 세포에서의 GEE 처리에 의한 멜라닌 억제 활성 평가
GEE 처리가 B16F10 세포의 멜라닌 합성에 미치는 영향을 알아보기 위해 0.5 mM IBMX로 멜라닌 생성을 유도하였으며, GEE를 10, 50, 100, 200 및 400 μg/mL의 농도로 120 hr 동안 처리하여 멜라닌 억제 활성을 평가하였다(Fig. 2). 그 결과 GEE 처리가 B16F10 세포에서 총 멜라닌 함량을 46.69%, 44.42%, 27.90%, 19.37% 및 –3.15%로 농도 의존적으로 억제시키는 것을 확인하였으며(Fig. 2A), 총 멜라닌 함량 외에도 세포 외 및 세포 내에서도 동일하게 농도 의존적으로 억제함을 확인하였으며, 세포 외의 멜라닌 함량을 농도가 증가함에 따라 53.64%, 54.86%, 30.74%, 17.89 및 –8.85%로 억제하였고(Fig. 2B), 세포 내에서는 39.73%, 33.98%, 25.06%, 20.84% 및 2.28%로 억제하였다(Fig. 2C). 또한, 현미경과 이미지를 통해 GEE 처리에 의한 멜라닌 억제 정도를 확인하였다(Fig 2D, 2E). 따라서 B16F10 세포에서 멜라닌 생합성 억제율을 통해 GEE 처리가 세포 내 멜라닌 생합성을 효과적으로 억제하는 것을 확인하였다. Bodurlar Y & Caliskan M (2022)에 의하면 대두 세포 배양 추출물이 B16F10 세포에서 멜라닌 생성을 유의하게 억제한다고 보고하였으며, 이는 대두에서 발견되는 많은 이소플라본 및 기타 페놀 화합물의 효과적인 anti-tyrosinase 및 멜라닌 합성 억제 활성에 기인한 것으로 보고 있다. 이와 관련하여 이전 연구(Park JH & Kim GN 2023)에서 GEE의 총 폴리페놀 함량을 측정하였으며, 이를 통해 GEE의 멜라닌 생성 억제 효과 또한 페놀 화합물과의 관계성이 있다고 판단할 수 있다.
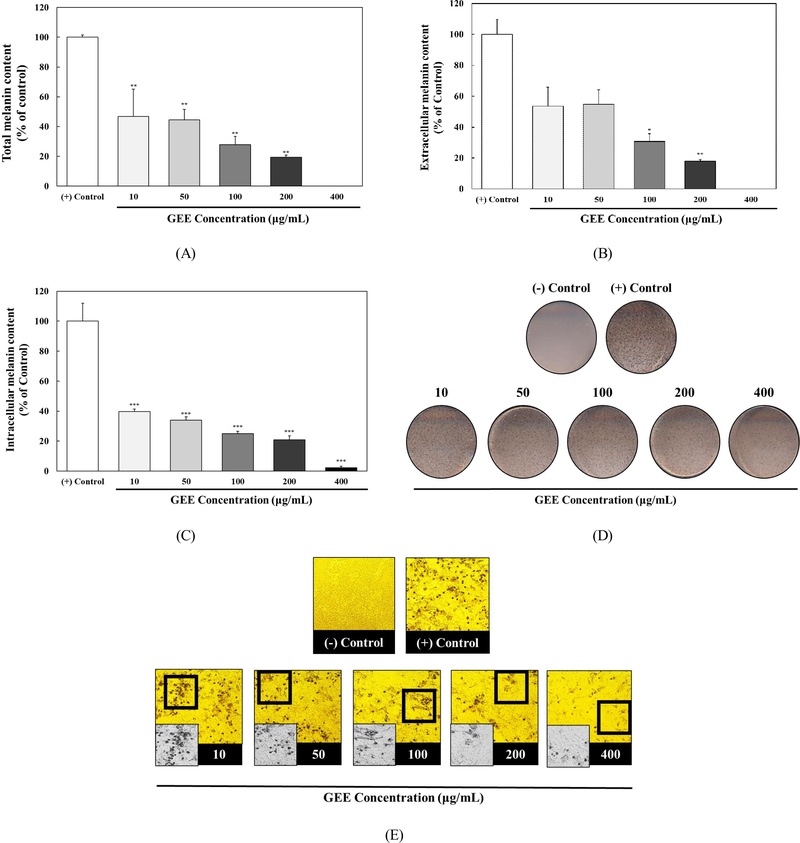
Inhibitory effect of GEE treatment on the melanin synthesis of B16F10 cells.B16F10 cells were induced by 0.5 mM IBMX to incubate in the presence or absence of 10, 50, 100, 200, and 400 μg/mL for 120 hr. Melanin contents of B16F10 cells were quantified at 405 nm (A), (B), and (C). The secreted cellular melanin content was obtained using image scanner (D) and the levels of melanin content was analyzed by photomicrograph (E). Different corresponding letters indicate significant differences by Student’s t-test (* p<0.05, ** p<0.01 and, *** p<0.001).(-) Control: No treatment.(+) Control: 0.5 mM IBMX-treated for 120 hr in B16F10 cells.GEE: Glycine max (L.) Merr ethanol extract.
3. GEE 처리가 B16F10 세포의 멜라닌 생성에 관련된 유전자의 발현에 미치는 영향
멜라닌의 생성은 멜라닌 생성에 관련된 효소의 발현 및 멜라노좀을 통해 이동하는 과정에 의해서도 조절되며(Choe YS & Choe TB 2014), 멜라닌 생성 초기 반응에 작용하는 효소인 tyrosinase는 L-tyrosine을 L-DOPA로 hydroxylase하고, L-DOPA는 TRP-1 및 TRP-2 등의 효소가 관여하여 최종적으로 멜라닌이 합성된다(Yoon YM 등 2013). 또한, 세포 내에서 미백 효과는 tyrosinase의 발현 억제 및 tyrosinase의 활성을 감소시켜 멜라닌 생성에 미치는 영향을 파악함으로써 확인할 수 있다(Park SI 등 2021). 본 실험에서는 RT-PCR을 통하여 B16F10 세포에서 GEE 처리가 멜라닌 생성에 관여하는 대표적 유전자인 tyrosinase, TRP-1 및 TRP-2의 mRNA 발현 수준에 미치는 영향을 알아보고자 하였다(Fig. 3). GEE를 10, 50, 100, 200 및 400 μg/mL의 농도로 120 hr 동안 처리하였을 때, GEE 처리는 TRP-1 및 TRP-2의 발현에는 아무런 영향을 미치지 않았지만(Fig. 3B), 멜라닌 생성 과정 중 핵심 요소인 tyrosinase의 발현은 유의미하게 하향 조절하였다(Fig. 3A). 이를 정량화한 결과 IBMX로 멜라닌을 유도한 (+) 대조군에 대비하여 GEE를 농도별로 처리하였을 때 농도가 증가함에 따라 tyrosinase의 발현이 감소함을 확인하였으며, 가장 높은 농도인 400 μg/mL의 농도에서는 (+) 대조군에 대비하여 2배 이상의 tyrosinase 발현을 감소시킴을 확인하였다(Fig. 3C). Shin SH & Lee YM(2013)에서 대두의 글리세올린은 B16F10 세포에서 멜라닌 세포 특이적 단백질인 tyrosinase 발현의 유의한 하향 조절을 통하여 미백 효과를 나타낸다고 보고된 바 있다.
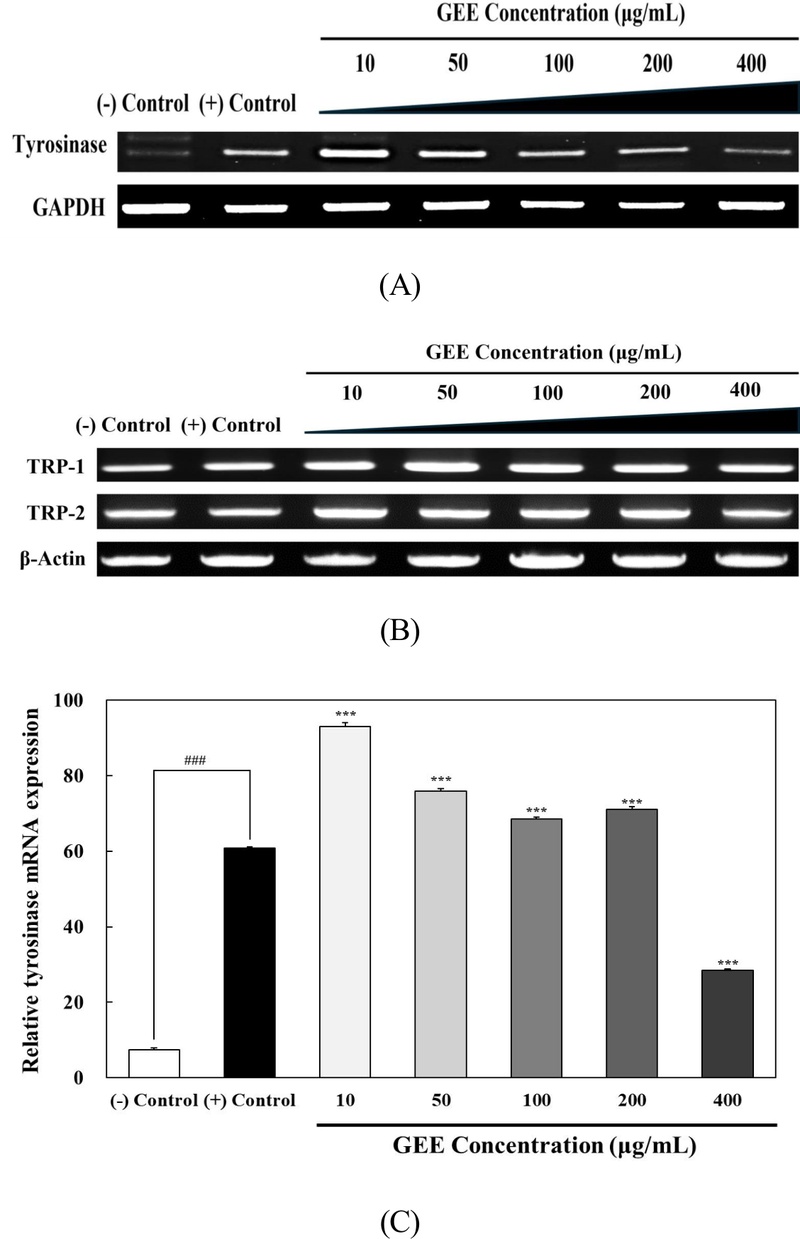
Effect of GEE treatment on the mRNA expression levels of melanogenesis-related genes in B16F10 cells.The total RNA of B16F10 cells were isolated by TrizolⓇ reagent. The mRNA expression levels of melanogenesis-related genes such as tyrosinase, TRP-1 and TRP-2 were determined by RT-PCR (A) and (B). The mRNA expression levels of tyrosinase was quantified using Image J program (C). GAPDH and β-actin were used as a control. Different corresponding letters indicate significant differences by Student’s t-test (*** p<0.001 and ### p<0.001).(–) Control: No treatment.(+) Control: 0.5 mM IBMX-treated for 120 hr in B16F10 cells.GEE: Glycine max (L.) Merr ethanol extract.GAPDH: Glyceraldehyde 3-phosphate dehydrogenase.TRP-1: Tyrosinase related protein-1.TRP-2: Tyrosinase related protein-2.
4. B16F10 세포 내에서 GEE 처리에 의한 Tyroinsae의 활성 감소
멜라닌 합성 과정의 주된 효소인 tyrosinase는 생체 내에서 tyrosine으로부터 DOPA와 DOPA quinone을 거쳐 최종적으로 멜라닌 고분자를 생합성할 때 관여하는 효소이므로 멜라닌 세포에서의 tyrosinase의 활성은 피부 멜라닌 생성에 결정적인 영향을 미치게 된다(Li W & Hill HZ 1997). 따라서 GEE 처리가 B16F10 세포 내에서 tyrosinase의 활성 자체에 영향을 미치는지를 알아보기 위해 세포 내 tyrosinase의 활성을 측정하였다(Fig. 4). GEE를 10, 50, 100, 200 및 400 μg/mL의 농도로 120 hr 동안 처리하였을 때, tyrosinase의 활성은 IBMX만 단독으로 처리한 대조군 그룹과 비교하여 80.42%, 78.13%, 67.26%, 64.25% 및 40.46%로 농도 의존적으로 감소시키는 것을 확인하였다. 대두의 isoflavone 성분인 글리시테인과 다이드제인의 대사 산물인 6,7,4′-trihydroxyisoflavone은 강력한 tyrosinase 활성 저해를 보이는 것으로 보고된 바 있으며(Chang TS 등 2005), 이 밖에도 대두의 다이진, 제니스테인 등은 anti-tyrosinase의 특성이 있는 것으로 보고되었다(Loizzo MR 등 2012). 이를 통해 GEE 처리는 tyrosinase의 유전자 발현 수준을 억제하는 것뿐만 아니라 세포 내에서 tyrosianse 활성 또한 억제하여 B16F10 세포에서 멜라닌 생성을 감소시킨다는 것을 알 수 있다.
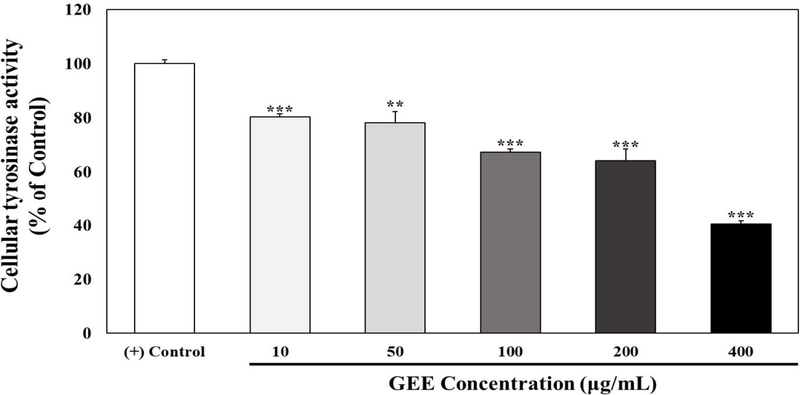
Inhibitory effect of GEE treatment on tyrosinase activity in B16F10 cells.Intracellular tyrosinase activity was determined with L-DOPA as the substrate. Different corresponding letters indicate significant differences by Student’s t-test (** p<0.01 and *** p<0.001).(–) Control : No treatment.(+) Control : 0.5 mM IBMX-treated for 120 hr in B16F10 cells.GEE : Glycine max (L.) Merr ethanol extract.
요 약
본 연구에서는 B16F10 세포에서 GEE 처리가 멜라닌 생성 억제 효과에 관한 기전을 규명하여 천연 미백 소재로서의 적합성을 검증하고자 하였다. 실험 결과 10, 50, 100, 200 그리고 400 μg/mL 농도로 GEE 처리하였을 때, B16F10 세포에서 농도 의존적으로 효과적인 멜라닌 생성 억제 효과를 나타내었으며, 멜라닌 생성에 관여하는 가장 주요한 tyrosinase만을 특이적으로 억제하는 것을 확인하였다. 대두 추출물은 tyrosinase의 유전자 발현량을 효과적으로 감소시켰으며, 이뿐만 아니라 세포 내에서 tyrosinase의 활성 또한 유의미하게 억제시키는 것을 확인하였다. 특히, 400 μg/mL 농도로 처리한 GEE에서 IBMX를 처리하여 멜라닌을 유도한 (+) control에 대비하여 우수한 멜라닌 축적 억제 활성을 나타냄을 확인하였으며, 높은 tyrosinase 저해 활성을 나타내었다. 따라서 GEE 처리에 의한 멜라닌 생성 억제 효과는 tyrosinase의 mRNA 발현 수준 감소와 활성 억제에 기인한 것이라고 판단되며, 이를 토대로 대두가 tyrosinase를 저해하는 향후 효과적인 천연 미백 소재로서 활용될 가능성이 높다고 생각된다.
REFERENCES
-
Ando S, Ando O, Suemoto Y, Mishima Y (1993) Tyrosinase gene transcription and its control by melanogenic inhibitor. J Invest Dermatol 100(2 Suppl): 150S-155S.
[https://doi.org/10.1111/1523-1747.ep12465056]

-
Bodurlar Y, Caliskan M (2022) Inhibitory activity of soybean (Glycine max L. Merr.) cell culture extract on tyrosinase activity and melanin formation in alpha: Melanocyte stimulating hormone-induced B16-F10 melanoma cells. Mol Biol Rep 49(8): 7827-7836.
[https://doi.org/10.1007/s11033-022-07608-6]

-
Chang TS, Ding HY, Lin HC (2005) Identifying 6,7,4′-trihydroxyisoflavone as a potent tyrosinase inhibitor. Biosci Biotechnol Biochem 69(10): 1999-2001.
[https://doi.org/10.1271/bbb.69.1999]

-
Chen KI, Erh MH, Su NW, Liu WH, Chou CC, Cheng KC (2012) Soyfoods and soybean products: From traditional use to modern applications. Appl Microbiol Biotechnol 96(1): 9-22.
[https://doi.org/10.1007/s00253-012-4330-7]

- Choe YS, Choe TB (2014) Melanogenesis inhibitory effects of Allium hookeri extract in B16F10 mouse melanoma cell. Asian J Beauty Cosmetol 12(2): 163-168.
-
Choung MG, Hwang YS, Kim GP, Ahn KG, Shim HS, Hong SB, Choi JH, Yu CY, Chung IM, Kim SH, Lim JD (2013) Antimelanogenic effect and whitening of anthocyanin rich fraction from seeds of Liriope platyphylla. Korean J Medicinal Crop Sci 21(5): 361-371.
[https://doi.org/10.7783/KJMCS.2013.21.5.361]

-
Circu ML, Aw TY (2010) Reactive oxygen species, cellular redox systems, and apoptosis. Free Radic Biol Med 48(6): 749-762.
[https://doi.org/10.1016/j.freeradbiomed.2009.12.022]

-
Dorsky RI, Moon RT, Raible DW (2000) Environmental signals and cell fate specification in premigratory neural crest. Bioessays 22(8): 708-716.
[https://doi.org/10.1002/1521-1878(200008)22:8<708::AID-BIES4>3.0.CO;2-N]

- Imokawa G, Mishima Y (1982) Loss of melanogenic properties in tyrosinases induced by glycosylation inhibitors within malignant melanoma cells. Cancer Res 42(5): 1994-2002.
- Kim KY, Lee NK (2014) Herbal extracts research trend that have effects on melanin production and control. Asian J Beauty Cosmetol 12(4): 453-461.
-
Kim YE, Yang JW, Lee CH, Kwon EK (2009) ABTS radical scavenging and anti-tumor effects of Tricholoma matsutake Sing. (pine mushroom). J Korean Soc Food Sci Nutr 38(5): 555-560.
[https://doi.org/10.3746/jkfn.2009.38.5.555]

-
Lee EJ, Jang YS, Hong IK (2023) Inhibitory effect of lamb placenta peptide powder on melanogenesis. Korean J Food Sci Technol 55(3): 220-228.
[https://doi.org/10.9721/KJFST.2023.55.3.220]

- Lee YS (2010) Effects of soybean fermented extract glyceollins on skin whitening. Ph D Dissertation Gyeongbuk National University, Daegu. pp 17-18.
-
Li W, Hill HZ (1997) Induced melanin reduces mutations and cell killing in mouse melanoma. Photochem Photobiol 65(3): 480-485.
[https://doi.org/10.1111/j.1751-1097.1997.tb08594.x]

-
Loizzo MR, Tundis R, Menichini F (2012) Natural and synthetic tyrosinase inhibitors as antibrowning agents: An update. Compr Rev Food Sci Food Saf 11(4): 378-398.
[https://doi.org/10.1111/j.1541-4337.2012.00191.x]

- Masuda M, Tejima T, Suzuki T, Imokawa G (1996) Skin lighteners. Cosmetics and Toiletries 111(10): 65-77.
-
Park JH, Kim GN (2023) In vitro antioxidant and tyrosinase inhibitory activities of Glycine max (L.) Merr ethanol extract. J East Asian Soc Diet Life 33(4): 323-330.
[https://doi.org/10.17495/easdl.2023.8.33.4.323]

- Park SI, Yoon HR, Shin JH, Lee SJ, Kim DY, Lee HM (2021) Tyrosinase inhibitory activity and melanin production inhibitory activity of taraxinic acid from Taraxacum coreanum. Korean J Plant Res 34(4): 368-376.
-
Pillaiyar T, Manickam M, Jung SH (2017) Recent development of signaling pathways inhibitors of melanogenesis. Cell Signal 40: 99-115.
[https://doi.org/10.1016/j.cellsig.2017.09.004]

-
Pillaiyar T, Namasivayam V, Manickam M, Jung SH (2018) Inhibitors of melanogenesis: An updated review. J Med Chem 61(7): 7395-7418.
[https://doi.org/10.1021/acs.jmedchem.7b00967]

-
Shin SH, Lee YM (2013) Glyceollins, a novel class of soybean phytoalexins, inhibit SCF-induced melanogenesis through attenuation of SCF/c-kit downstream signaling pathways. Exp Mol Med 45(4): e17.
[https://doi.org/10.1038/emm.2013.20]

-
Shukla S, Park JY, Kim DH, Hong SY, Lee JS, Kim MH (2016) Total phenolic content, antioxidant, tyrosinase and α-glucosidase inhibitory activities of water soluble extracts of noble starter culture Doenjang, a Korean fermented soybean sauce variety. Food Control 59: 854-861.
[https://doi.org/10.1016/j.foodcont.2015.07.003]

-
Soares AR, de Lourdes Lucio Ferrarese M, de Cássia Siqueira-Soares R, Marchiosi R, Finger-Teixeira A, Ferrarese-Filho O (2011) The allelochemical L-DOPA increases melanin production and reduces reactive oxygen species in soybean roots. J Chem Ecol 37(8): 891-898.
[https://doi.org/10.1007/s10886-011-9988-2]

-
Sundaram MK, Ansari MZ, Al Mutery A, Ashraf M, Nasab R, Rai S, Rais N, Hussain A (2018) Genistein induces alterations of epigenetic modulatory signatures in human cervical cancer cells. Anticancer Agents Med Chem 18(3): 412-421.
[https://doi.org/10.2174/1871520617666170918142114]

-
Vallabha VS, Tiku PK (2014) Antihypertensive peptides derived from soy protein by fermentation. Int J Pept Res Ther 20: 161-168.
[https://doi.org/10.1007/s10989-013-9377-5]

-
Videira IF, Moura DF, Magina S (2013) Mechanisms regulating melanogenesis. An Bras Dermatol 88(1): 76-83.
[https://doi.org/10.1590/S0365-05962013000100009]

-
Xu B, Chang SK, Liu Z, Yuan S, Zou Y, Tan Y (2010) Comparative studies on the chemical and cell-based antioxidant activities and antitumor cell proliferation properties of soy milk manufactured by conventional and commercial UHT method. J Agric Food Chem 58(6): 3558-3566.
[https://doi.org/10.1021/jf903796c]

-
Yoo KM (2011) Effect of soybean varieties on the physi-cochemical and sensory characteristics of Tofu. Korean J Food Nutr 24(3): 451-457.
[https://doi.org/10.9799/ksfan.2011.24.3.451]

-
Yoon JW, Han JM, Yoon HJ, Ko WS (2013) Inhibitory effects of methanol extract of Kaempferia galanga on melanogenesis in B16/F10 melanoma cells. J Korean Med Ophthalmol Otolaryngol Dermatol 26(1): 1-18.
[https://doi.org/10.6114/jkood.2013.26.1.001]

- Yoon YM, Bae SH, An SK, Choe YB, Ahn KJ, An IS (2013) Effects of ultraviolet radiation on the skin and skin cell signaling pathways. Asian J Beauty Cosmetol 11(3): 417-426.
-
Yusof HM, Ali NM, Yeap SK, Ho WY, Beh BK, Kor SP, Long K, Alitheen NB (2019) Anti-inflammatory, analgesic and acute toxicity effects of fermented soybean. BMC Complenment Altern Med 19(1): 373.
[https://doi.org/10.1186/s12906-019-2791-2]


