
락토페린의 기능과 역할에 관한 문헌 고찰


Abstract
In this study, we recently reported a high correlation between lactoferrin and health and summarized the related research. Lactoferrin has significant advantages over other chemical drugs because milk basic protein (MBP) derived from food has fewer side effects and higher stability. In addition, it can minimize the clinical and financial risks of the research period and the subjects. Lactoferrin is abundant in the colostrum. It affects osteoporosis, immune function regulation, and inflammatory diseases. It is therefore used as a health functional food in various commercial products such as nutritional supplements, infant formula, cosmetics, and toothpaste. It is expected that the utility of lactoferrin in the medical field will increase in the future. Therefore, it is important to accelerate animal testing and clinical studies of lactoferrin and undertake the synthesis, purification, and mass production of recombinant lactoferrin.
Keywords:
lactoferrin, osteoporosis, immunity, inflammatory disease, central nervous system diseases, cancer서 론
의학의 발달은 인간의 생명을 연장시켰으며, 이로 인한 노인 인구의 증가는 초고령 사회 진입을 단축시켰다. 따라서 우리의 생활 속에서 노후에 얼마나 건강을 유지하면서 사느냐가 삶의 큰 비중을 차지하게 되었다. 인간의 건강한 삶에 대한 욕망은 노화로 인해 발생되는 갱년기 장애, 근감소증, 안과 질환, 고혈압 및 당뇨병과 같은 심뇌혈관질환, 암 등의 질환 발병을 늦추기 위해 노력하고 있으며, 이러한 사회적 문제점을 개선하기 위해 다양한 기능성 소재에 대한 관심도가 증가하였다. 그중 우유 속 함유 성분에 대한 장 발달 및 면역 촉진 기능이 알려지고, 여러 우유 유래 생리 활성 물질이 발견되면서 우유 염기성 단백질(milk basic protein; MBP)에 관심이 모아지고 있다(Han RH 등 2019). 선행연구(Han RH 등 2019)에서는 우유 생리활성 물질은 가격이 저렴하고, 식품에서 유래했기 때문에 다른 화합물에 비해 안정성이 높고, 적용 범위가 넓어서 식품으로서 폭넓게 사용이 가능하다고 보고하였다. MBP는 우유 속에 함유되어 있는 특정 단백질 성분이다. MBP의 구성은 락토페린(lactoferrin; LF)과 락토페록시다아제(lactoperoxidase)가 주를 이루며, 초유에 많이 함유되어 있는 미량의 성분들의 복합체이다.
이 중에서 락토페린은 주로 유즙에 포함되어 있으며(Nuijens JH 등 1996), 당단백질이고, 미생물 감염에 대한 방어작용이 있는 것으로 보고되었다(Anderson BF 등 1989; Wang B 등 2019). 락토페린은 Sorensen M & Sorensen SPL (1939)에 의해 1939년 소젖에서 처음 분리된 고도의 단백질로서 우유와 타액과 같은 포유류의 외분비 분비물에 다량 존재하며(Sorensen M & Sorensen SPL 1939), 눈물ㆍ점액ㆍ백혈구ㆍ정액ㆍ기관지 분비물에서도 발견되었다(Ryu YK & Kim WS 2009). 락토페린은 1960년에는 Johanson B(1960)에 의해 사람 모유에서 확인되었으며, 사람의 모유(약 6∼8 mg/L)에 가장 많이 존재한다. 또한 소의 초유(약 0.02∼0.2 mg/L)에도 소량 존재하나, 일반적으로 생산되는 우유 1 L당 락토페린 함량은 0.1∼0.2 mg에 불과하며, 돼지ㆍ생쥐 및 말의 젖에는 각각 0.2 mg/mL 및 2 mg/mL가 함유된 반면에, 쥐ㆍ토끼 및 개 젖에는 적은 양 0.05 mg/mL가 함유되어 있다(Hirai Y 등 1990; Iyer S & Lönnerdal B 1993; Levay PF & Viljoen M 1995; Steijns JM 2001; Karav S 등 2017). 락토페린은 초유에 다량 존재하는 항바이러스 항균성 물질이며(Wang B 등 2019), 지질 산화 방지, 미생물총의 개선, 면역력 강화, 항균 작용의 효과 및 여드름 등의 피부질환 개선에 도움을 준다고 보고되었다(Karav S 등 2017). 락토페린은 주로 영양 보충제, 유아용 조제분유, 화장품 및 치약과 같은 상용 제품에 추가되고 있다. 락토페린은 온도 및 기타 물리 화학적 스트레스로 인한 변성에 민감하며(Wang B 등 2019), 락토페린의 추출, 분말 형성 공정 및 락토페린 함유 제품의 가공 매개 변수는 원치 않는 변성을 최소화하기 위해 최적화되어야 한다고 보고되고 있다(Wang B 등 2019).
따라서 본 연구에서는 건강과 관련하여 최근 사회적으로 이슈가 되고 있는 락토페린에 대해 골다공증 예방, 면역기능 조절, 항균 및 항염증 질환 예방, 중추신경계 질환 예방, 암 예방, 락토페린의 생산 및 산업 발달에 응용 등에 대해 정리 및 향후 연구 방향과 제안점 등을 제시하였다.
연구방법
본 논문은 락토페린의 생리활성을 연구를 위해 3단계로 나누어 총설을 작성하였다. 1단계는 락토페린의 정의와 내용을 문헌 검색을 통해 확인하였다. 2단계는 선정된 문헌의 연구적 배경을 바탕으로 내용을 서술하였다. 3단계는 본 논문에서 피력하고자 했던 내용에 대해 객관적으로 내용을 분석하고, 해석하였으며, 결론을 유추하였다(Shin MY & Kwun IS 2016). 본 문헌의 검색과 결과의 정리 기간은 2025년 6월 3일부터 2025년 7월 17일까지 이루어졌으며, 문헌 검색은 database로서 PubMed와 국내 각각의 학회 사이트를 활용하였다. 문헌 검색은 ‘lactoferrin, MBP, milk, osteoporosis, immunity, antioxidant, antibacterial, inflammatory disease, central nervous system, cancer’ 등의 용어들을 사용하여 검색하였으며, 총 90여 편의 논문을 참고하여 총설을 작성하였다.
결과 및 고찰
1. 락토페린의 구조 및 특징
락토페린은 락토(lacto)=젖(milk) 중에 페린(ferrin)=철과 결합하는 붉은 단백질이다(Kim SH 2012). 락토페린은 비헴 철 결합 단백질에 속하며, 철과 높은 친화도로 결합해 철에 민감한 장내 미생물에 미생물 압력을 가한다(Han RH 등 2019). 반면에, 철과 결합하지 않은 락토페린(아포락토페린; apo-lactoferrin)은 무색이다(Shimazaki K 2000). 락토페린은 692개의 아미노산으로 구성되었으며, 분자량은 약 82 KDa의 금속 결합성 당단백질이다(González-Chávez SA 등 2009; Singh J 등 2022; Chen R 등 2024). 락토페린의 3차원적 구조의 경우 80% 이상이 homology를 가지고, N, C-lobe로 나누어져 있으며, 각각 하나의 철 결합 부위를 가지고 있다(Fig. 1)(Anderson BF 등 1987). 락토페린을 N-말단, C-말단, 전체 부위를 COS-1 세포에 발현시켜 전사활성을 측정한 결과, C-말단 쪽은 전사활성이 없었으나, N-말단 90개 아미노산 부위(NIa)가 전사활성을 가지고 있음이 규명되었다(Anderson BF 등 1989). 락토페린은 금속 결합성 당단백질이기 때문에 2개의 로브(lobe)에 각각 하나씩 2가 철 이온과 결합하고 있다(Kim SH 2012)(Fig. 1). 선행연구(Tomita M 등 1994)에서 보면, 락토페린을 펩신으로 분해하면, 사람의 락토페린에서 47개의 아미노산으로 구성된 펩티드(lactoferricin-H)가 생성되고, 소의 락토페린에서는 25개의 아미노산으로 구성된 펩티드(lactoferricin-B)가 생성되는데, 이들 lactoferricin은 락토페린보다 항균성이 강한 것으로 보고되었다. 락토페린은 생체 내 철 이온을 운반 및 저장의 기능을 가지고 있으며, 생체 내에서 철의 항상성 유지에 관여한다(Anderson BF 등 1989; Yu DY 1997). 또한 락토페린은 철 이온뿐만 아니라, 구리, 아연, 알루미늄, 코발트, 칼슘 등 많은 금속이온과 결합한다. 락토페린은 초유를 비롯한 타액선, 담관, 유선과 같은 체액성 분비물에도 포함되어 있다(Ryu YK & Kim WS 2009). 락토페린의 주요 기능으로는 골다공증 예방, 면역 반응 부활, 항균 작용, 항염증 작용 및 항암 작용 등이 알려져 있다(Shimazaki K 2000; Kim SH 2012; Kowalczyk P 등 2022).
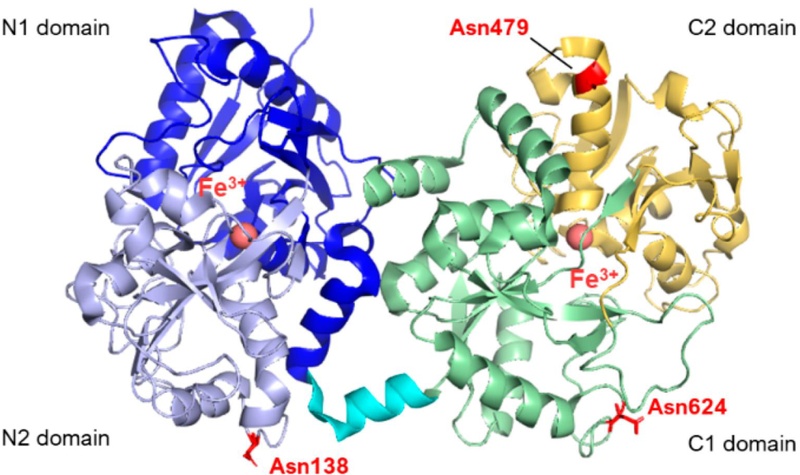
Structure of human lactoferrin. Lobes N and C are represented in different colors (blue and lavender for N1 and N2, green and yellow for C1 and C2, respectively), and the α-helix connecting the two domains is in cyan.The three glycosylation sites are highlighted in red (PDB: 2BJJ). Image created with PyMOL Molecular Graphic System version 3.0 Schrödinger, LLC.출처: Piacentini R, Boffi A, Milanetti E (2024) Lactoferrins in their interactions with molecular targets: A structure-based overview. Pharmaceuticals 17(3): 398.
2. 락토페린의 기능
MBP의 구성성분인 락토페린은 골 침착(골 형성)을 촉진하고, 골 흡수를 억제하여 골 손실을 예방하는 데 효과적인 물질이다(Table 1). 마이크로컴퓨터 단층 촬영에 의한 분석을 통해 MBP를 탈 이온수에 첨가하여 투여한 흰쥐의 경우 경골 피질 골밀도와 대퇴골 섬유주 골 부피를 증가시켰으며, in vitro 실험에서 MBP가 조골세포 증식을 촉진하고, 파골 세포 형성을 억제하는데(Yoneme H 등 2015), 이는 IGF-1의 혈장 수준에 영향을 받는다고 보고하였다(Ono-Ohmachi A 등 2017). 흰쥐의 생체 실험에서 3주 동안 MBP를 섭취시킨 결과, 혈장 그렐린(ghrelin) 농도와 뒷다리 경골의 골밀도가 증가하였으며, MBP에 의해 상승된 그렐린 수치는 뼈 형성을 위한 매개체 역할을 한다고 보고하였다(Ishida Y 등 2017). MBP는 급성 구강 독성 연구, 기형학 연구, 아만성 구강 독성 연구 및 역돌연변이 분석에서도 연구되었으며, 치료 관련 부작용은 발견되지 않았다고 보고하였다(Kruger CL 등 2007). 6개월 동안 35명의 가임 여성을 대상으로 위약군과 MBP(하루 40 mg) 섭취군으로 나누어 실험한 연구(Uenishi K 등 2007)에서 MBP 섭취군이 요추 골밀도 및 혈청 오스테오칼신이 유의하게 증가하였다. MBP 보충제를 섭취한 건강한 가임 여성과 폐경기 여성을 대상으로 한 연구(Kumegawa M 2006)에서 MBP는 뼈 형성을 촉진하고 뼈 흡수를 억제하여 골밀도를 증가시켰으며, 우유를 싫어하는 여성에 있어서 MBP 보충제 섭취는 뼈 건강에 효과적이라고 보고하였다. 또한 MBP 보충제는 흰쥐의 경골의 골절 치유 및 뼈 강도를 향상시킬 수 있으며, MBP는 뼈 골절 환자의 이차 골절을 예방하기 위해 안전하고 저렴하며 쉽게 관리할 수 있는 영양성분이 될 수 있음을 시사하였다(Toba Y 등 2000; Yoneme H 등 2015). 하루에 300 mg의 MBP가 함유된 실험용 음료를 정상 성인 남성 30명에게 16일 동안 섭취시킨 연구(Toba Y 등 2001)에서 혈청 오스테오칼신(osteocalcin) 농도를 증가시켰으며, 소변 NTx 배설은 감소하였다고 보고하였는데, 이는 MBP가 뼈 재형성의 균형을 유지하면서 뼈 형성을 촉진하고 뼈 흡수를 억제함을 시사한다고 보고하였다. 세포 석회화의 지표인 Alizarin Red S 염색 강도는 MBP 처리(100 µg/mL) 세포에서 처리되지 않은 대조군 세포보다 낮았고, 콜라겐 형성을 도와 MBP가 석회화로의 분화를 억제함으로써 연골 세포의 증식을 촉진함을 시사하였다(Nakatani S 등 2019). 서러브레드(Thoroughbred) 말의 뼈 대사와 MBP에 대한 연구에서는 90일 동안 MBP를 1 g씩 섭취시킨 결과 혈청 오스테오칼신이 45일 이후 증가하였으며, 이는 MBP의 지속적인 섭취가 말의 뼈 형성에 영향을 미친다고 보고하였다(Inoue Y 등 2006). MBP를 첨가한 분획은 생체 내 뼈 대사를 개선하고 파골 세포에 의한 뼈 재흡수를 억제하며, 시험관 내에서 마우스 조골 세포 MC3T3-E1 세포 증식을 촉진한다. CysC은 MC3T3-E1 세포 증식 촉진에 기여하여 함량이 높은 MBP는 골 대사를 보다 효과적으로 개선한다고 보고하였다(Yasueda T 등 2018). 쥐의 치주염에서 MBP가 치조골 손실을 회복할 수 있는지를 조사한 결과 치주염의 치조골 손실 회복에 효과적이라고 보고하였다(Seto H 등 2007). MBP 속의 락토페린과 뼈 조직의 연관성 연구(Park HS & Kim HJ 2015)에서는 뼈의 형성 및 흡수를 조절하는 뼈모세포(osteoblast) 및 뼈파괴세포(osteoclast) 상호조절에 있어서 락토페린이 미치는 영향을 보고하고 있다. 또한 뼈에서 락토페린은 파골세포 분화를 억제시켜서 골 형성을 도와주며, 골아세포에 있어서 동화인자로 작용하고, 골아세포를 활성시키는 사이토카인으로써 골 형성 단백질과 염기성선 유아세포 증식인자로 알려져 있다(Park HS & Kim HJ 2015). 이에 고령화 시대에 골다공증으로 다양한 건강 문제가 발생되고 있는데(Ryu YK & Kim WS 2009), 지속적인 락토페린의 섭취는 골다공증에서 뼈의 콜라겐 양 증가 및 골밀도 개선에 도움을 줄 것으로 사료된다.
락토페린은 호중구의 secondary granules의 주요한 성분이며(Kovacic B 등 2014; Li NC 등 2024), 염증 반응 시 호중구 세포 밖으로 분비되어 myelopoiesis의 조절, NK 세포의 활성화, granulopoiesis의 억제, Killer 세포의 활성화 자극 등의 면역 반응에 작용한다(Nishiya K & Horwitz PA 1982; Rado TA 등 1987; Slater K & Fletcher J 1987; Berthon BS 등 2022)(Table 2). 또한 선행연구(Penco S 등 1995; Sorimachi K 등 1997; Choe YH & Lee SW 1999; Tung YT 등 2013; Han RH 등 2019)에서 락토페린은 인터루킨-1β, 인터루킨-8, TNF-α, NO, GM-CSF와 같은 사이토카인의 분비와 생성에 영향을 준다고 보고하였으며, 면역 조절, 혈관 생성 억제(antiangiogenic), 세포 자살 활성 및 항염증 기능을 가진다고 보고하였다. 특히 Liposomal lactoferrin 제재의 경우 일반 젖소 락토페린보다 동물실험(쥐)에서 TNF-α의 생산을 억제했다고 보고하였으며(Ryu YK & Kim WS 2009), 이에 젖소 락토페린을 함유한 리보솜은 염증성 질환의 치료 및 예방(Ryu YK & Kim WS 2009)에 효과적으로 사용이 가능할 것으로 사료된다.
자가 면역 질환 및 알레르기와 같은 T 세포 관련 염증성 질환에서 MBP의 새로운 기능을 조사하기 위해 식품에서 오브알부민(ovalbumin; OVA) 특정 T 세포의 원인 반응에 대한 MBP의 효과를 평가한 연구에서는 MBP 보충제에 의한 MLN과 골수 모두에서 T 세포 활성화를 억제하면 과도한 IL-4 생성 및 장 병증을 동반한 골 손실로 인한 IgE 수치 증가를 예방할 수 있다고 제시하였으며, MBP가 T 세포 관련 염증과 뼈 손실을 모두 약화시키는 데 도움이 된다고 보고하였다(Ono-Ohmachi A 등 2018). 락토페린과 T 세포의 수용체 간의 결합에 있어서 N-로브의 도메인-Ⅰ부위가 관여하며(Leveugle B 등 1993), 소장점막 상피조직에서도 락토페린 수용체가 발현되는 것으로 보고되었다(Hu WL 등 1988). 선행연구(Han RH 등 2019)에서는 락토페린은 세포 성장과 분화 조절 및 면역 반응에 영향을 주므로 미생물 형성 환경에서 중요한 역할을 하기 때문에 종양 성장을 억제하여 암 치료제로 적용될 수 있다고 보고하였다. 특히 재조합 락토페린의 투여는 폐암 환자의 평균 생존률을 65%까지 연장시켰으며, 동일한 락토페린을 화학 요법의 보조제로 사용하자 폐암 환자의 생존율이 현저히 향상되었다고 보고하였다(Digumarti R 등 2011; Han RH 등 2019). 또한 소에서 추출한 락토페린을 하루에 3 g씩 섭취한 성인은 결장에서 adenomatous polyps 성장이 두드러지게 억제되었으며(Kozu T 등 2009), 또 다른 연구(Sun X 등 2012; Han RH 등 2019)에서는 유방암 화학치료요법 효과를 향상시킬 수 있다고 제안하였다. 최근 수용체 및 종양 증식을 조절하는 광범위한 분자 표적, 생존, 이동, 침입 및 전이 등 여러 분자 메커니즘 세포의 조절을 포함하여 락토페린의 근본적인 항암 활성이 밝혀지고 있다(Wang Y 등 2020). 또한 락토페린은 LPS(lipopolysaccharide)와 상호작용을 일으켜 세균성 내독소에 의한 마크로파지(macrophage)의 활성을 감소시키고, 세균 감염에 의한 패혈증을 억제한다(Appelmelk BJ 등 1994).
선행연구(Arnold RR 등 1982)에서는 미생물의 생육에 필요한 철 이온을 락토페린이 chelate 함으로써 증식을 억제하는 작용으로 철의 요구성이 높은 미생물에 대해 정균 및 항균 효과가 높은 것으로 보고되었고, 락토페린의 등전점이 염기성이므로 세포의 전하(–)를 중화하여 응집시키는 효과가 있으며, 면역 글로블린과 상호작용을 통해 항균 작용을 상승시키는 것으로 보고되었다(Table 3). 생체 외 실험에서 재조합된 락토페린은 Staphylococcus aureus, Escherichia. coli, Pseudomonas aeruginosa, Helicobacter pylori, Candida albicans, Bacillus subtilis, Vibrio cholerae를 포함한 병원성 미생물들의 성장을 억제하였으며, HIV, herpesvirus, hepatitis B, human cytomegalovirus, hepatitis C, hantavirus, human papillomavirus, rotavirus, adenovirus, influenza A의 증식을 억제하였다고 보고하였다(Berlutti F 등 2011; Brock JH 2012; Han RH 등 2019). 대장균에 감염된 흰쥐에게 소의 락토페린을 경구 투여한 결과, 장내 패혈증이 감소하였으며(Edde L 등 2001), 과저체중으로 태어난 미숙아에게 소의 락토페린을 투여한 결과, 생후 45일 동안 위약 치료에 비해 세균성 패혈증 발생률이 70% 감소하였다고 보고하였다(Manzoni P 등 2012). 모유 유래 락토페린을 첨가한 분유는 일반 분유와 비교했을 때, 생후 1년 동안 호흡기 질환 발병률을 감소시켰다고 보고하였다(King JC Jr 등 2007; Han RH 등 2019). 또한 선행연구(Han RH 등 2019)에서는 모유 유래 재조합 락토페린은 박테리아, 곰팡이, 식물 및 동물벡터에서 성공적으로 발현되었고, 형질전환을 통해 상업적으로 락토페린의 대량 생산이 가능해지면서 다양한 형태의 락토페린이 임상에 적용되고 있다고 시사하였다.
세포와 신경세포의 손실로 인해 발생하는 신경퇴행성 질환에서 락토페린은 ROS의 생성을 줄임으로써 단백질 발현을 조절한다(Metz-Boutigue MH 등 1984; Li YQ & Guo C 2021). 알츠하이머병의 기본 메커니즘은 β-아밀로이드 전구체 단백질(APP)이 아밀로이드를 통해 상당한 수준의 신경독성 Aβ42를 생성하는데, 이때 TNF-α, IL-1β, IL-6 및 기타 염증 인자가 증가하면서 락토페린의 요구도가 증가한다(Tan MS 등 2014; Kaushal V 등 2015). “떨림 마비”라고도 알려진 파킨슨병(Parkinson’s disease; PD)은 발병률이 알츠하이머병보다 흔한 신경 퇴행성 질환이며, dysosmia, 수면 장애, 정동 장애, 자율 신경 기능 장애, 불안, 우울증 및 인지 장애, 운동 이상증의 시작 등의 신경 병리학적 특징이 보고되었다(Li YQ & Guo C 2021). 이러한 파킨슨병에서 말초혈액의 순환에 의해 락토페린은 수용체 매개를 통해 파킨스병에 관여하는 뇌 영역에 도달하여 민감한 뉴런을 보호하고, 신경보호 효과를 나타낸다(Wang J 등 2015). 프리온병(Prion diseases)은 퇴행성 신경질환인데, 락토페린의 투여는 PrP의 발생을 억제하며(Fillebeen C 등 2001), 뇌동맥경화증, 혈전증, 협착증과 같은 크고 작은 혈관 질환, 폐색, 뇌동맥염, 뇌동맥 손상, 뇌동맥류 등 두개골 내 혈관 기형 등의 다양한 뇌 질환은 락토페린 섭취로 인해 신경학적 결손, 관류 저하, 저산소증 및 신경염증의 억제될 수 있다고 보고하였다(Larsson SC 2017). 뇌출혈(cerebral hemorrhage; ICH) 질환의 경우 락토페린은 철 킬레이트제 및 항염증 인자로서 혈종을 해독하고, 뇌 조직 세포의 파괴를 완화하는 데 도움이 된다고 보고되었다(Table 4)(Zhao X 등 2017; Li YQ & Guo C 2021).
5) 락토페린과 암
많은 연구(Hu Z 등 2025)를 통해 락토페린이 종양의 증식, 침윤, 전이를 다양한 경로를 통해 억제한다는 사실이 밝혀지면서 종양 형성 및 종양 미세환경에 미치는 영향이 보고되고 있다(Table 5). 동물연구(Tsuda H 등 2004)에서 락토페린은 쥐의 결장암, 식도암, 폐암, 방광암을 억제하고, 결장 상피암 세포의 자멸을 유도하는 것으로 보고되었다. 또한 인체 연구(Arcella A 등 2015; Yan M 등 2022; Ramezani R 등 2023)에서 락토페린은 유방암, 간암, 비인두암, 위암, 신경교종, 두경부 편평세포암, 폐암, 대장암 및 백혈병과 같은 여러 유형의 암에서 광범위한 항종양 효과가 입증되었다. 인체 내 메커니즘 측면에서 락토페린은 세포 주기를 조절하여 종양 세포의 증식 억제, 종양 세포의 사멸 활성화, 종양의 혈관신생 억제, 종양 면역 환경 조절, 종양의 침습 및 이동 등을 억제할 수 있다고 보고되었다(Cutone A 등 2020). 위에서 제시한 연구를 바탕으로 다른 종양 치료에도 락토페린의 적용을 위한 추가 연구가 필요하다고 판단된다.
3. 락토페린의 생산 및 산업 발달에 응용
락토페린은 세균이나 바이러스에 대해 방어작용이 있으며, 감염 예방 및 치료의 관점에서 중요한 기능을 담당하고 있다(Ryu YK & Kim WS 2009). 락토페린 연구는 의학, 약학, 수의학 분야 및 식품 분야에서 다양하게 이루어지고 있으며, 임상시험도 꾸준히 이어지고 있다(Ryu YK & Kim WS 2009). 최근 유전공학기법을 활용하여 사람의 락토페린의 대량 생산은 인체 의료 분야까지 도움을 줄 수 있다고 보고하였으며(Yu DY 1997), 이에 암 환자에게 소의 락토페린을 장기 투여할 경우, 수개월 후에 몸속의 혈중 락토페린이 증가할 것이라는 보고도 있다(Ryu YK & Kim WS 2009). 선행연구(Lönnerdal B & Iyer S 1995)에서는 모유, 호중구, 그리고 소의 젖에서 락토페린의 완전한 cDNA를 보고하였고, 재조합 단백질도 생산되었다고 보고하였다. 또한 형질전환 동물(소)을 사용하여 임상시험을 위한 사람의 락토페린의 대량 생산이 가능해졌으며(Krimpenfort P 1993), 재조합 사람의 락토페린(Recombinant human lactoferrin)은 Saccharomyces (Liang Q & Richardson T 1993) 또는 Aspergillus(Ward PP 등 1992)와 같은 미생물을 사용하여 대량으로 생산될 수 있다고 보고하였다. 따라서 고품질의 원료를 가지고, 최적의 형태로 분리 및 정제하는 것이 락토페린의 품질과 안정성에 중요한 요소가 될 것으로 판단되며, 단백질의 양이나 순도 등을 고려한 락토페린 생산은 골다공증 예방, 면역기능 조절, 항균 및 항염증 질환 예방, 중추신경계 질환 예방, 암 예방 등의 인간의 건강 개선 및 나아가서는 재생 조직 생산에 있어서도 활용이 가능할 것으로 기대된다.
락토페린의 세계 시장 규모는 2022년에 2억 7,640만 달러였으며, 2023년 3억 45만 달러에서 2031년에는 5억 8,560만 달러로 성장하고, 예측 기간(2024∼2031년) 연평균 복합 성장률(CAGR)은 8.7%를 나타낼 것으로 전망하였다(Global informatiom 2024).
최근 산업 분야에서 락토페린은 기존의 항생물질에 비해 부작용이 적고, 안정성이 강하다는 장점을 가지고 있기 때문에, 유아용 조제분유, 건강보조식품 산업, 화장품 및 의약품 개발 등에서 활용이 증가하고 있다(Table 6). 동물 관련 선행연구 보고에 의하면, 양식어에 감염하는 백점충에 대한 예방효과(Sakai M 등 1993), 고양이 등의 반려동물의 구내염 치료제(Sato R 등 1996) 등으로도 이용되고 있다. 또한 소의 락토페린을 정제하여 조제분유 첨가제, 양식장에서 항생 보조제로 활용, 반려동물의 치료 보조제 등으로 개발되고 있다(Yu DY 1997). 식품 산업에서는 락토페린을 첨가한 저지방 세절소시지 개발(Kang IH 등 2008), 화장품 산업에서는 lactoferrin을 함유한 유산균 음료 섭취가 여드름 피부염 예방(Ko YJ 2008), 구강 및 maxillofacial 질환 예방(Velliyagounder K 등 2019), 항노화(Li B 등 2022) 등의 연구들이 대표적인 예이다. 의약품 분야에서 락토페린과 나노기술의 통합이라는 혁신적인 약물 개발 모델은 락토페린이 암 등의 치료 분야에서 활용 가능성을 시사한다(Rodrigues L 등 2009; Rascón-Cruz Q 등 2021; Hu Z 등 2025). 또한 락토페린은 혈액-뇌 장벽을 통과할 수 있어 뇌종양 치료를 포함한 화학요법제의 이상적인 운반체로 밝혀졌으며, 특히 병용 요법에서 암 예방 및 치료에 유망한 도구로 전 세계적으로 주목받고 있다(Cutone A 등 2020). 최근 락토페린에서 다양한 생명공학 및 의학적 해결책을 모색하고 있으며, 보철 및 임플란트 시술 시 감염 위험을 줄이는 요인으로 락토페린에 관한 연구가 진행되고 있다(Bukowska-Ośko I 등 2022). 또한 락토페린의 DNA 보호 효과가 보고되면서 유전 물질 손상으로 인한 여러 질병 과정에서 새로운 치료 가능성을 제시하고 있다(Bukowska-Ośko I 등 2022).
4. 락토페린 섭취 시 부작용 및 임상적 한계
위에서 언급한 것과 같이 동물과 인체 내에서 락토페린의 다양한 효능이 보고되었다. 그러나 락토페린을 지속적으로 과다 복용 시 소화장애, 복통, 설사, 두통 및 피로감 등을 야기시킬 수 있으며, 유제품 알레르기, 임산부 및 수유 중인 여성의 섭취 시 주의가 필요하다. 또한 락토페린은 유제품에서 추출되므로 원료의 품질에 따라 효능이 달라질 수 있으므로 순도가 높은 제품을 선택하는 것이 중요하다. 인체 내 대사질환과 관련된 락토페린의 임상 연구에서는 락토페린의 효능과 안정성 및 일부 락토페린의 기능성을 입증(Miyakawa M 등 2023)하기 위해 추가적인 연구의 검증이 필요하다고 사료된다.
요약 및 결론
본 연구는 최근 락토페린과 건강에 대한 상관관계가 높다고 보고되어 이에 관련된 연구내용을 정리 및 고찰하였다. MBP에 함유된 락토페린은 식품에서 유래했기 때문에 부작용이 적고 안정성이 높아서 다른 화학 약품에 비해 장점이 크다. 또한 연구에 있어서도 연구기간, 피험자의 임상 및 재정적 위험을 최소화할 수 있다. 락토페린은 주로 초유에 많이 함유되어 있다. 락토페린은 골다공증 예방, 면역기능 조절, 항균 및 항염증 질환 예방, 중추신경계 질환 예방, 암 예방 등에 영향을 준다. 그러나 락토페린 과량 복용 시 복통, 설사, 두통 등이 발생함으로 전문가와 상의 후에 적절한 양을 섭취하는 것도 중요한 요소이다.
최근 락토페린은 건강기능성 식품으로 영양 보충제, 유아용 조제분유, 화장품 및 치약과 같은 상용 제품에 사용되고 있으며, 앞으로 의학 분야에서도 락토페린의 활용 가치는 증가할 것으로 사료된다. 또한 재조합 락토페린의 합성, 정제 및 대규모 생산을 통해 락토페린의 동물실험 및 임상 연구를 가속화 할 필요성이 있다고 판단된다.
REFERENCES
-
Anderson BF, Baker HM, Dodson EJ, Norris GE, Rumball SV, Waters JM, Baker EN (1987) Structure of human lactoferrin at 3.2-A resolution. Proc Natl Acad Sci USA 84(7): 1769-1773.
[https://doi.org/10.1073/pnas.84.7.1769]

-
Anderson BF, Baker HM, Norris GE, Rice DW, Baker EN (1989) Structure of human lactoferrin: crystallographic structure analysis and refinement at 2.8 A resolution. J Mol Biol 209(4): 711-734.
[https://doi.org/10.1016/0022-2836(89)90602-5]

-
Appelmelk BJ, An YQ, Geerts M, Thijs BG, de Boer HA, MacLaren DM, de Graaff J, Nuijens JH (1994) Lactoferrin is a lipid A-binding protein. Infect Immun 62(6): 2628-2632.
[https://doi.org/10.1128/iai.62.6.2628-2632.1994]

-
Arcella A, Oliva MA, Staffieri S, Aalberti S, Grillea G, Madonna M, Bartolo M, Pavone L, Giangaspero F, Cantore G, Frati A (2015) In vitro and in vivo effect of human lactoferrin on glioblastoma growth. J Neurosurg 123(4): 1026-1035.
[https://doi.org/10.3171/2014.12.JNS14512]

-
Arnold RR, Russell JE, Champion WJ, Brewer M, Gauthier JJ (1982) Bactericidal activity of human lactoferrin: differentiation from the stasis of iron deprivation. Infect Immun 35(3): 792-799.
[https://doi.org/10.1128/iai.35.3.792-799.1982]

-
Berlutti F, Pantanella F, Natalizi T, Frioni A, Paesano R, Polimeni A, Valenti P (2011) Antiviral properties of lactoferrin: a natural immunity molecule. Molecules 16(8): 6992-7018.
[https://doi.org/10.3390/molecules16086992]

-
Berthon BS, Williams LM, Williams EJ, Wood LG (2022) Effect of lactoferrin supplementation on inflammation, immune function, and prevention of respiratory tract infections in humans: a systematic review and meta-analysis. Adv Nutr 13(5): 1799-1819.
[https://doi.org/10.1093/advances/nmac047]

-
Brock JH (2012) Lactoferrin--50 years on. Biochem Cell Biol 90(3): 245-251.
[https://doi.org/10.1139/o2012-018]

-
Bukowska-Ośko I, Sulejczak D, Kaczyńska K, Kleczkowska P, Kramkowski K, Popiel M, Wietrak E, Kowalczyk P (2022) Lactoferrin as a human genome “Guardian”- an overall point of view. Int J Mol Sci 23(9): 5248.
[https://doi.org/10.3390/ijms23095248]

-
Chen R, Ding J, Li Y, Zhang Y, Yang R (2024) Lactoferrin-based heteroprotein systems, from their formation mechanism, properties, to applications. J Agric Food Chem 72(40): 21986-22000.
[https://doi.org/10.1021/acs.jafc.4c05298]

-
Choe YH, Lee SW (1999) Effect of lactoferrin on the production of tumor necrosis factor-alpha and nitric oxide. J Cell Biochem 76(1): 30-36.
[https://doi.org/10.1002/(SICI)1097-4644(20000101)76:1<30::AID-JCB4>3.3.CO;2-L]

-
Cutone A, Rosa L, Laniro G, Lepanto MS, Bonaccorsi di Patti MC, Valenti P, Musci G (2020) Lactoferrin’s anti-cancer properties: safety, selectivity, and wide range of action. Biomolecules 10(3): 456.
[https://doi.org/10.3390/biom10030456]

-
Digumarti R, Wang Y, Raman G, Doval DC, Advani SH, Julka PK, Parikh PM, Patil S, Nag S, Madhavan J, Bapna A, Ranade AA, Varadhachary A, Malik R (2011) A randomized, double-blind, placebo-controlled, phase II study of oral talactoferrin in combination with carboplatin and paclitaxel in previously untreated locally advanced or metastatic non-small cell lung cancer. J Thorac Oncol 6(6): 1098-1103.
[https://doi.org/10.1097/JTO.0b013e3182156250]

-
Edde L, Hipolito RB, Hwang FF, Headon DR, Shalwitz RA, Sherman MP (2001) Lactoferrin protects neonatal rats from gut-related systemic infection. Am J Physiol Gastrointest Liver Physiol 281(5): G1140-G1150.
[https://doi.org/10.1152/ajpgi.2001.281.5.G1140]

-
Fillebeen C, Ruchoux MM, Mitchell V, Vincent S, Benaïssa M, Pierce A (2001) Lactoferrin is synthesized by activated microglia in the human substantia nigra and its synthesis by the human microglial CHME cell line is upregulated by tumor necrosis factor alpha or 1-methyl-4-phenylpyridinium treatment. Brain Res Mol Brain Res 96(1-2): 103-113.
[https://doi.org/10.1016/S0169-328X(01)00216-9]

- Global informatiom (2024) Lactoferrin market size, share, growth analysis, by function (iron absorption, antiinflammatory), by application (food products, infant formula), by region-industry forecast 2024-2031 (2024). https://www.giiresearch.com, (accessed on 24. 11. 2024).
-
González-Chávez SA, Arévalo-Gallegos S, Rascón-Cruz Q (2009) Lactoferrin: structure, function and applications. Int J Antimicrob Agents 33(4): 301.e1-301.e8.
[https://doi.org/10.1016/j.ijantimicag.2008.07.020]

-
Han RH, Yoon SH, Kim GB (2019) Clinical applications of bioactive milk components: a review. J Dairy Sci Biotechnol 37(3): 167-176.
[https://doi.org/10.22424/jmsb.2019.37.3.167]

-
Hirai Y, Kawakata N, Satoh K, Ikeda Y, Hisayasu S, Orimo H, Yoshino Y (1990) Concentrations of lactoferrin and iron in human milk at different stages of lactation. J Nutr Sci Vitaminol 36(6): 531-544.
[https://doi.org/10.3177/jnsv.36.531]

-
Hu WL, Mazurier J, Sawatzki G, Montreuil J, Spik G (1988) Lactotransferrin receptor of mouse small-intestinal brush border. Binding characteristics of membrane-bound and triton X-100-solubilized forms. Biochem J 249(2): 435-441.
[https://doi.org/10.1042/bj2490435]

-
Hu Z, Li W, Wei L, Ma J (2025) Lactoferrin in cancer: Focus on mechanisms and translational medicine. Biochim Biophys Acta Rev Cancer 1880(3): 189330.
[https://doi.org/10.1016/j.bbcan.2025.189330]

-
Inoue Y, Asai Y, Tomita M, Kuribara K, Kobayashi M, Kaneko M, Toba Y (2006) The effect of milk basic protein supplementation on bone metabolism during training of young thoroughbred racehorses. Equine Vet J Suppl 36: 654-658.
[https://doi.org/10.1111/j.2042-3306.2006.tb05621.x]

-
Ishida Y, Chacrabati R, Ono-Ohmachi A, Gong Z, Ikenoya C, Aizawa S, Nara TY, Morita Y, Kato K, Sakai T, Sakata I (2017) Milk basic protein increases ghrelin secretion and bone mineral density in rodents. Nutrition 39-40: 15-19.
[https://doi.org/10.1016/j.nut.2017.02.003]

- Iyer S, Lönnerdal B (1993) Lactoferrin, lactoferrin receptors and iron metabolism. Eur J Clin Nutr 47(4): 232-241.
-
Johanson B (1960) Isolation of an iron-containing red protein from human milk. Acta Chem Scand 14(2): 510-512.
[https://doi.org/10.3891/acta.chem.scand.14-0510]

-
Kang IH, Lee HC, Chin KB (2008) Physicochemical and textural properties, and shelf-life effects of low-fat sausages manufactured with various levels of activated lactoferrin during refrigerated storage. Korean J Food Sci Ani Resour 28(4): 408-414.
[https://doi.org/10.5851/kosfa.2008.28.4.408]

-
Karav S, German JB, Rouquié C, Le Parc A, Barile D (2017) Studying lactoferrin N-glycosylation. Int J Mol Sci 18(4): 870.
[https://doi.org/10.3390/ijms18040870]

-
Kaushal V, Dye R, Pakavathkumar P, Foveau B, Flores J, Hyman B, Ghetti B, Koller BH, LeBlanc AC (2015) Neuronal NLRP1 inflammasome activation of Caspase-1 coordinately regulates inflammatory interleukin-1-beta production and axonal degeneration-associated Caspase-6 activation. Cell Death Differ 22(10): 1676-1686.
[https://doi.org/10.1038/cdd.2015.16]

- Kim SH (2012) Physiological function and change of lactoferrin in colostrum. MS Thesis Hankyong National University, Anseong-si. pp 3-4.
-
King JC Jr, Cummings GE, Guo N, Trivedi L, Readmond BX, Keane V, Feigelman S, de Waard R (2007) A double-blind, placebo-controlled, pilot study of bovine lactoferrin supplementation in bottle-fed infants. J Pediatr Gastroenterol Nutr 44(2): 245-251.
[https://doi.org/10.1097/01.mpg.0000243435.54958.68]

- Ko YJ (2008) Dietary effect of lactoferrin, on the skin surface lipids of Korean adolescence with Acne vulgaris. MS Thesis Kyunghee University, Seoul. pp 1-56.
-
Kovacic B, Hoelbl-Kovacic A, Fischhuber KM, Leitner NR, Gotthardt D, Casanova E, Sexl V, Müller M (2014) Lactotransferrin-Cre reporter mice trace neutrophils, monocytes/macrophages and distinct subtypes of dendritic cells. Haematologica 99(6): 1006-1015.
[https://doi.org/10.3324/haematol.2013.097154]

-
Kowalczyk P, Kaczyńska K, Kleczkowska P, Bukowska-Ośko I, Kramkowski K, Sulejczak D (2022) The lactoferrin phenomenon-a miracle molecule. Molecules 27(9): 2941.
[https://doi.org/10.3390/molecules27092941]

-
Kozu T, Iinuma G, Ohashi Y, Saito Y, Akasu T, Saito D, Alexander DB, Iigo M, Kakizoe T, Tsuda H (2009) Effect of orally administered bovine lactoferrin on the growth of adenomatous colorectal polyps in a randomized, placebo-controlled clinical trial. Cancer Prev Res 2(11): 975-983.
[https://doi.org/10.1158/1940-6207.CAPR-08-0208]

- Krimpenfort P (1993) The production of human lactoferrin in the milk of transgenic animals. Cancer Detect Prev 17(2): 301-305.
-
Kruger CL, Marano KM, Morita Y, Takada Y, Kawakami H, Kobayashi T, Sunaga M, Furukawa M, Kawamura K (2007) Safety evaluation of a milk basic protein fraction. Food Chem Toxicol 45(7): 1301-1307.
[https://doi.org/10.1016/j.fct.2007.01.017]

- Kumegawa M (2006) Prevention of osteoporosis by foods and dietary supplements. Bone reinforcement factor in milk: Milk basic protein (MBP). Clin Calcium 16(10): 1624-1631.
-
Larsson SC (2017) Dietary approaches for stroke prevention. Stroke 48(10): 2905-2911.
[https://doi.org/10.1161/STROKEAHA.117.017383]

- Levay PF, Viljoen M (1995) Lactoferrin: a general review. Haematologica 80(3): 252-267.
-
Leveugle B, Mazurier J, Legrand D, Mazurier C, Montreuil J, Spik G (1993) Lactotransferrin binding to its platelet receptor inhibits platelet aggregation. Eur J Biochem 213(3): 1205-1211.
[https://doi.org/10.1111/j.1432-1033.1993.tb17871.x]

-
Li B, Zhang B, Liu X, Zheng Y, Han K, Liu H, Wu C, Li J, Fan S, Peng W, Zhang F, Liu X (2022) The effect of lactoferrin in aging: role and potential. Food Funct 13(2): 501-513.
[https://doi.org/10.1039/D1FO02750F]

-
Li NC, Iannuzo N, Christenson SA, Langlais PR, Kraft M, Ledford JG, Li X (2024) Investigation of lactotransferrin messenger RNA expression levels as an anti-type 2 asthma biomarker. J Allergy Clin Immunol 154(3): 609-618.
[https://doi.org/10.1016/j.jaci.2024.05.013]

-
Li YQ, Guo C (2021) A review on lactoferrin and central nervous system diseases. Cells 10(7): 1810.
[https://doi.org/10.3390/cells10071810]

-
Liang Q, Richardson T (1993) Expression and characterization of human lactoferrin in yeast Saccharomyces cerevisiae. J Agric Food Chem 41(10): 1800-1807.
[https://doi.org/10.1021/jf00034a053]

-
Lönnerdal B, Iyer S (1995) Lactoferrin: molecular structure and biological function. Annu Rev Nutr 15: 93-110.
[https://doi.org/10.1146/annurev.nu.15.070195.000521]

-
Manzoni P, Stolfi I, Messner H, Cattani S, Laforgia N, Romeo MG, Bollani L, Rinaldi M, Gallo E, Quercia M, Maule M, Mostert M, Decembrino L, Magaldi R, Mosca F, Vagnarelli F, Memo L, Betta PM, Stronati M, Farina D (2012) Bovine lactoferrin prevents invasive fungal infections in very low birth weight infants: a randomized controlled trial. Pediatrics 129(1): 116-123.
[https://doi.org/10.1542/peds.2011-0279]

-
Metz-Boutigue MH, Jollès J, Mazurier J, Schoentgen F, Legrand D, Spik G, Montreuil J, Jollès P (1984) Human lactotransferrin: amino acid sequence and structural comparisons with other transferrins. Eur J Biochem 145(3): 659-676.
[https://doi.org/10.1111/j.1432-1033.1984.tb08607.x]

-
Miyakawa M, Oda H, Tanaka M (2023) Clinical research review: usefulness of bovine lactoferrin in child health. Biometals 36(3): 473-489.
[https://doi.org/10.1007/s10534-022-00430-4]

-
Nakatani S, Taguchi Y, Ueda H, Ishida Y, Morita Y, Kato K, Wada M, Kobata K (2019) Short communication: milk basic protein promotes proliferation and inhibits differentiation of mouse chondrogenic ATDC5 cells. J Dairy Sci 102(4): 2873-2878.
[https://doi.org/10.3168/jds.2018-15656]

-
Nishiya K, Horwitz DA (1982) Contrasting effects of lactoferrin on human lymphocyte and monocyte natural killer activity and antibody-dependent cell-mediated cytotoxicity. J Immunol 129(6): 2519-2523.
[https://doi.org/10.4049/jimmunol.129.6.2519]

-
Nuijens JH, van Berkel PH, Schanbacher FL (1996) Structure and biological actions of lactoferrin. J Mammary Gland Biol Neoplasia 1(3): 285-295.
[https://doi.org/10.1007/BF02018081]

-
Ono-Ohmachi A, Ishida Y, Morita Y, Kato K, Y Nara T (2017) Milk basic protein facilitates increased bone mass in growing mice. J Nutr Sci Vitaminol 63(5): 315-322.
[https://doi.org/10.3177/jnsv.63.315]

-
Ono-Ohmachi A, Nakajima-Adachi H, Morita Y, Kato K, Hachimura S (2018) Milk basic protein supplementation exerts an anti-inflammatory effect in a food-allergic enteropathy model mouse. J Dairy Sci 101(3): 1852-1863.
[https://doi.org/10.3168/jds.2017-13253]

-
Park HS, Kim HJ (2015) Effect of lactoferrin on tooth development in rats. Korean J Oral Anatomy 36(1): 37-43.
[https://doi.org/10.35607/kjoa.36.1.201512.005]

-
Penco S, Pastorino S, Bianchi-Scarrà G, Garrè C (1995) Lactoferrin down-modulates the activity of the granulocyte macrophage colony-stimulating factor promoter in interleukin-1 beta-stimulated cells. J Biol Chem 270(20): 12263-12268.
[https://doi.org/10.1074/jbc.270.20.12263]

-
Piacentini R, Boffi A, Milanetti E (2024) Lactoferrins in their interactions with molecular targets: a structure-based overview. Pharmaceuticals 17(3): 398.
[https://doi.org/10.3390/ph17030398]

-
Rado TA, Wei X, Benz EJ (1987) Isolation of lactoferrin cDNA from a human myeloid library and expression of mRNA during normal and leukemic myelopoiesis. Blood 70(4): 989-993.
[https://doi.org/10.1182/blood.V70.4.989.989]

-
Ramezani R, Mohammadian M, Hosseini ES, Zare M (2023) The effect of bovine milk lactoferrin-loaded exosomes (exoLF) on human MDA-MB-231 breast cancer cell line. BMC Complement Med Ther 23(1): 228.
[https://doi.org/10.1186/s12906-023-04045-1]

-
Rascón-Cruz Q, Espinoza-Sánchez EA, Siqueiros-Cendón TS, Nakamura-Bencomo SI, Arévalo-Gallegos S, Iglesias-Figueroa BF (2021) Lactoferrin: a glycoprotein involved in immunomodulation, anticancer, and antimicrobial processes. Molecules 26(1): 205.
[https://doi.org/10.3390/molecules26010205]

-
Rodrigues L, Teixeira J, Schmitt F, Paulsson M, Månsson HL (2009) Lactoferrin and cancer disease prevention. Crit Rev Food Sci Nutr 49(3): 203-217.
[https://doi.org/10.1080/10408390701856157]

- Ryu YK, Kim WS (2009) Current trends in lactoferrin research and development. J Dairy Sci Technol 27(1): 19-28.
-
Sakai M, Otubo T, Atsuta S, Kobayashi M (1993) Enhancement of resistance of bacteria infection in rainbow trout, Oncorhynchus mykiss (Walbaum), by oral administration of bovine lactoferrin. J Fish Dis 16(3): 239-247.
[https://doi.org/10.1111/j.1365-2761.1993.tb01253.x]

-
Sato R, Inanami O, Tanaka Y, Takase M, Naito Y (1996) Oral administration of bovine lactoferrin for treatment of intractable stomatitis in feline immunodeficiency virus (FIV)-positive and FIV-negative cats. Am J Vet Res 57(10): 1443-1446.
[https://doi.org/10.2460/ajvr.1996.57.10.1443]

-
Seto H, Toba Y, Takada Y, Kawakami H, Ohba H, Hama H, Horibe M, Nagata T (2007) Milk basic protein increases alveolar bone formation in rat experimental periodontitis. J Periodontal Res 42(1): 85-89.
[https://doi.org/10.1111/j.1600-0765.2006.00919.x]

-
Shimazaki K (2000) Lactoferrin: a marvelous protein in milk. Anim Sci J 71(4): 329-347.
[https://doi.org/10.2508/chikusan.71.329]

-
Shin MY, Kwun IS (2016) Vitamin D: hormone-like nutrient. J Nutr Health 49(1): 1-7.
[https://doi.org/10.4163/jnh.2016.49.1.1]

-
Singh J, Sharma M, Jain N, Aftab I, Vikram N, Singh TP, Sharma P, Sharma S (2022) Lactoferrin and its nano-formulations in rare eye diseases. Indian J Ophthalmol 70(7): 2328-2334.
[https://doi.org/10.4103/ijo.IJO_303_22]

-
Slater K, Fletcher J (1987) Lactoferrin derived from neutrophils inhibits the mixed lymphocyte reaction. Blood 69(5): 1328-1333.
[https://doi.org/10.1182/blood.V69.5.1328.1328]

- Sorensen M, Sorensen SPL (1939) The Proteins in Whey. Hagerup in Komm. pp 55-99.
-
Sorimachi K, Akimoto K, Hattori Y, Ieiri T, Niwa A (1997) Activation of macrophages by lactoferrin: secretion of TNF-alpha, IL-8 and NO. Biochem Mol Biol Int 43(1): 79-87.
[https://doi.org/10.1080/15216549700203841]

-
Steijns JM (2001) Milk ingredients as nutraceuticals. Int J Dairy Technol 54(3): 81-88.
[https://doi.org/10.1046/j.1364-727x.2001.00019.x]

-
Sun X, Jiang R, Przepiorski A, Reddy S, Palmano KP, Krissansen GW (2012) “Iron-saturated” bovine lactoferrin improves the chemotherapeutic effects of tamoxifen in the treatment of basal-like breast cancer in mice. BMC Cancer 12: 591.
[https://doi.org/10.1186/1471-2407-12-591]

-
Tan MS, Tan L, Jiang T, Zhu XC, Wang HF, Jia CD, Yu JT (2014) Amyloid-β induces NLRP1-dependent neuronal pyroptosis in models of Alzheimer’s disease. Cell Death Dis 5(8): e1382.
[https://doi.org/10.1038/cddis.2014.348]

-
Toba Y, Takada Y, Matsuoka Y, Morita Y, Motouri M, Hirai T, Suguri T, Aoe S, Kawakami H, Kumegawa M, Takeuchi A, Itabashi A (2001) Milk basic protein promotes bone formation and suppresses bone resorption in healthy adult men. Biosci Biotechnol Biochem 65(6): 1353-1357.
[https://doi.org/10.1271/bbb.65.1353]

-
Toba Y, Takada Y, Yamamura J, Tanaka M, Matsuoka Y, Kawakami H, Itabashi A, Aoe S, Kumegawa M (2000) Milk basic protein: a novel protective function of milk against osteoporosis. Bone 27(3): 403-408.
[https://doi.org/10.1016/S8756-3282(00)00332-X]

-
Tomita M, Takase M, Wakabayashi H, Bellamy W (1994) Antimicrobial peptides of lactoferrin. Adv Exp Med Biol 357: 209-218.
[https://doi.org/10.1007/978-1-4615-2548-6_20]

-
Tsuda H, Ohshima Y, Nomoto H, Fujita K, Matsuda E, Iigo M, Takasuka N, Moore MA (2004) Cancer prevention by natural compounds. Drug Metab Pharmacokinet 19(4): 245-263.
[https://doi.org/10.2133/dmpk.19.245]

-
Tung YT, Chen HL, Yen CC, Lee PY, Tsai HC, Lin MF, Chen CM (2013) Bovine lactoferrin inhibits lung cancer growth through suppression of both inflammation and expression of vascular endothelial growth factor. J Dairy Sci 96(4): 2095-2106.
[https://doi.org/10.3168/jds.2012-6153]

-
Uenishi K, Ishida H, Toba Y, Aoe S, Itabashi A, Takada Y (2007) Milk basic protein increases bone mineral density and improves bone metabolism in healthy young women. Osteoporosis Int 18(3): 385-390.
[https://doi.org/10.1007/s00198-006-0228-5]

-
Velliyagounder K, Bahdila D, Pawar S, Fine DH (2019) Role of lactoferrin and lactoferrin-derived peptides in oral and maxillofacial diseases. Oral Dis 25(3): 652-669.
[https://doi.org/10.1111/odi.12868]

-
Wang B, Timilsena YP, Blanch E, Adhikari B (2019) Lactoferrin: structure, function, denaturation and digestion. Crit Rev Food Sci Nutr 59(4): 580-596.
[https://doi.org/10.1080/10408398.2017.1381583]

-
Wang J, Bi M, Liu H, Song N, Xie J (2015) The protective effect of lactoferrin on ventral mesencephalon neurons against MPP+ is not connected with its iron binding ability. Sci Rep 5: 10729.
[https://doi.org/10.1038/srep10729]

-
Wang Y, Liu Y, Liu J, Kang R, Tang D (2020) NEDD4L-mediated LTF protein degradation limits ferroptosis. Biochem Biophys Res Commun 531(4): 581-587.
[https://doi.org/10.1016/j.bbrc.2020.07.032]

-
Ward PP, May GS, Headon DR, Conneely OM (1992) An inducible expression system for the production of human lactofenin in Aspergillus nidulans. Gene 122(1): 219-223.
[https://doi.org/10.1016/0378-1119(92)90054-S]

-
Yan M, Rodgers M, Harbhajanka A, Gilmore H (2022) Lactotransferrin-related breast amyloidosis: report of a first case. Int J Surg Pathol 30(1): 50-54.
[https://doi.org/10.1177/10668969211016053]

-
Yasueda T, Abe Y, Shiba M, Kamo Y, Seto Y (2018) A new insight into cystatin C contained in milk basic protein to bone metabolism: effects on osteoclasts and osteoblastic MC3T3-E1 cells in vitro. Anim Sci J 89(7): 1027-1032.
[https://doi.org/10.1111/asj.13005]

-
Yoneme H, Hatakeyama J, Danjo A, Oida H, Yoshinari M, Aijima R, Murata N, Watanabe T, Oki Y, Kido MA (2015) Milk basic protein supplementation enhances fracture healing in mice. Nutrition 31(2): 399-405.
[https://doi.org/10.1016/j.nut.2014.08.008]

- Yu DY (1997) Studied on the structure, function and production of lactoferrin. Korean Dairy Techno 15(2): 83-89.
-
Zhao X, Ting SM, Liu CH, Sun G, Kruzel M, Roy-O’Reilly M, Aronowski J (2017) Neutrophil polarization by IL-27 as a therapeutic target for intracerebral hemorrhage. Nat Commun 8(1): 602.
[https://doi.org/10.1038/s41467-017-00770-7]

