인삼꽃 주정 추출물의 항산화 활성 및 HepG2 세포를 대상으로 한 산화적 스트레스 억제 효과
Abstract
Ginsenosides, the bioactive compounds found in Panax ginseng, are distributed throughout all the parts of the plant. However, during the harvesting process, the flowers are typically removed to prioritize root growth and subsequently remain underutilized. This study sought to investigate the potential applications of Panax ginseng flowers by assessing their antioxidant activity and inhibitory effects on oxidative stress. Ethanolic extracts of Panax ginseng flowers were prepared, and their bioactive properties were comprehensively evaluated. These extracts were found to have a total phenolic and flavonoid content of 32.24±2.54 mg/g and 6.46±0.82 mg/g, respectively. Antioxidant activity assays demonstrated a significant concentration-dependent enhancement in 2,2-diphenyl-1-picrylhydrazyl (DPPH) 2,2-Azino-bis-3-ethylbenzothiazoline-6-sulfonic acid (ABTS) radical scavenging activities. Specifically, the DPPH radical scavenging activity reached 62.23±1.84% at a concentration of 5 mg/mL, while the ABTS radical scavenging activity was 79.44±0.54% at 1 mg/mL concentration. The extract’s reducing power was measured as 2.105±0.017 at 5 mg/mL, and the ferric reducing antioxidant power (FRAP) assay yielded an absorbance of 1.051±0.026 at the same concentration. Cytotoxicity assessments conducted on HepG2 cells indicated that the Panax ginseng flower ethanolic extracts exhibited low cytotoxicity, maintaining over 95% cell viability at concentrations up to 12.5 μg/mL. Furthermore, when oxidative stress was induced in the HepG2 cells using sodium nitroprusside (SNP), treatment with the extract significantly improved cell viability. At a concentration of 10 μg/mL, the extract restored cell viability to 56.78±2.58%, representing a 32% increase compared to the SNP-treated cells without the extract (p<0.05). These results highlight the significant antioxidant and cytoprotective properties of the ethanolic extracts of the Panax ginseng flower. Thus, Panax ginseng flowers, which are currently an underutilized part of the plant, have the potential to serve as a valuable source of bioactive compounds for the development of therapeutic agents aimed at mitigating oxidative stress-related diseases.
Keywords:
Panax ginseng, ginseng flower, antioxidants, oxidative stress, HepG2서 론
인삼(Panax ginseng C. A. Meyer)은 한의학에서는 뿌리만을 약재로 사용해 왔고 식품업계에서도 뿌리를 추출하여 농축액이나 파우치 형태로 제품화하고 있다. 인삼은 항비만 효과(Kim HR 등 2019), 항산화 활성(Kim YC 등 2007), 항암 활성(Kim HY 등 2010), 주름개선 효과(Kim MJ 등 2012), 면역 활성(Sung JH 등 2004)이 있는 것으로 알려져 있다. 이는 인삼 뿌리 추출물에 관한 효능 연구가 대부분을 차지하고 있고 인삼의 꽃이나 잎에 관한 연구는 이루어지고 있지 않다. 또한 식품에 사용할 수 있는 인삼 부위는 뿌리, 줄기(수경재배), 잎, 열매, 씨앗으로 되어 있고 인삼꽃은 식품으로 사용할 수 있는 원료로 되어 있지 않아서 인삼꽃의 연구는 미비한 것으로 판단된다. 그러나 인삼의 대표적인 생리활성 물질인 ginsenoside는 인삼의 전체 부위에 다양하게 분포하고 있고 그 종류도 많아서 염증, 암 및 심혈관계 질환 등을 포함한 여러 질병에 대해 다양한 약리작용을 하는 것으로 보고되었다(Xue Q 등 2021).
인삼꽃의 ginsenoside 분석에 관한 연구로는 Wu W 등(2016)은 인삼 꽃봉우리에서 14종의 ginsenoside와 5종의 malonyl ginsenoside를 분석하였고, Choi JE 등(2009)은 인삼꽃에 ginsenoside Rb2, Rc, Rd, Re, Rg1 및 총 ginsenoside가 많고 특히 Re의 함량은 채취시기와 관계없이 많이 함유되어 있다고 보고하였다. 또한 Kang MW 등(2020)은 ginsenoside Rg1, Rb1 및 Rg3의 합은 인삼꽃 에탄올 추출물에서 35.95 mg/g으로 백삼과 백미삼에 비해 높게 함유되어 있었고, 활성 사포닌으로 알려진 ginsenoside Rg3 및 CK(compound K)의 함량에서도 인삼꽃 에탄올 추출물이 10.50 mg/g으로 가장 높은 함량이라고 보고하였다. Cho SH(1977)은 인삼의 부산물인 인삼의 꽃과 세근에는 뿌리보다 많은 ginsenoside가 함유되어 있다고 하였다. 인삼꽃의 기능성에 관한 연구로 Kim HS & Ko KS(2021)은 인삼꽃 에탄올 추출물이 피부의 항산화 활성(DPPH), 세포독성(MTT assay), 항염효능(NO assay), 세포 재생 효능이 있어 피부노화 억제 효과가 있다고 보고하였고, Kim KH 등(2013)은 Bacillus subtilis를 이용하여 인삼꽃 발효물을 제조하는 것이 항산화 활성이 증가한다고 보고하였다.
인삼을 수확하는 과정에서 4년 이상의 인삼은 뿌리의 생장을 돕기 위해 꽃을 제거하고 있으며 거의 활용하지 못하고 있는 실정이다. 많은 연구에서 인삼꽃도 인삼과 마찬가지로 사포닌을 함유하고 있다고 보고하였다. 따라서 본 연구에서는 인삼꽃 주정 추출물을 제조하고 항산화효능과 세포보호 효과를 조사하여 향후 인삼꽃의 활용 가능성을 모색하고자 하였다.
재료 및 방법
1. 실험재료 및 주정 추출물 제조
본 연구의 재료로 이용한 인삼꽃은 강원도 원주 소재의 대형마트에서 구입하였고 깨끗이 손질하여 동결 건조한 후 실험에 사용하였다. 주정 추출조건은 50% 주정과 재료를 1:1로 하여 90℃에서 6 hr 환류 냉각 추출방법으로 추출하였다. 인삼꽃 주정 추출물은 여과지(Whatmman No 41, Whatmman International Ltd., Maid stone, UK)로 이물질을 제거한 후 농축기(EYELA N-N series, Tokyo Rikakikai Co., Tokyo, Japan)로 농축하여 동결건조 후 냉동(—20℃) 보관하여 실험에 이용하였다.
2. 총 페놀 함량 측정
인삼꽃 주정 추출물의 총 페놀화합물의 함량은 Folin-Denis법(Folin O & Denis W 1915)을 응용하여 측정하였다. 인삼꽃 주정 추출물을 증류수로 희석한 추출물 0.2 mL을 시험관에 넣고 증류수를 1.8 mL와 Folin 시약 0.2 mL를 첨가하여 혼합한 다음 실온에서 3 min 방치하였다. 그리고 10% Na2CO3 포화용액 0.4 mL와 증류수 1.4 mL을 가하여 혼합하고 실온에서 1 hr 반응시킨 후 분광광도계(X-ma 3100, Human Corporation, Seoul, Korea) 725 nm에서 흡광도를 측정하였다. 표준물질은 caffeic acid을 0∼100 μg/mL의 농도로 제조하여 시료와 동일한 방법으로 분석하였으며, 표준검량곡선으로부터 인삼꽃 주정 추출물의 총 페놀 함량을 계산하였다.
3. 총 플라보노이드 함량 측정
인삼꽃 주정 추출물의 총 플라보노이드 함량은 Moreno (Moreno MIN 등 2000)의 방법으로 시료 0.5 mL에 10% aluminum nitrate 0.1 mL, 1 M potassium acetate 0.1 mL 및 80% ethanol 4.3 mL를 차례로 혼합하고 실온에서 40 min 방치한 다음 분광광도계(X-ma 3100, Human Corporation, Seoul, Korea) 415 nm에서 흡광도를 측정하였다. 표준물질은 quercetin을 0∼100 μg/mL의 농도로 제조하여 시료와 동일한 방법으로 분석하였으며, 표준검량곡선으로부터 인삼꽃 주정 추출물의 총 플라보노이드 함량을 계산하였다.
4. DPPH(2,2-Diphenyl-1-picrylhydrazyl) Radical 소거활성 측정
DPPH radical 소거활성은 Blois MS(1958)의 방법에 의하여 측정하였다. 즉, 시료 희석액 0.4 mL에 0.1 mM DPPH 용액 5.6 mL를 첨가한 후, 10 min 방치한 후 분광광도계(X-ma 3100, Human Corporation, Seoul, Korea) 525 nm에서 흡광도를 측정하였다. DPPH 라디칼 소거능은 시료 무 첨가구에 대한 첨가구의 흡광도 비로 나타내었다.
5. ABTS(2,2-azino-bis-(3-ethylbenzothiazoline-6-sulfonic acid)) Radical 소거활성 측정
ABTS radical 소거활성 측정은 Re R 등(1999) 방법에 따라 7.4 mM ABTS 용액에 2.6 mM potassium persulfate를 넣고 암실에서 12∼16 hr 동안 반응시킨 다음 ABTS+ 이온을 형성시킨 후 이 용액을 734 nm에서 흡광도 값이 0.7이 되도록 증류수로 희석하였다. 희석된 ABTS 용액 1 mL에 시료 500 μL를 가하여 실온에서 10 min 반응시켜 흡광도를 측정하였다. ABTS 라디칼 소거능은 시료 첨가구와 무첨가구의 흡광도 비로 나타내었다.
6. 환원력 측정
인삼꽃 주정 추출물의 환원력 측정은 Oyaizu M 등(1986)의 방법으로 측정하였다. 즉, 농도별 시료 1 mL에 인산 완충액(200 mM, pH 6.6)과 1% potassium ferricyanide를 1 mL씩 차례로 혼합한 후 50℃에서 20 min 반응시켰다. 10% trichloroacetic acid(TCA)를 1 mL를 가하고 2,000 rpm에서 20 min 원심분리하여 얻은 상징액 2 mL에 증류수 1 mL와 0.1% ferric chloride 1 mL를 혼합한 후 700 nm에서 흡광도를 측정하였다.
7. FRAP(Ferric-Reducing Antioxidant Power)에 의한 항산화능 측정
FRAP 활성은 Benzie IFF & Strain JJ(1996)에 의한 방법에 따라 측정하였다. FRAP 시약은 acetate buffer(pH 3.6), 40 mM HCl에 용해시킨 10 mM 2,4,6-tripyridyl-s-triazine(TPTZ), 증류수로 용해시킨 20 mM FeCl3·6H2O를 10 : 1 : 1(v/v/v)로 혼합하여 만들어 사용하였다. 실험은 각각의 시료 50 μL에 FRAP 시약 1.5 mL를 혼합한 후 37℃ 항온수조에서 5 min 반응시킨 후 분광광도계(X-ma 3100, Human Corporation, Seoul, Korea) 593 nm에서의 흡광도를 측정하였다. 높은 흡광도의 값은 높은 항산화 활성을 의미한다.
8. 세포배양
본 실험에 사용한 인간 간암세포인 HepG2(Hepatoblastoma, KCLB No. 88065)는 Korea Cell Line Bank로부터 구입하여 사용하였다. 100 units/mL의 penicillin-streptomycin(GIBCO, NY, USA)과 10% fetal bovine serum(GenDEPOT, TX, USA)이 함유된 Dulbecco’s modified Eagle’s medium(GenDEPOT, TX, USA)를 사용하여 37℃, 5% CO2 incubator(Sanyo MCO-18AC, PHC Corporation, Tokyo, Japan)에서 배양하여 사용하였다. 배양된 세포는 2∼3일마다 계대배양을 하면서 실험에 사용하였다.
9. 세포내 산화적 스트레스에 대한 세포보호 효과
세포가 75% confluence 상태가 되면 24-well plate에 5 × 104 cells/mL 농도로 1 mL씩 각 well에 분주하여 5% CO2와 37℃ 조건에서 48 hr 동안 배양시킨 후 세포 생존율에 영향을 미치지 않는 시료의 농도 범위를 측정하였다(data not shown). 24-well plate에 5 × 104 cells/mL 농도로 세포를 분주하고 24 hr 배양하고 배지에 녹인 시료를 1 mL를 첨가하고 다시 24 hr 배양하였다. 그 후 각 well의 상층액을 제거한 후 2.5 mM SNP(sodium nitroprusside) 용액 1 mL를 24 hr 처리하여 산화적 스트레스를 유발하였다. 산화적 스트레스 유발 후 인삼꽃 주정 추출물을 농도별로 처리하여 다시 24 hr 배양한 뒤 세포 생존율은 MTT assay를 이용하여 측정하였다. 즉, 상등액을 제거한 후 MTT 용액(5 mg/mL)을 각 well에 첨가하고 37℃, 5% CO2 incubator에서 4 hr 더 배양 후 상등액을 제거하고 DMSO(dimethyl sulfoxide)을 이용하여 용해시킨 시료를 microplate reader(Epoch, Bio Tek Instruments, VT, USA)로 570 nm에서 흡광도를 측정하였다. 흡광도 측정 시 공시료는 DMSO로 하였고, 세포의 생존율은 다음과 같이 계산하였다.
10. 통계처리
실험 결과는 mean±S.D.로 표시하였으며 SPSS(Statistical Package for the Social Sciences) version 20.0 프로그램(SPSS Inc., Chicago, IL, USA)을 사용하여 분산분석(ANOVA) 및 t-test 방법으로 실시하였고, 각 측정 평균값의 유의성은 p<0.05 수준으로 Duncan’s multiple range test로 검증하였다.
결과 및 고찰
1. 인삼꽃 주정 추출물의 총 페놀 및 플라보노이드 함량
인삼꽃 주정 추출물의 총 페놀 및 플라보노이드 함량은 Table 1에 나타내었다. 인삼꽃 주정 추출물의 총 페놀 함량은 caffeic acid 등량값으로 표시하였으며, 시료 1 g 당 32.24±2.54 mg/g으로 측정되었다. 그리고 총 플라보노이드 함량은 quercetin 등량값으로 표시하였으며 시료 1 g 당 6.46±0.82 mg/g을 나타내었다. Kang MW 등(2020)이 보고한 인삼꽃 물 추출물의 총 페놀 함량은 22.85 mg/g, 인삼꽃 70% 에탄올의 총 페놀 함량은 28.85 mg/g을 나타내어 본 실험에서 사용한 인삼꽃 주정 추출물의 총 페놀 함량이 더 높게 나타났다. 또한 총 플라보노이드 함량에 있어서도 Kang MW 등(2020)이 보고한 인삼꽃 물 추출물(0.19 mg/g)과 70% 에탄올 추출물(1.09 mg/g)보다 본 연구에 사용한 인삼꽃 주정 추출물의 총 플라보노이드 함량이 더 높게 측정되었다. 이러한 결과는 추출 용매에 따라 인삼꽃의 총 페놀 함량과 총 플라보노이드의 함량이 달라지는 것을 알 수 있다.
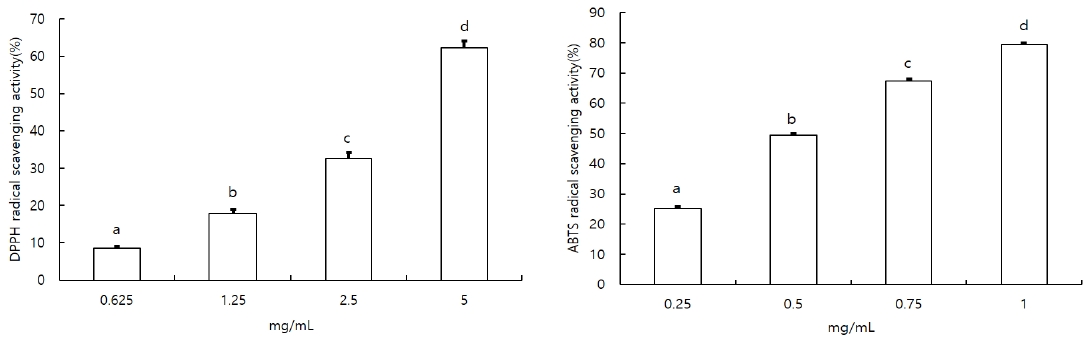
2. 인삼꽃 주정 추출물의 DPPH 및 ABTS 라디칼 소거활성
DPPH는 그 자체가 free radical로서 활성산소를 의미하고 시료의 free radical 소거 능력이나 수소 공여능력을 평가하는 방법으로 짙은 자색을 띄는 diphenylpicrylhydrazyl이 항산화제에 의해 diphenylpicrylhydazine으로 환원되면서 색깔이 사라지는 것을 517 nm의 파장에서 흡광도를 관찰하여 측정하는 방법이다(Kim MJ 등 2018). ABTS 라디칼 소거 활성은 친수성 및 소수성 물질의 항산화 활성 평가에 모두 활용되는 방법으로 ABTS와 potassium persulfate의 반응으로 생성되는 ABTS+ free radical이 시료의 항산화 물질에 의해 제거되어 짙은 청록색이 무색으로 변화되는 원리를 이용한 방법이다(Lee CW 등 2016). 인삼꽃 주정 추출물의 DPPH 라디칼 소거능과 ABTS 라디칼 소거능은 Fig. 1과 같다. 인삼꽃 주정 추출물은 농도 의존적으로 DPPH 라디칼 소거 활성을 나타내었으며 0.625 mg/mL, 1.25 mg/mL, 2.5 mg/mL 및 5 mg/mL의 농도에서 각각 8.62±0.34%, 17.87±1.10%, 32.57±1.60% 및 62.23±1.84%를 나타내었다(p<0.05). Kim HS & Ko KS(2021)은 인삼꽃 에탄올 추출물 1 mg/mL의 농도에서 71.91±5.67%의 DPPH 라디칼 소거능을 보인다고 보고하였으나 본 연구결과에서는 5 mg/mL 농도에서 62.23±1.84%로 이보다 낮은 라디칼 소거능을 나타내었다. 이러한 차이는 Kim HS & Ko KS(2021)의 연구에서는 인삼꽃에 70% 에탄올을 가하고 25℃에서 6 hr 초음파 추출법으로 시료를 제조하였기에 본 연구 결과와 차이를 보이는 것으로 보인다. 인삼꽃 주정 추출물의 ABTS 라디칼 소거능은 농도 의존적으로 증가하였으며(p<0.05), 각각의 농도에서 0.25 mg/mL(25.18±0.78%), 0.5 mg/mL(49.53±0.41%), 0.75 mg/mL(67.45±0.57%) 및 1 mg/mL(79.44±0.54%)의 소거능을 나타내었다. Kang KM 등(2012)은 개두릅 추출물의 항산화 활성 측정결과 500 μg/mL의 농도에서 DPPH 라디칼 소거능은 52.90%를 나타내었으나 ABTS 라디칼 소거능은 같은 농도에서 99.16%로 ABTS 라디칼 소거능이 더 높게 나타났다고 보고하였다. 또한 Ryu HS 등(2018)도 새송이버섯과 팽이버섯 열수 추출물의 DPPH 및 ABTS 라디칼 소거능을 측정한 결과 시료농도 10 mg/mL에서는 40% 이하의 DPPH 라디칼 소거능을 나타내었고, 시료농도 5 mg/mL에서는 70% 이상의 ABTS 라디칼 소거능을 나타낸다고 보고하였다. 본 연구에서도 인삼꽃 주정 추출물 5 mg/mL에서는 DPPH 라디칼 소거능은 62.23±1.84%, ABTS 라디칼 소거능은 1 mg/mL의 농도에서 79.44±0.54%로 ABTS 라디칼 소거능이 낮은 농도에서 더 높은 소거능을 나타내어 두 연구 보고와 유사한 결과를 나타내었다.
3. 인삼꽃 주정 추출물의 환원력 측정
환원력은 Fe3+ 이온을 F2+ 이온으로 환원시키는 능력을 측정하는 방법으로 전자를 주는 환원력이 클수록 Fe2+ 생성이 높아 푸른색을 띠게 되고 강력한 항산화제가 되는데 높은 환원력을 가지는 물질은 흡광도 수치가 높게 나타난다(Kim SH 등 2010). 인삼꽃 주정 추출물의 Fe3+ 이온을 F2+ 이온으로 환원시키는 능력을 측정한 결과를 Table 2에 나타내었다. 인삼꽃 주정 추출물은 농도가 증가할수록 환원력이 증가하였으며(p<0.05), 인삼꽃 주정 추출물이 5 mg/mL 농도에서 가장 높은 2.105±0.017의 흡광도를 나타내었다. Kim KH 등(2013)은 인삼꽃 열수 추출물 5 mg/mL 농도에서 0.48±0.04의 흡광도를 나타낸다고 보고하였으나, 본 연구에서는 같은 농도에서 2.105±0.017로 더 높은 흡광도 값을 나타내었다. 그러나 화(花)차 개발의 일환으로 찔레꽃 열수 추출물 0.5 mg/mL에서의 환원력을 측정한 결과 0.775±0.003의 흡광도를 나타내어 인삼꽃 주정 추출물보다 높은 흡광도를 나타내었다(Yeo JS 등 2014).
4. 인삼꽃 주정 추출물의 FRAP Assay에 의한 항산화 측정
FRAP 분석은 pH 3.6 이하의 조건에서 ferric tripyridyltriazine(Fe(Ⅲ)-TPTZ) 복합체가 항산화제에 의해 ferrous tripyridyltriazine(Fe(II)-TPTZ)로 환원되는 원리를 이용하여 항산화 활성을 측정하는 방법이다(Kim SG 등 2022). Table 3은 인삼꽃 주정 추출물을 이용하여 FRAP assay에 의한 항산화 활성을 측정한 결과이다. 인삼꽃 주정 추출물의 농도가 0.625, 1.25, 2.5 및 5 mg/mL일 때 각각의 흡광도 값이 0.179±0.006, 0.311±0.007, 0.549±0.023 및 1.051±0.026으로 농도 의존적으로 증가하였다(p<0.05). Beom SH 등(2021)의 보고에 의하면 찔레꽃 추출물이 항산화 화장품에 적용할 수 있는지를 검토하고자 찔레꽃 열수 추출물, 찔레꽃 70% 에탄올 추출물 및 찔레꽃 70% 아세톤 추출물을 제조 후에 비타민 C를 각각 첨가하여 시너지 효과를 나타내는지 평가하였고 그 결과 모든 시료에서 대조구로 사용한 ascorbic acid와 유사한 FRAP 값을 나타내었다고 보고하였다. 따라서 인삼꽃 추출물은 식품으로 사용할 수 있는 원료는 아니지만 높은 환원력을 보이므로 화장품 원료로 사용할 수 있는 좋은 생물자원이라고 판단된다.
5. 인삼꽃 주정 추출물 처리에 의한 세포내 산화적 스트레스 억제효과
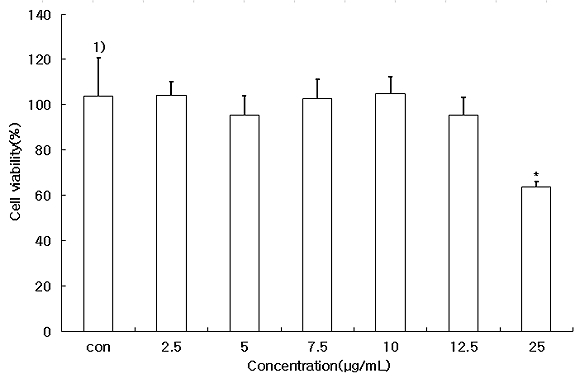
HepG2 세포에서 인삼꽃 주정 추출물의 세포독성을 조사하기 위해 다양한 농도(2.5, 5, 7.5, 10, 12.5 및 25 μg/mL)를 세포 배양액에 처리하여 세포를 각각 24 hr 배양한 후 MTT assay 실시하여 살아있는 세포수를 확인하였고 아무것도 처리하지 않은 대조군(0 μg/mL)과 비교하여 세포 생존율을 Fig. 2에 나타내었다. 인삼꽃 주정 추출물 농도를 2.5∼25 μg/mL로 처리하였고, 12.5 μg/mL의 농도까지는 대조군과 큰 차이가 없는 95% 이상의 세포 생존율을 나타내었으나 25 μg/mL에서는 63.65±2.59%로 대조군에 비해 70% 이하의 세포 생존율을 나타내어 산화적 스트레스 개선효과 측정을 위한 인삼꽃 주정 추출물 농도는 10 μg/mL 이하로 진행하였다.
세포 내 항산화 방어시스템을 증가시킬 수 있는 항산화 물질 탐색 연구에서 인간의 간세포인 HepG2 세포를 모델로 사용하고 있으며(Chung MJ 등 2006; Kim SH 등 2008; Quan YY 등 2017), 본 연구에서도 인삼꽃 주정 추출물이 HepG2 세포내 산화적 스트레스로부터 세포를 보호할 수 있는지 세포 생존율을 측정함으로써 알아보았다. HepG2 세포에 인삼꽃 주정 추출물을 농도별로 처리한 후 세포내에서 NO(nitric oxide) 공여체를 생성시키는 SNP를 처리하여 산화적 스트레스를 유발시켰을 때 세포 생존율에 미치는 영향은 Fig. 3에 나타내었다. 아무것도 처리하지 않은 무처리군(normal), SNP를 처리한 대조군(0 μg/mL) 그리고 SNP 처리군에 인삼꽃 주정 추출물을 농도별(2.5∼10 μg/mL) 처리한 실험군을 비교하였다. 그 결과 무처리군의 세포 생존율을 100%라고 보았을 때, 대조군의 세포 생존율은 49.72±1.60%로 감소하였으며(p<0.001), 인삼꽃 주정 추출물을 2.5, 5, 7.5 및 10 μg/mL 농도로 처리하였을 때 각각 49.15±4.86%, 49.15±1.69%, 53.95±4.03% 및 56.78±2.58%로 농도 의존적으로 세포 생존율이 증가하였으며 특히 인삼꽃 주정 추출물 10 μg/mL의 농도에서는 대조군에 비해 유의적으로 세포 생존율이 증가하였다(p<0.05). 항산화 활성이 높은 시료에 대해서 세포 내 항산화 방어 시스템을 증가시켜 산화적 스트레스로부터 세포를 보호 할 수 있는지에 대한 연구가 진행되고 있다. 특히 Kim SH 등(2008)은 SNP를 처리한 HepG2 세포에 더덕 및 도라지 에틸아세테이트 분획물 100 μg/mL의 농도에서 SNP 처리 대조군에 비해 유의적으로 세포 생존율이 증가하였다고 보고하였다. Ryu HS & Choi HY(2024)는 SNP 처리군(41.89%)은 세포 생존율이 감소하였으나 삼채 주정 추출물 2.5∼10 μg/mL 농도로 처리한 결과 모든 농도에서 50% 이상으로 세포생존율이 증가(p<0.05)하였다고 보고하여 본 연구 결과와 유사한 경향을 나타내었다. 이상의 결과를 종합하여 볼 때, 인삼꽃 주정 추출물이 가진 항산화 활성이 세포 내에서 발생하는 활성산소의 생성을 억제하거나 또는 제거함으로써 산화적 스트레스로부터 세포를 보호하는 것으로 판단된다.
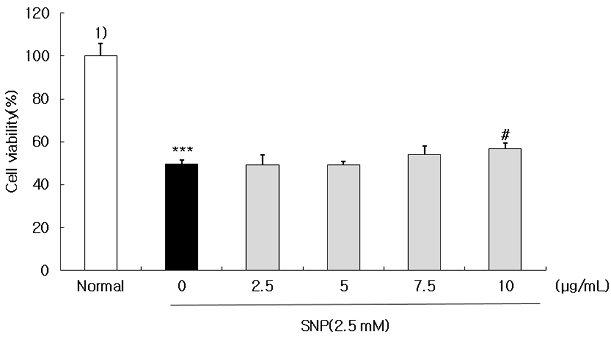
Effect of ethanol extract from Panax ginseng flower against SNP (sodium nitroprusside)-induce cytotoxicity.1) Data are expressed as mean±standard deviation of three independent experiments. *** p<0.001 indicating significant differences from the normal group. # p<0.05 indicating significant differences from the SNP group.
요 약
인삼의 생리활성 물질인 ginsenoside는 인삼의 전체 부위에 다양하게 분포되어 있다. 그러나 인삼을 수확하는 과정에서 뿌리의 생장을 돕기 위해 꽃을 제거하고 있고 그 꽃을 활용하지 못하고 있는 실정이다. 본 연구에서는 인삼꽃의 활용 가능성을 모색하고자 인삼꽃 주정 추출물을 제조하여 항산화 활성 및 HepG2 세포를 대상으로 한 산화적 스트레스 억제 효과를 검색하였다. 인삼꽃 주정 추출물의 총 페놀 및 플라보노이드 함량은 각각 32.24±2.54 mg/g 및 6.46±0.82 mg/g의 함량을 나타내었다. DPPH 라디칼과 ABTS 라디칼 소거능은 농도 의존적으로 유의적으로 증가하였다. DPPH 라디칼 소거능은 5 mg/mL에서 62.23±1.84%를 나타내었고, ABTS 라디칼 소거능은 1 mg/mL에서 79.44±0.54%를 나타내었다. 환원력은 최고 농도인 5 mg/mL에서 2.105±0.017로 높은 환원력을 나타내었고, FRAP 측정 결과 같은 농도에서 1.051±0.026의 흡광도를 나타내었다. HepG2 세포에서 인삼꽃 주정 추출물의 세포독성 측정 결과 12.5 μg/mL의 농도까지는 95% 이상의 세포 생존율을 나타내었으나 25 μg/mL에서는 63.65±2.59%로 대조군에 비해 70% 이하의 세포 생존율을 나타내었다. HepG2 세포에 인삼꽃 주정 추출물을 농도별로 처리한 후 세포내에서 NO(nitric oxide) 공여체를 생성시키는 SNP를 처리하여 산화적 스트레스를 유발시켰을 때 세포 생존율 측정하였다. 그 결과 인삼꽃 주정 추출물 10 μg/mL에서 세포 생존율이 56.78±2.58%로 SNP 단독 처리군에 비해 32% 증가하였다(p<0.05). 따라서 인삼꽃 주정 추출물은 우수한 항산화 활성 및 세포보호 효과를 확인하였고 산화적 스트레스로부터 유발될 수 있는 각종 질병에 대한 도움을 줄 수 있는 활용 가능성이 높은 소재라고 판단된다.
Acknowledgments
본 논문은 서일대학교 학술연구비에 의해 연구되었음.
References
-
Benzie IFF, Strain JJ (1996) The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: The FRAP assay. Anal Biochem 239(1): 70-76.
[https://doi.org/10.1006/abio.1996.0292]

- Beom SH, Kwon HJ, Hyun JA, Kang EB, Park HE, Han DG, Kim HJ, Choi EY, An BJ (2021) Analysis of antioxidant activity and total phenol content and flavonoid content through the synergistic effect of Rosa multiflora extracts and ascorbic acid. J Soc Cosmet Sci Korea 47(4): 333-340.
-
Blois MS (1958) Antioxidant determinations by the use of a stable free radical. Nature 181: 1199-1200.
[https://doi.org/10.1038/1811199a0]

- Cho SH (1977) Saponins of Korean Ginseng C.A. Meyer (PartⅡ)-The saponins of the ground part of ginseng. J Appl Biol Chem 20(1): 142-146.
- Choi JE, Li XG, Han YH, Lee KT (2009) Change of saponin contents of leaves, stems and flower-buds of Panax ginseng C. A. Meyer by harvesting days. Korean J Medicinal Crop Sci 17(4): 251-256.
-
Chung MJ, Hogstrand C, Lee SJ (2006) Cytotoxicity of nitric oxide is alleviated by zinc-mediated expression of antioxidant genes. Exp Biol Med 231(9): 1555-1563.
[https://doi.org/10.1177/153537020623100916]

-
Folin O, Denis W (1915) A colorimetric method for the determination of phenols (and phenol derivatives) in urine. J Biol Chem 22(2): 305-308.
[https://doi.org/10.1016/S0021-9258(18)87648-7]

-
Kang KM, No HK, Park CS, Youn KS, Hong JH, Lee SH (2012) Antioxidative activity of Kalopanax pictus shoot extracted using different extraction methods. J Korean Soc Food Sci Nutr 41(12): 1686-1692.
[https://doi.org/10.3746/jkfn.2012.41.12.1686]

- Kang MW, Kim GW, Kang KO, Shim JY, Son JY (2020) Antioxidant activities and functional components of ginseng root, ginseng fine root and ginseng flower extract. FoodService Industry Journal 16(2): 181-194.
- Kim HR, Lee CH, Jung MY, Kim JS, Kim HJ, Jeon HS, Lee SH, Kim JH, Shin MJ, Ma SY, Kwon J, Oh CH (2019) Anti-obesity effects of cultivated ginseng, -wild simulated ginseng and -red ginseng extracts. The Journal of Herbal Formula Science 27(4): 269-284.
-
Kim HS, Ko KS (2021) The effect of ginseng flower extract on the skin ageing inhibition. J Korean Soc Cosmetol 27(3): 688-694.
[https://doi.org/10.52660/JKSC.2021.27.3.688]

-
Kim HY, Joung EM, Hwang IG, Jeong JH, Yu KW, Lee JS, Jeong HS (2010) Effect of fermented ginseng extract by mushroon mycelia on antiproliferation of cancer cells. J Korean Soc Food Sci Nutr 39(1): 36-41.
[https://doi.org/10.3746/jkfn.2010.39.1.036]

-
Kim KH, Kim DM, Byun MW, Yun YS, Yook HS (2013) Antioxidant activity of panax ginseng flower-buds fermented with various microorganisms. J Korean Soc Food Sci Nutr 42(5): 663-669.
[https://doi.org/10.3746/jkfn.2013.42.5.663]

- Kim MJ, Kim JH, Lee SH, Cho EJ, Kim HY (2018) Determination of radical scavenging activity of Aster yomena (Kitam.) Honda. Journal of the Korea Academia-Industrial Cooperation Society 19(9): 402-407.
-
Kim MJ, Kwon RH, Jang MW, Ha BJ (2012) Antioxidant and anti-wrinkle effects of steamed three ginseng extracts. J Soc Cosmet Sci Korea 38(2): 155-162.
[https://doi.org/10.15230/SCSK.2012.38.2.155]

- Kim SG, Kim HY, Choi HM, Lee HJ, Han SM (2022) Antioxidant activity of honeydew honey produced by Apis mellifera L. Korean J Appl Entomol 61(4): 669-673.
- Kim SH, Choi HJ, Oh HT, Chung MJ, Cui CB, Ham SS (2008) Cytoprotective effect by antioxidant activity of Codonopsis lanceolata and Platycodon grandiflorum ethyl acetate fraction in human HepG2 cells. Korean J Food Sci Technol 40(6): 696-701.
-
Kim SH, Chung MJ, Jang HD, Ham SS (2010) Antioxidative activities of the Codonopsis lanceolata extract in vitro and in vivo. J Korean Soc Food Sci Nutr 39(2): 193-202.
[https://doi.org/10.3746/jkfn.2010.39.2.193]

-
Kim YC, Cho CW, Rhee YK, Yoo KM, Rho JH (2007) Antioxidant activity of ginseng extracts prepared by enzyme and heat treatment. J Korean Soc Food Sci Nutr 36(11): 1482-1485.
[https://doi.org/10.3746/jkfn.2007.36.11.1482]

-
Lee CW, Park YI, Kim SH, Lim HY, Chung MJ (2016) Antioxidant and anti-adipogenic activities of bread containing corn silk, job’s tears, Lentinus edodes, and apple peel in 3T3-L1 preadipocytes. J Korean Soc Food Sci Nutr 45(5): 651-663.
[https://doi.org/10.3746/jkfn.2016.45.5.651]

-
Moreno MIN, Isla MI, Sampietro AR, Vattuone MA (2000) Comparison of the free radical-scavenging activity of propolis from several region of Argentina. J Ethnopharmacol 71(1-2): 109-114.
[https://doi.org/10.1016/S0378-8741(99)00189-0]

-
Oyaizu M (1986) Studies on products of browning reaction: Antioxidative activities of products of browning reaction prepared from glucosamine. Jpn J Nutr Diet 44(6): 307-315.
[https://doi.org/10.5264/eiyogakuzashi.44.307]

-
Quan YY, Liu YH, Lin CM, Wang XP, Chen TS (2017) Peroxynitrite dominates sodium nitroprusside-induced apoptosis in human hepatocellular carcinoma cells. Oncotarget 8(18): 29833-29845.
[https://doi.org/10.18632/oncotarget.16164]

-
Re R, Pellegrini N, Proteggente A, Pannala A, Yang M, Rice-Evans C (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radic Biol Med 26(9-10): 1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]

- Ryu HS, Choi HY (2024) Antioxidant and cell protection effects of ethanolic extract from Cirsium setidens, Allium hookeri, Aronia melancocarpa. Korean J Food Nutr 37(4): 211-219.
- Ryu HS, Kim SH, Jeon MH, Choi HY (2018) Antioxidant and anticancer effects of water extract from Pleurotus eryngii, Flammulina velutipes. Korean J Food Nutr 31(6): 911-918.
-
Sung JH, Choi DH, Kim DH, Chun BG, Choi SH (2004) White ginseng saponin upregulated the production of TNF-α, IL-1β, and NO in primary cultures of mixed glial cells. J Ginseng Res 28(2): 120-126.
[https://doi.org/10.5142/JGR.2004.28.2.120]

-
Wu W, Lu Z, Teng Y, Guo YY, Liu S (2016) Structural characterization of ginsenosides from flower buds of panax ginseng by RRLC-Q-TOF MS. J Chromatogr Sci 54(2): 136-143.
[https://doi.org/10.1093/chromsci/bmv115]

-
Xue Q, He N, Wang Z, Fu X, Aung LHH, Liu Y, Li M, Cho JY, Yang Y, Yu T (2021) Functional roles and mechanisms of ginsenosides from panax ginseng in atherosclerosis. J Ginseng Res 45(1): 22-31.
[https://doi.org/10.1016/j.jgr.2020.07.002]

-
Yeo JS, Chun SS, Choi JH (2014) Antioxidant activities of solvents extracts from Rosa multiflora. J Life Sci 24(11): 1217-1223.
[https://doi.org/10.5352/JLS.2014.24.11.1217]