
생강 유래 페놀 화합물의 항산화 활성 및 B16F10 세포에서의 멜라닌 생성 억제 효과
Abstract
This study evaluated the antioxidant and skin whitening potential of phenolic compounds derived from ginger (Zingiber officinale), including 6-gingerol, 8-gingerol, 6-shogaol, and zingerone. This study examined the antioxidant activity using the DPPH radical scavenging activity and cupric ion reducing capacity assays and evaluated the whitening effects through tyrosinase inhibition, cytotoxicity assessment, and inhibition of melanin production in B16F10 cells. All phenolic compounds derived from ginger exhibited dose-dependent increases in the DPPH radical scavenging activity and cupric ion reducing capacity. The tyrosinase inhibitory activity was not concentration-dependent but was comparable to that of arbutin, the positive control. Nevertheless, melanin production was suppressed by the ginger-derived phenolic compounds in B16F10 cells. Among the tested compounds, 6-shogaol exhibited superior antioxidant activity and melanin inhibitory effects. These results suggest that ginger-derived phenolic compounds may inhibit melanogenesis through mechanisms other than direct tyrosinase inhibition. Overall, these results suggest the potential application of phenolic compounds derived from ginger as individual compounds for use as naturally derived functional food ingredients and bioactive agents.
Keywords:
gingerol, shogaol, zingerone, antioxidant, melanogenesis서 론
산화 스트레스는 활성산소종(reactive oxygen species, ROS)과 활성질소종(reactive nitrogen species, RNS)의 과도한 생성으로 인해 발생하며, 이는 세포 손상, 노화 및 다양한 만성 질환의 병태생리에 관여하는 주요 요인으로 알려져 있다(Reddy VP 2023). 이러한 반응성 물질은 정상적인 세포 신호 전달과 면역 방어에 필수적인 역할을 하지만, 체내에서 균형이 붕괴될 경우 지질 과산화, 단백질 변성 및 DNA 손상을 유발하여 인체 항상성 유지에 부정적인 영향을 미친다(Di Meo S 등 2016; Muscolo A 등 2024). 특히 산화 스트레스는 멜라닌 생성과 관련된 효소 활성 조절에 관여하는 것으로 보고되며, 색소 형성과 같은 생리적 반응의 이상을 유발할 수 있다(Kim NH & Lee AY 2023). 이에 따라 항산화 활성을 기반으로 산화 스트레스 관련 생리 반응을 조절할 수 있는 기능성 소재 개발의 필요성이 제기되고 있다.
현재 이러한 기능을 목적으로 다양한 합성 항산화 및 색소 조절 소재가 산업적으로 활용되고 있다. 과일이나 채소 등 천연자원에서 유래한 항산화 및 미백 소재도 보고되고 있으나(Xu X 등 2021), 원료 확보의 제한성, 복잡한 추출의 공정 및 성분 함량의 변동성 등으로 인해 천연 소재만으로 산업적 수요를 충족하는 데에는 한계가 있다. 이에 따라 비교적 제조가 용이하고, 비용 효율성이 높은 합성 항산화제 및 미백 소재가 널리 사용되어 왔다(Saad B 등 2007; Kim JM 등 2016). 그러나 최근 연구에 따르면 일부 합성 항산화 소재는 신장 및 간 손상, 돌연변이 유발 효과 및 암을 포함한 다양한 건강 문제의 잠재적 원인이 되며(Gulcin İ 2025), 합성 미백 성분들도 산업적으로 활용되고 있으나, 특정 화합물의 경우 자극 및 부작용이 보고되는 등 안정성 우려가 제기되고 있다(Couteau C & Coiffard L 2016). 이에 따라, 최근에는 안정성과 생리활성을 동시에 충족할 수 있는 안정적인 천연 유래 기능성 소재의 확보 및 활용에 대한 연구의 중요성이 점차 강조되고 있다.
생강(Zingiber officinale)은 전 세계적으로 다양한 음식과 음료의 향신료로 사용되어 왔을 뿐만 아니라, 소화 불량 및 기침 등 다양한 증상의 완화를 위한 약용 식물로도 활용되어 왔다(Mao QQ 등 2019). 또한, 생강은 풍부한 페놀 화합물을 포함하며, 주요 활성 성분인 gingerol은 가공 및 열처리 과정 중 shogaol, zingerone 및 paradol 등의 유도체로 전환되며, 이러한 생강 유래 화합물들은 항산화(Ali AMA 등 2018; Rossi M 등 2025), 항염증(Dugasani S 등 2010) 및 항균(Jung EH 등 2025) 등 다양한 생리활성을 나타내어 기능성 식품 및 천연 기능성 소재로서 높은 잠재력을 지닌 것으로 보고되고 있다(Ayustaningwarno F 등 2024).
생강 유래 페놀 화합물 중 주요 성분인 6-gingerol 및 6-shogaol의 항산화(Bak MJ 등 2012; Aloliqi AA 2022), 미백(Huang HC 2011; Huang HC 등 2014) 및 항노화 효과(Han HS 등 2018)에 대한 연구는 다수 보고되어 있지만, 이러한 효과가 어떠한 분자적 또는 세포 내 작용 기전을 통해 발현되는지에 대한 연구는 상대적으로 부족한 실정이다. 또한, 6-gingerol 및 6-shogaol과 구조적으로 유사한 페놀 화합물(8-gingerol 및 zingerone 등)의 기능성 소재로서의 활용 가능성에 대한 체계적인 비교 연구는 아직 제한적인 실정이다.
따라서 본 연구에서는 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone 각각의 항산화 활성을 평가하고, B16F10 세포에서 멜라닌 축적 억제 효과를 분석함으로써, 기능성 식품 및 천연 기능성 소재로서의 활용 가능성을 확인하고자 하였다.
재료 및 방법
1. 재료 및 시약
본 실험에서 사용된 생강 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone은 MedChemExpress(New Jersey, USA)에서 구매하였다. 항산화 활성을 측정하기 위해 사용한 2,2-diphenyl-1-picrylhydrazyl(DPPH), ascorbic acid, copper(Ⅱ) chloride 및 neocuproine과 세포 내의 멜라닌 합성 유도를 위한 3-isobutyl-1-methylxanthine(IBMX)과 세포 독성 측정 실험에 사용한 thiazolyl blue tetrazolium bromide(MTT)는 Sigma-Aldrich Co.(St. Louis, MO, USA)에서 구입하였다. Dimethyl sulfoxide(DMSO)는 Junsei Chemical Co., Ltd.(Chuo-ku, Tokyo, Japan)에서 구입하였다. Potassium phosphate monobasic 및 potassium phosphate dibasic anhydrous는 Daejung Chemicals & Metal Co., Ltd.(Siheung, Korea)에서 구입하였다. 실험에 사용된 B16F10 세포는 한국세포주은행(Seoul, Korea)에서 분양받았으며, 세포 배양을 위해 Dulbecco’s modified Eagle medium(DMEM), fetal bovine serum(FBS) 및 penicillin-streptomycin은 WELGENE Inc.(Daegu, Korea)에서 구입하여 사용하였다.
2. DPPH 라디칼 소거 활성 평가
DPPH(2,2-diphenyl-1-picrylhydrazyl) 라디칼 소거 활성 분석을 통해 생강 페놀 화합물의 항산화 활성을 측정하였으며, 양성대조군은 ascorbic acid를 사용하여 비교하였다. 200 μM 농도의 DPPH를 제조하기 위해 에탄올에 용해시킨 후, 96-well plate에 DPPH 190 μL를 분주 후 생강 유래 페놀 화합물(6-gingerol, 8-gingerol, 6-shogaol 및 zingerone)을 각각 10, 25 및 50 μM로 희석하여 10 μL를 넣고 빛을 차단하여 30 min 동안 반응하였으며, 양성대조군인 ascorbic acid도 동일한 농도로 처리하여 반응하였다. 이후 microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA)를 사용하여 517 nm의 흡광도를 측정하여 아래의 방법과 같이 계산하였다.
3. 구리 이온 환원력 평가
생강 유래 페놀 화합물(6-gingerol, 8-gingerol, 6-shogaol 및 zingerone)의 환원력을 측정하기 위해 구리(Ⅱ) 이온을 구리(Ⅰ) 이온으로 전환시키는 정도를 측정하였다. 생강 페놀 화합물의 농도는 각각 10, 25 및 50 μM로 단계 희석하였으며, 96-well plate에 생강 페놀 화합물 각각 40 μL, pH 7.39로 조절된 10 mM potassium phosphate buffer 60 μL를 넣어준다. 그리고 0.625 mM 농도의 neocuproine 용액 80 μL 및 증류수에 용해하여 제조한 100 μM CuCl2 용액 20 μL를 분주한 후 25℃에서 1 hr 동안 반응시켰다. 또한, 양성대조군인 ascorbic acid의 농도는 동일하게 처리하여 반응시킨 후 microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA)로 454 nm에서 흡광도를 측정하였다. 측정된 흡광도는 구리(Ⅰ)/neocuproine의 extinction coefficient(7.95×103 M—1cm—1)를 이용하여 환산하였다.
4. Tyrosinase 저해 활성
Tyrosinase 저해 활성을 평가하기 위해 tyrosinase와 반응하는 L-tyrosine을 기질로 하여 생강 유래 페놀 화합물(6-gingerol, 8-gingerol, 6-shogaol 및 zingerone)의 저해 활성을 평가하였다. 양성 대조군으로는 tyrosinase 저해 활성이 우수한 arbutin을 사용하였다. 96-well plate에 10, 25 및 50 μM 농도로 단계 희석한 생강 페놀 화합물 용액 20 μL, 1.5 mM 농도의 기질 L-tyrosine 40 μL 및 0.1 M sodium phosphate buffer(pH 6.49) 220 μL을 첨가한 후, 1,500 U tyrosinase 20 μL를 첨가하여 37℃에서 15 min 동안 반응시켰다. 양성대조군 arbutin은 생강 페놀 화합물과 동일한 농도로 처리하였으며, 반응 후 microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA)의 490 nm에서 흡광도를 측정하여 아래와 같은 식으로 계산하였다.
5. 생강 페놀 화합물의 세포 생존율
생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone을 처리하였을 때 B16F10 세포에서 독성 여부를 평가하기 위해 MTT assay를 실시하였다. 1, 5 및 10 μM 농도의 생강 페놀 화합물을 포함한 FBS-media는 24 hr 동안 처리한 후, FBS-media를 완전히 제거하였다. 이후 200 μg/mL 농도의 MTT-media를 첨가한 다음 1 hr 동안 반응시킨 후 완전히 제거하고 각 well에 DMSO 1 mL를 첨가하여 생성된 formazan을 용해하였다. 이후 녹인 formazan 100 μL씩 96-well plate에 분주하여 흡광도 570 nm에서 microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA)를 통해 세포 생존율(%)을 측정 후 계산하였다.
6. B16F10 세포에서 멜라닌 생합성 억제 활성
B16F10 세포에 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone을 처리하였을 때 멜라닌 생합성 억제 활성을 평가하였다. 0.75 mM IBMX를 처리하여 멜라닌 생성을 유도한 후 생강 페놀 화합물을 각각 1, 5 및 10 μM 농도로 96 hr 동안 처리하였다. 세포 내의 멜라닌 축적에 대한 생강 페놀 화합물의 억제 정도는 현미경(Optinity; Korea Lab Tech, Hwaseong, Korea)을 통해 관찰하였다. 이후 생강 페놀 화합물을 포함한 media를 완전히 제거하여 PBS로 세척하고 각 well에 trypsin-EDTA 200 μL씩 처리하여 세포를 분리한 후, 453 ×g에서 5 min 동안 원심분리 하여 얻은 pellet에 1 N NaOH와 10% DMSO를 첨가하고 100℃에서 10 min 동안 가열하여 용해시킨 다음 microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA)를 사용하여 405 nm에서 흡광도를 측정하여 멜라닌 억제 활성을 평가하였다.
7. 통계분석
본 연구에서 모든 실험은 3회 이상 독립적으로 반복하였고, 실험 결과는 평균±표준편차로 표현하였으며, 얻어진 결과의 통계분석은 SPSS software(Ver. 18, SPSS Inc., Chicago, IL, USA)를 이용하여 수행하였다. 세 집단 이상 비교는 일원배치 분산분석(one-way ANOVA) 후 Duncan’s test를 통해 p<0.05 수준에서 유의성을 검정하였으며, 두 집단 간 비교에는 t-test를 이용하였다.
결과 및 고찰
1. 생강 유래 페놀 화합물의 DPPH 라디칼 소거 활성 평가
DPPH(2,2-diphenyl-1-picrylhydrazyl)는 질소 원자에 있는 단일 전자가 항산화제로부터 수소 원자를 받아 환원되는 안정적인 자유 라디칼이며, 강렬한 색을 나타내는 특성 때문에 DPPH 라디칼을 이용한 항산화 활성 평가가 광범위하게 사용되는 대표적인 항산화 분석법이다(Gulcin İ & Alwasel SH 2023). 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone의 항산화 활성을 평가하기 위해 DPPH 라디칼 소거 활성을 측정하였다. 각 생강 페놀 화합물은 10, 25 및 50 μM의 농도로 평가하였다. 그 결과, 6-gingerol은 각각 18.15%, 27.96% 및 38.66%의 소거 활성을 나타내었으며, 8-gingerol는 17.43%, 29.42% 및 41.17%를 나타내었다. 또한, 6-shogaol은 21.80%, 34.32% 및 46.47%를, zingerone은 18.95%, 27.03% 및 40.99%를 나타내었다. 양성대조군 ascorbic acid는 동일한 농도에서 생강 유래 페놀 화합물과 비교하였을 때 통계적으로 유의하게 높은 활성을 나타내었지만, 생강 유래 페놀 화합물 또한 농도 의존적으로 항산화 활성이 증가하는 경향을 보였으며, 상대적으로 우수한 DPPH 라디칼 소거 활성을 나타내었다(Fig. 1). 생강의 유용성분으로 알려진 6-gingerol, 8-gingerol 및 6-shogaol 등을 함유한 생강 에탄올 추출물은 DPPH 라디칼 소거 활성 평가에서 다른 분획물과 비교하여 높은 항산화 활성을 나타내었다(Lee EJ 등 2011). 또한, 생강에 함유된 gingerol 및 그 유사체의 DPPH 라디칼 소거 활성을 비교한 연구에서도 본 논문의 결과와 같이 6-shogaol에서 높은 항산화 활성을 보였다고 보고되었다(Dugasani S 등 2010). 이러한 선행 연구 결과와 본 연구의 결과를 종합할 때, 생강 유래 페놀 화합물은 천연 항산화 소재로 활용될 수 있는 잠재력을 지닌 것으로 사료된다.
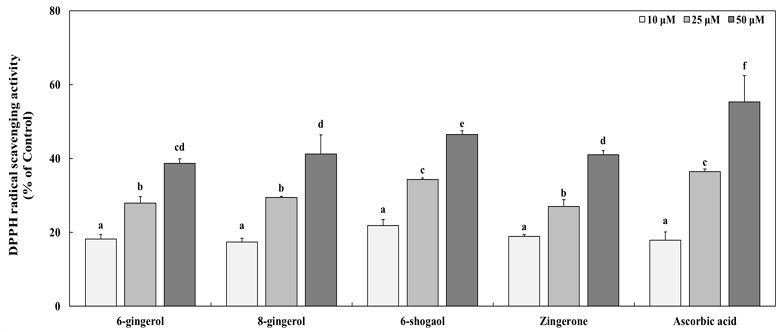
The DPPH radical scavenging activities of ginger (Zingiber officinale)-derived phenolic compounds.The DPPH radical scavenging activities of ginger-derived phenolic compounds (6-gingerol, 8-gingerol, 6-shogaol, and zingerone) and ascorbic acid, which was used as a positive control, were analyzed at concentrations of 10, 25, and 50 μM in this test. Values are presented as mean±S.D. and different letters indicate significant differences based on one-way ANOVA followed by Duncan’s multiple range test (p<0.05).
2. 생강 유래 페놀 화합물의 구리 이온 환원력 측정
항산화 능력은 시험관 내(in vitro) 연구에서 광범위하게 수행되어 왔으며, 항산화 활성은 다양한 기전과 물질 특성에 따라 다르게 발현되므로 이를 평가하기 위해 여러 분석 방법이 사용되어 왔다(Kotha RR 등 2022). 여러 방법 중 전자 전달 기반 분석은 항산화제가 기질에 전자를 전달하는 능력을 측정함으로써 항산화 활성을 평가하는 방식이다(Granato D 등 2018). 본 실험에서는 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone의 항산화 활성을 평가하기 위해 구리(II)-neocuproine 시약을 산화제로 사용하였으며, 항산화제에 의해 환원된 구리(Ⅰ)-neocuproine 착화물의 형성을 측정하였다(Apak R 등 2007). 그 결과, 6-gingerol은 각각 16.36, 29.42 및 35.72 μM의 환원력을 나타내었으며, 8-gingerol는 16.91, 32.95 및 41.77 μM을 나타내었다. 또한, 6-shogaol은 21.66, 35.89 및 46.37 μM를, zingerone은 16.33, 25.62 및 36.28 μM를 나타내었다. 생강 유래 페놀 화합물과 동일한 농도의 양성 대조군인 ascorbic acid와 비교하였을 때, 50 μM 농도에서 8-gingerol은 ascorbic acid와 유사한 활성을 나타내었고, 6-shogaol은 ascorbic acid보다 유의적으로 높은 활성을 나타내었다(Fig. 2). Choi SY & Kim KT(2022)의 선행 연구에서 추출 온도와 추출 시간을 달리하여 생강 추출물의 항산화 활성을 비교한 결과, 가장 높은 항산화 효과를 나타낸 조건에서 6-gingerol과 6-shogaol의 함량이 유의적으로 높게 나타났다고 보고하였다. 또한, 6-gingerol과 6-shogaol을 함유한 phytosome을 이용한 항산화 활성 평가 중 Fe 이온을 이용한 환원력 실험 결과, 6-gingerol과 6-shogaol을 함유한 피토솜이생강 추출물보다 우수한 환원력과 항산화 활성이 보고되었다(Mariue N 등 2024). 이러한 선행연구 결과를 통해, 생강 추출물 자체의 항산화 활성도 우수하지만, 생강 유래 페놀 화합물을 단독 및 복합으로 사용하거나 전달체 형태로 적용 시 항산화 효과가 더욱 증진될 가능성이 있는 것으로 판단된다.
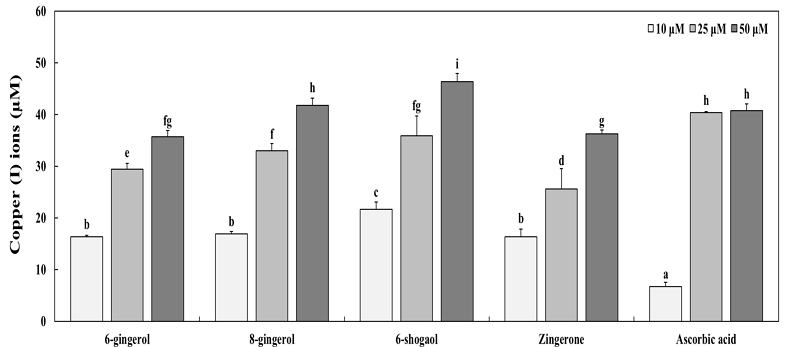
The cupric ions-reducing capacities of ginger (Zingiber officinale)-derived phenolic compounds.The cupric ions-reducing capacities of ginger-derived phenolic compounds (6-gingerol, 8-gingerol, 6-shogaol, and zingerone) and ascorbic acid, which was used as a positive control, were analyzed at concentrations of 10, 25, and 50 μM in this test. Values are presented as mean±S.D. and different letters indicate significant differences based on one-way ANOVA followed by Duncan’s multiple range test (p<0.05).
3. 생강 유래 페놀 화합물의 Tyrosinase 저해 활성 평가
멜라닌 생성과 피부의 색소 침착은 자외선으로부터 피부를 보호하는 중요한 요소이지만, 비정상적인 생성 감소나 탈색은 심각한 피부 질환 문제를 야기할 수 있다(Brenner M & Hearing VJ 2008). 멜라닌은 다수의 효소적 및 화학적 반응의 복잡한 과정으로 생성되며, tyrosinase 및 tyrosinase 관련 단백질과 같은 효소들이 멜라닌 합성에 중요한 역할을 한다(Garcia-Jimenez A 등 2017). 특히 tyrosinase는 멜라닌 합성에서 속도 제한 효소로 작용하므로, 해당 효소의 활성을 조절하는 것은 멜라닌 생성 조절에 있어 핵심적인 요소로 여겨진다(Zolghadri S 등 2019). 본 실험에서는 L-tyrosine을 기질로 사용하여 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone의 tyrosinase 저해 활성을 평가하였다. 그 결과 6-gingerol은 63.09%, 66.53% 및 67.41%의 tyrosinase 저해 활성을 나타내었으며, 8-gingerol은 63.29%, 64.90% 및 68.30%를 나타내었다. 또한, 6-shogaol은 64.42%, 66.14% 및 68.07%를, zingerone은 64.35%, 64.83% 및 66.44%의 저해 활성을 보였다. 본 연구에서 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone은 모든 처리 농도에서 tyrosinase 활성을 효과적으로 억제하였으며, 양성대조군 arbutin보다 유의적으로 높은 저해 활성을 나타내었다(Fig. 3). 선행 연구(Kim SY 등 2021)에서도 추출 용매를 달리한 생강 추출물로 tyrosinase 활성을 전반적으로 억제하였으나 농도 의존적인 경향은 나타나지 않았다고 보고하였다. 이러한 결과를 종합하면, 생강 유래 페놀 화합물이 농도 증가에 따른 저해 양상보다는 성분 자체의 활성에 의해 tyrosinase 활성을 억제하는 효과를 가지며, 이는 미백 기능성 소재로의 활용 가능성을 시사한다.
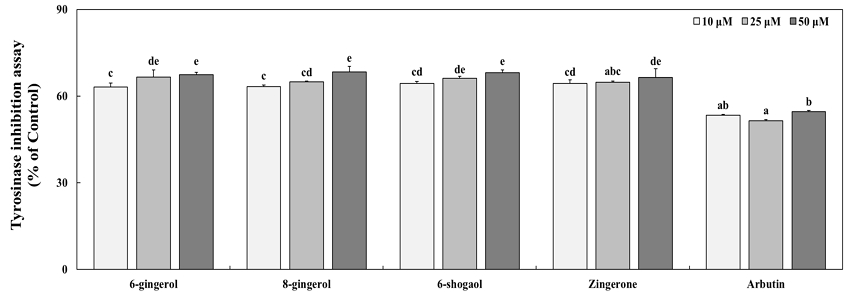
The tyrosinase inhibition activities of ginger (Zingiber officinale)-derived phenolic compounds.The tyrosinase inhibition activities of ginger-derived phenolic compounds (6-gingerol, 8-gingerol, 6-shogaol, and zingerone) and arbutin, which was used as a positive control, were evaluated at concentrations of 10, 25, and 50 μM in this test. Values are presented as mean±S.D. and different letters indicate significant differences based on one-way ANOVA followed by Duncan’s multiple range test (p<0.05).
4. B16F10 세포에서 생강 유래 페놀 화합물 처리에 대한 세포 생존율 평가
B16F10 세포에서 생강 유래 페놀 화합물(6-gingerol, 8-gingerol, 6-shogaol 및 zingerone)의 세포 독성을 평가하기 위해 MTT assay를 실시하였다(Fig. 4). 대조군과 생강 유래 페놀 화합물을 1, 5 및 10 μM의 농도로 24 hr 동안 처리한 결과, B16F10 세포의 생존율은 6-gingerol에서 각각 100.23%, 103.86% 및 102.05%의 생존율을 나타내었고, 8-gingerol은 98.01%, 100.33% 및 100.72%를 나타내었다. 또한, 6-shogaol에서 99.26%, 100.31% 및 101.65%를, zingerone에서는 103.21%, 103.03% 및 102.02%의 생존율을 나타내었으며, 결과적으로 생강 유래 페놀 화합물들의 모든 농도에서 대조군과 유의적인 차이를 나타내지 않았다. 이러한 결과를 바탕으로 생강 유래 페놀 화합물은 해당 농도 범위에서 B16F10 세포에 대한 세포 독성을 나타내지 않았기에, 이후 실험은 1, 5 및 10 μM의 농도로 진행하였다.
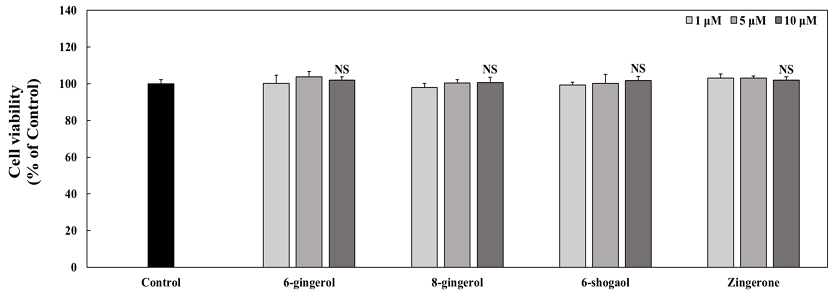
The cytotoxic effects of ginger (Zingiber officinale)-derived phenolic compounds treatments for 24 hr in B16F10 cells.The cytotoxic effects of isolated ginger phenolic compounds (6-gingerol, 8-gingerol, 6-shogaol, and zingerone) were assessed at concentrations of 1, 5, and 10 μM. Different letters represent significant differences as determined by t-test.NS: Not significant.
5. B16F10 세포에서 생강 유래 페놀 화합물 처리에 대한 멜라닌 억제 활성
생강 유래 페놀 화합물(6-gingerol, 8-gingerol, 6-shogaol 및 zingerone)이 멜라닌 생합성을 억제하는 효과를 평가하기 위해 B16F10 세포에 0.75 mM 3-isobutyl-1-methylxanthine(IBMX)을 처리하여 멜라닌 생성을 유도한 후, 각 생강 유래 페놀 화합물을 1, 5 및 10 μM 농도로 96 hr 동안 처리하였다. 생강 유래 페놀 화합물 처리 후, B16F10 세포에서 세포 외로 분비된 멜라닌 함량을 측정하였으며, 동시에 현미경 관찰을 통해 세포 내 멜라닌 축적 정도를 각각 분석함으로써 멜라닌 생합성 억제 효과를 평가하였다(Figs. 5 and 6). 세포 외로 분비된 멜라닌 함량은 멜라닌 생성을 유도한 대조군과 비교하였을 때, 6-gingerol에서 각각 98.09%, 88.24% 및 81.62%를 나타내었고, 8-gingerol은 79.76%, 76.48% 및 60.66%로 감소하였다. 또한, 6-shogaol에서 88.47%, 64.52% 및 58.05%를 나타내었고, zingerone에서는 98.65%, 101.18% 및 96.59%로 나타났다. 이러한 결과를 바탕으로, 6-gingerol과 zingerone은 모든 농도에서 대조군 대비 유의적인 차이를 보이지 않았으나, 8-gingerol과 6-shogaol은 농도가 증가함에 따라 세포 외 멜라닌 분비량이 유의적으로 감소함이 관찰되었다(Fig. 5A). 또한, B16F10 세포 내에서 멜라닌 축적 정도를 분석한 결과, 멜라닌 생성을 유도한 대조군과 비교했을 때, 6-gingerol에서 각각 44.64%, 39.85% 및 33.17%로 멜라닌 축적이 감소하였으며, 8-gingerol은 44.18%, 37.19% 및 32.10%로 감소하였다. 또한, 6-shogaol에서 41.19%, 28.83% 및 25.52%의 감소를 나타내었고, zingerone에서는 52.48%, 54.12% 및 46.33%를 보였다(Fig. 5B). B16F10 세포 내에 축적된 멜라닌의 양을 이미지 기반으로 정성적 분석한 결과, 앞선 세포 내 멜라닌 축적의 정량 분석 결과와 유사하게 멜라닌 생성을 유도한 대조군 대비 생강 페놀 화합물을 처리한 군에서 전반적으로 멜라닌 형성이 감소한 것으로 관찰되었다(Figs. 6A and B). 선행연구(Yao C 등 2013)에서 생강의 주요 성분인 6-shogaol로 미백 활성을 평가한 결과, 본 연구와 유사하게 tyrosinase 저해 활성에서 뚜렷한 효과가 나타나지 않았으나, 멜라닌 축적 농도 의존적으로 유의하게 감소하는 것으로 보고되었다. 이러한 결과는 생강 페놀 화합물이 tyrosinase를 직접적으로 억제하기보다는, 다른 세포 내 경로를 통해 멜라닌 축적을 억제함으로써 미백 활성을 나타낼 가능성을 시사한다. 이와 같은 결과를 바탕으로, 본 연구에서 사용된 생강 유래 페놀 화합물들의 구조적 특성을 고려할 때, 이들 화합물은 공통적으로 페놀성 수산기를 포함하고 있으나 알킬 사슬 길이 및 작용기의 차이에 따라 생리활성에 차이를 나타내는 것으로 판단된다(Jiang X 2025). 특히, 6-shogaol의 경우 α,β-불포화 카보닐 구조를 포함하는 구조적 특징을 지니기에 다른 화합물에 비해 멜라닌 형성 억제 효과가 상대적으로 우수하게 나타났을 가능성이 있다(Dugasani S 등 2010). 이러한 구조적 차이에 따른 생리활성의 차이는, 생강 유래 페놀 화합물이 tyrosinase의 직접적인 저해 이외의 기전을 통해 멜라닌 형성 억제를 유도했을 가능성을 시사한다. 또한 zingerone의 경우, 세포 외로 분비된 멜라닌의 양에서는 유의적인 감소가 관찰되지 않았으나, 세포 내 멜라닌 축적은 전반적으로 감소하는 경향을 나타내었다. 이는 zingerone이 멜라닌 분비 단계보다는 세포 내 멜라닌 생성 과정에 보다 선택적으로 작용할 가능성을 시사한다. 본 연구에서는 멜라닌 생성과 관련된 신호전달 경로 또는 전사 인사 조절과 같은 분자 수준의 기전을 직접적으로 규명하지 못하였으므로, 향후 멜라닌 생성 관련 신호전달 경로 및 핵심 조절 인자의 발현 분석을 포함한 추가적인 연구가 필요할 것으로 사료된다.
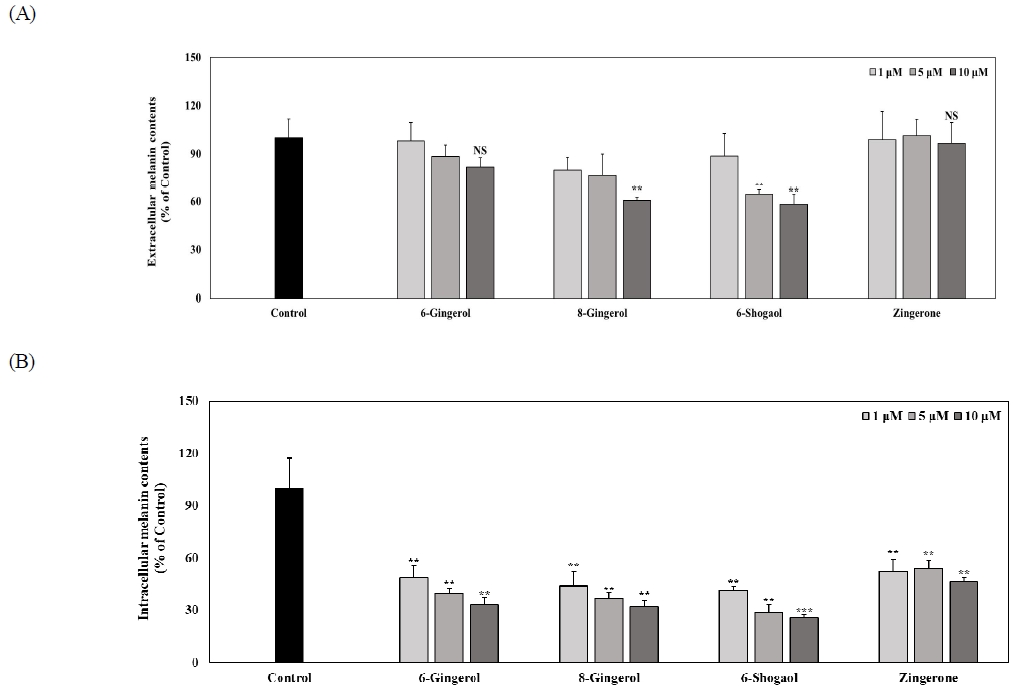
Effects of ginger (Zingiber officinale)-derived phenolic compounds treatments on extracellular and intracellular melanin content of B16F10 cells.Extracellular melanin (A) and intracellular melanin (B) content of B16F10 cells were quantified by measuring absorbance at 405 nm. Melanin was induced using 0.75 mM IBMX. Statistical significance was determined by t-test (** p<0.01, *** p<0.001 vs. control).NS: Not significant.
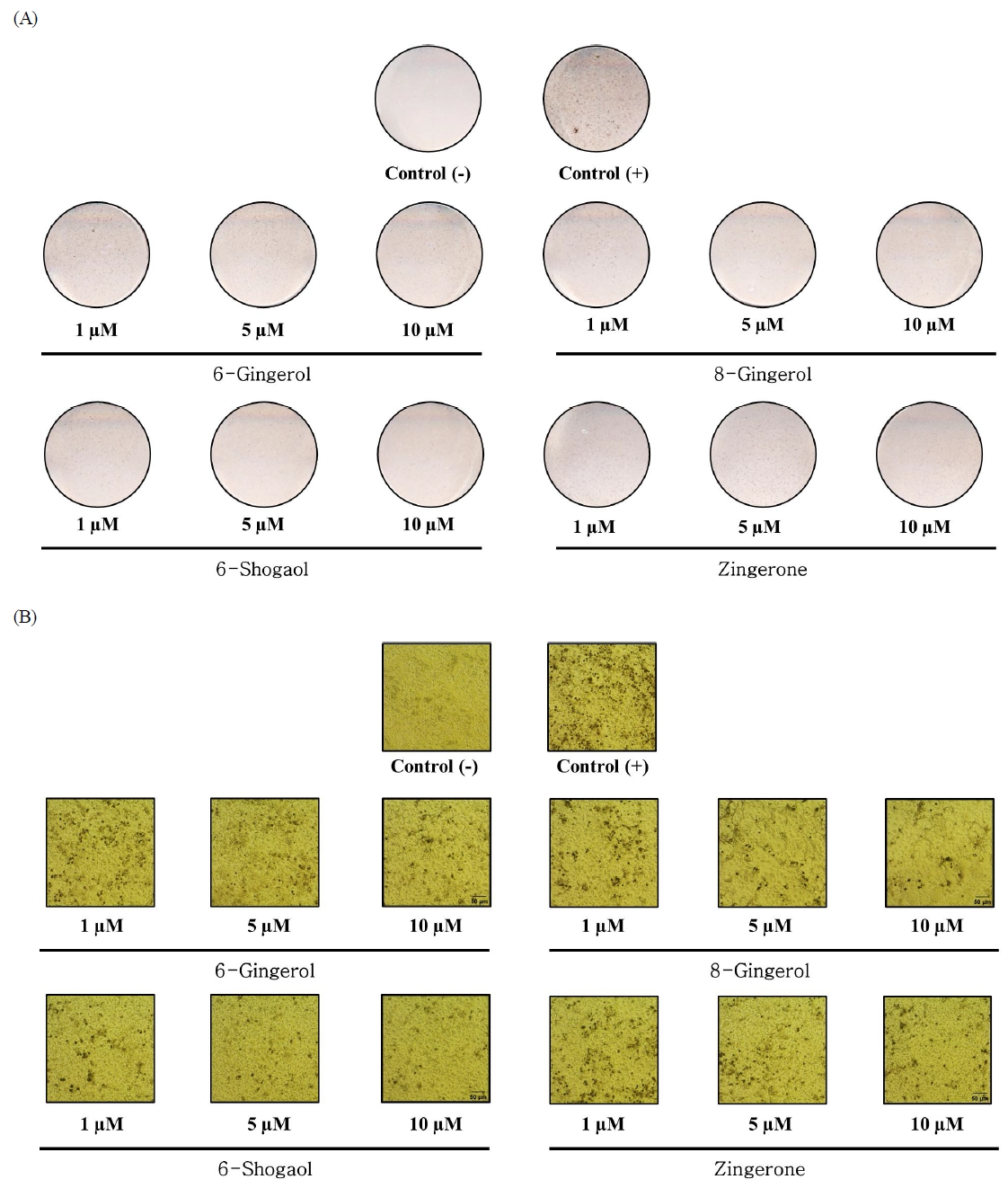
Effects of ginger (Zingiber officinale)-derived phenolic compounds treatments on intracellular melanin content of B16F10 cells.Melanin accumulation in B16F10 cells in the presence or absence of isolated ginger phenolic compounds (6-gingerol, 8-gingerol, 6-shogaol, and zingerone) was assessed using scanned images (A) and photomicrographs (B). All photomicrographs were acquired at the same magnification. The scale bar represents 50 μm.
요 약
본 연구에서는 생강 유래 페놀 화합물인 6-gingerol, 8-gingerol, 6-shogaol 및 zingerone의 항산화 및 미백 활성을 평가하여 이들 화합물의 천연 기능성 소재로서의 잠재력을 확인하고자 하였다. 항산화 활성을 측정하기 위해 DPPH 라디칼 소거 활성 실험과 구리 이온의 환원력 실험을 진행한 결과, 생강 유래 페놀 화합물들은 두 실험 모두에서 농도 의존적으로 항산화 활성을 나타내었다. 또한, 미백 활성을 확인하고자 tyrosinase 저해 활성을 평가하였을 때, 농도 의존적인 경향은 뚜렷하게 나타나지 않았으나 전반적으로 tyrosinase 저해 효과를 확인하였다. 또한, B16F10 세포에서의 생강 페놀 화합물 처리에 의한 멜라닌 축적 억제를 평가한 결과, 6-gingerol, 8-gingerol 및 6-shogaol은 농도 의존적으로 세포 내 멜라닌 축적을 억제하였으며, zingerone은 농도 의존적이지는 않지만, 멜라닌 축적을 효과적으로 억제하는 것을 확인하였다. 이러한 본 연구의 결과를 종합해 볼 때, 생강 유래 페놀 화합물들은 항산화 및 미백 활성에 있어 우수한 효능을 나타내었으며, 개별 화합물 단독으로도 천연 기능성 식품 소재로 활용될 수 있음을 시사하였다. 추후 이들 화합물의 항산화 및 미백 효과에 대한 작용 기전 규명을 위한 추가적인 연구가 진행되어야 할 것으로 판단된다.
Acknowledgments
본 과제는 2025년도 교육부 및 경상남도의 재원으로 경상남도RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다(2025-RISE-16-005-R003).
References
-
Ali AMA, El-Nour MEM, Yagi SM (2018) Total phenolic and flavonoid contents and antioxidant activity of ginger (Zingiber officinale Rosc.) rhizome, callus and callus treated with some elicitors. J Genet Eng Biotechnol 16(2): 677-682.
[https://doi.org/10.1016/j.jgeb.2018.03.003]

-
Aloliqi AA (2022) Therapeutic potential of 6-gingerol in prevention of colon cancer induced by azoxymethane through the modulation of antioxidant potential and inflammation. Curr Issues Mol Biol 44(12): 6218-6228.
[https://doi.org/10.3390/cimb44120424]

-
Apak R, Güçlü K, Demirata B, Ozyürek M, Celik SE, Bektaşoğlu B, Berker KI, Ozyurt D (2007) Comparative evaluation of various total antioxidant capacity assays applied to phenolic compounds with the CUPRAC assay. Molecules 12(7): 1496-1547.
[https://doi.org/10.3390/12071496]

-
Ayustaningwarno F, Anjani G, Ayu AM, Fogliano V (2024) A critical review of ginger’s (Zingiber officinale) antioxidant, anti-inflammatory, and immunomodulatory activities. Front Nutr 11: 1364836.
[https://doi.org/10.3389/fnut.2024.1364836]

-
Bak MJ, Ok S, Jun M, Jeong WS (2012) 6-Shogaol-rich extract from ginger up-regulates the antioxidant defense systems in cells and mice. Molecules 17(7): 8037-8055.
[https://doi.org/10.3390/molecules17078037]

-
Brenner M, Hearing VJ (2008) The protective role of melanin against UV damage in human skin. Photochem Photobiol 84(3): 539-549.
[https://doi.org/10.1111/j.1751-1097.2007.00226.x]

-
Choi SY, Kim KT (2022) Anti-oxidative and muscle cell protective effects of ginger extract according to the extraction conditions. Food Sci Preserv 29(5): 762-767.
[https://doi.org/10.11002/kjfp.2022.29.5.762]

-
Couteau C, Coiffard L (2016) Overview of skin whitening agents: Drugs and cosmetic products. Cosmetics 3(3): 27.
[https://doi.org/10.3390/cosmetics3030027]

-
Di Meo S, Reed TT, Venditti P, Victor VM (2016) Role of ROS and RNS sources in physiological and pathological conditions. Oxid Med Cell Longev 2016: 1245049.
[https://doi.org/10.1155/2016/1245049]

-
Dugasani S, Pichika MR, Nadarajah VD, Balijepalli MK, Tandra S, Korlakunta JN (2010) Comparative antioxidant and anti-inflammatory effects of [6]-gingerol, [8]-gingerol, [10]-gingerol and [6]-shogaol. J Ethnopharmacol 127(2): 515-520.
[https://doi.org/10.1016/j.jep.2009.10.004]

-
Garcia-Jimenez A, Teruel-Puche JA, Garcia-Ruiz PA, Berna J, Rodríguez-López JN, Tudela J, Garcia-Canovas F (2017) Action of 2,2′,4,4′-tetrahydroxybenzophenone in the biosynthesis pathway of melanin. Int J Biol Macromol 98: 622-629.
[https://doi.org/10.1016/j.ijbiomac.2017.02.032]

-
Granato D, Shahidi F, Wrolstad R, Kilmartin P, Melton LD, Hidalgo FJ, Miyashita K, Camp JV, Alasalvar C, Ismail AB, Elmore S, Birch GG, Charalampopoulos D, Astley SB, Pegg R, Zhou P, Finglas P (2018) Antioxidant activity, total phenolics and flavonoids contents: Should we ban in vitro screening methods? Food Chem 264: 471-475.
[https://doi.org/10.1016/j.foodchem.2018.04.012]

-
Gulcin İ (2025) Antioxidants: A comprehensive review. Arch Toxicol 99(5): 1893-1997.
[https://doi.org/10.1007/s00204-025-03997-2]

-
Gulcin İ, Alwasel SH (2023) DPPH radical scavenging assay. Processes 11(8): 2248.
[https://doi.org/10.3390/pr11082248]

-
Han HS, Kim KB, Jung JH, An IS, Kim YJ, An S (2018) Anti-apoptotic, antioxidant and anti-aging effects of 6-shogaol on human dermal fibroblasts. Biomed Dermatol 2(1): 27.
[https://doi.org/10.1186/s41702-018-0037-4]

-
Huang HC, Chang SJ, Wu CY, Ke HJ, Chang TM (2014) [6]-Shogaol inhibits α-MSH-induced melanogenesis through the acceleration of ERK and PI3K/AKT-mediated MITF degradation. Biomed Res Int 2014: 842569.
[https://doi.org/10.1155/2014/842569]

-
Huang HC, Chiu SH, Chang TM (2011) Inhibitory effect of [6]-gingerol on melanogenesis in B16F10 melanoma cells and a possible mechanism of action. Biosci Biotechnol Biochem 75(6): 1067-1072.
[https://doi.org/10.1271/bbb.100851]

-
Jiang X (2025) Biological mechanisms, pharmacological and pathological activities, and quality optimization of gingerols and shogaols. J Funct Foods 127: 106773.
[https://doi.org/10.1016/j.jff.2025.106773]

-
Jung EH, Hwang G, Kim KR (2025) Effect of 6-shogaol derived from ginger (Zingiber officinale) on dual-species biofilm formation by Streptococcus mutans and Candida albicans. Nutrients 17(18): 2999.
[https://doi.org/10.3390/nu17182999]

-
Kim JM, Choi SH, Shin GH, Lee JH, Kang SR, Lee KY, Lim HS, Kang TS, Lee OH (2016) Method validation and measurement uncertainty for the simultaneous determination of synthetic phenolic antioxidant in edible oils commonly consumed in Korea. Food Chem 213: 19-25.
[https://doi.org/10.1016/j.foodchem.2016.06.053]

-
Kim NH, Lee AY (2023) Oxidative stress induces skin pigmentation in melasma by inhibiting hedgehog signaling. Antioxidants 12(11): 1969.
[https://doi.org/10.3390/antiox12111969]

- Kim SY, Choi MY, Do E, Kim MR (2021) Comparative evaluation on biological activities of Zingiber officinale Roscoe extracted from different solvents. Kor J Herbol 36(2): 19-29.
-
Kotha RR, Tareq FS, Yildiz E, Luthria DL (2022) Oxidative stress and antioxidants: A critical review on in vitro antioxidant assays. Antioxidants 11(12): 2388.
[https://doi.org/10.3390/antiox11122388]

-
Lee EJ, Yang SA, Choi HD, Im HG, Whang K, Lee IS (2011) Comparison of gingerols in various fractions and the antioxidant effects of supercritical fluid extracts from ginger. Korean J Food Sci Technol 43(4): 469-474.
[https://doi.org/10.9721/KJFST.2011.43.4.469]

-
Mairuae N, Noisa P, Palachai N (2024) Phytosome-encapsulated 6-gingerol-and 6-shogaol-enriched extracts from Zingiber officinale Roscoe protect against oxidative stress-induced neurotoxicity. Molecules 29(24): 6046.
[https://doi.org/10.3390/molecules29246046]

-
Mao QQ, Xu XY, Cao SY, Gan RY, Corke H, Beta T, Li HB (2019) Bioactive compounds and bioactivities of ginger (Zingiber officinale Roscoe). Foods 8(6): 185.
[https://doi.org/10.3390/foods8060185]

-
Muscolo A, Mariateresa O, Giulio T, Mariateresa R (2024) Oxidative stress: The role of antioxidant phytochemicals in the prevention and treatment of diseases. Int J Mol Sci 25(6): 3264.
[https://doi.org/10.3390/ijms25063264]

-
Reddy VP (2023) Oxidative stress in health and disease. Biomedicines 11(11): 2925.
[https://doi.org/10.3390/biomedicines11112925]

-
Rossi M, Teitsworth TS, McKenzie E, Caruso A, Thieke N, Caruso F (2025) Ginger (Zingiber officinale) and zingerone antioxidant properties studied using hydrodynamic voltammetry, zingerone crystal structure and density functional theory (DFT)-results support zingerone experimental catalytic behavior similar to superoxide dismutases (SODs). Int J Mol Sci 26(21): 10645.
[https://doi.org/10.3390/ijms262110645]

-
Saad B, Sing YY, Nawi MA, Hashim N, Ali ASM, Saleh MI, Sulaiman SF, Talib KM, Ahmad K (2007) Determination of synthetic phenolic antioxidants in food items using reversed-phase HPLC. Food Chem 105(1): 389-394.
[https://doi.org/10.1016/j.foodchem.2006.12.025]

-
Xu X, Liu A, Hu S, Ares I, Martínez-Larrañaga MR, Wang X, Martínez M, Anadón A, Martínez MA (2021) Synthetic phenolic antioxidants: Metabolism, hazards and mechanism of action. Food Chem 353: 129488.
[https://doi.org/10.1016/j.foodchem.2021.129488]

-
Yao C, Oh JH, Oh IG, Park C, Chung JH (2013) [6]-Shogaol inhibits melanogenesis in B16 mouse melanoma cells through activation of the ERK pathway. Acta Pharmacol Sin 34(2): 289-294.
[https://doi.org/10.1038/aps.2012.134]

-
Zolghadri S, Bahrami A, Hassan Khan MT, Munoz-Munoz J, Garcia-Molina F, Garcia-Canovas F, Saboury AA (2019) A comprehensive review on tyrosinase inhibitors. J Enzyme Inhib Med Chem 34(1): 279-309.
[https://doi.org/10.1080/14756366.2018.1545767]

