Cimicifuga heracleifolia Kom. 에탄올 추출물의 항비만 가능성 : AMPK 신호전달 경로를 통한 3T3-L1 지방세포 분화 억제 기전 탐색


Abstract
This study investigated the anti-obesity effects of the ethanol extract of Cimicifuga heracleifolia Kom. (CHEE) and its molecular mechanisms using 3T3-L1 preadipocytes. The ethanol extract of Cimicifuga heracleifolia Kom. was prepared by extraction with 70% ethanol. 3T3-L1 preadipocytes were treated with CHEE, and the levels of lipid accumulation, protein expression of adipogenic transcription factors, and AMP-activated protein kinase (AMPK) phosphorylation were measured. Lipid accumulationdetermined by Oil Red O staining, western blotting, and real-time PCR. The Chemical components of CHEE were analyzed by ultra-performance liquid chromatography coupled with a diode array detector (UPLC-DAD). CHEE inhibited lipid accumulation in 3T3-L1 cells in a dose-dependent manner without showing cytotoxicity up to 200 μg/mL with approximately 45% reduction at 200 μg/mL (p<0.01). CHEE significantly decreased the protein and mRNA expression of peroxisome proliferator-activated receptor gamma (PPARγ), CCAAT/enhancer-binding protein alpha (C/EBPα), CCAAT/enhancer-binding protein beta (C/EBPβ), and CCAAT/enhancer-binding protein delta (C/EBPδ). Additionally, CHEE treatment significantly increased phospho-AMPK levels, and UPLC analysis revealed that CHEE contained 18.25 mg/g of ferulic acid. This study demonstrated that CHEE suppresses 3T3-L1 preadipocyte differentiation by inhibiting the expression of PPARγ and C/EBPα through AMPK activation. These results suggest that the ethanol extract of Cimicifuga heracleifolia Kom. has potential for development as a therapeutic agent for obesity and metabolic diseases, mediated through AMPK-related signaling pathways. The anti-obesity activity of CHEE appears to result from multiple bioactive components working synergistically. Further study using AMPK inhibitors and component-specific analysis will be needed to elucidate the precise mechanism of action.
Keywords:
obesity, Cimicifuga heracleifolia, adipogenesis, AMPK, PPARγ서 론
비만은 에너지 섭취가 에너지 소비를 초과할 때 발생하는 전 세계적 건강문제로, 과도한 체중증가와 지방량 증가를 초래한다. 비만의 유병률은 전 세계적으로 계속 증가하고 있으며, 매년 약 280만 명이 비만 관련 질환으로 사망하고 있다(WHO 2025). 비만은 제2형 당뇨병, 동맥경화증, 고혈압 및 특정암을 포함한 다양한 대사이상 및 건강합병증과 관련이 있다(Thompson D & Wolf AM 2001; Rocha VZ & Libby P 2009; McCarthy MI 2010).
지방세포 분화(adipogenesis)는 전지방세포(preadipocytes)가 성숙지방세포(mature adipocytes)로 분화되는 복잡한 과정으로, 전사인자 및 신호전달 경로에 의해 조절된다. 분화 단계에서 다양한 전사인자들인 CCAAT/enhancer-binding proteins(C/EBPs)가 발현되는데 초기 단계에서는 C/EBPβ와 C/EBPδ는 C/EBPα와 peroxisome proliferator-activated receptorγ(PPARγ)의 발현을 유도하며, 이들은 지방생성 및 지질축적과 관련된 유전자의 전사를 조절한다(Yeh WC 1995; Ahmad B 등 2020). 특히 PPARγ와 C/EBPα는 지방세포 분화의 핵심조절인자이며, 이들이 서로 협력하여 지방세포의 기능을 조절한다(Rosen ED 등 1999; 2002). 이러한 전사인자들은 협력하여 지방산합성효소(fatty acid synthase, FAS) 및 스테롤조절원소결합단백질-1c(sterol regulatory element-binding protein-1c, SREBP-1c)와 같은 지방세포 특이유전자의 발현을 촉진하며, 이는 지방세포 발달에 필수적이다(Morrison RF & Farmer SR 2000).
AMPK는 세포에너지 항상성의 중추적 조절자로, 에너지 대사에서 중심적 역할을 한다(Carling D 2004). AMPK가 활성화되면 acetyl-CoA carboxylase(ACC)를 인산화하여 acetyl-CoA에서 malonyl-CoA로의 전환을 억제하고 지방산 합성을 감소시킨다(Ahmad B 등 2020). 최근 연구에 따르면 AMPK의 활성화는 특히 전지방세포 분화의 초기단계에서 C/EBPα와 PPARγ의 발현을 억제하여 지방생성을 저해한다(Pollard AE 2024). 따라서 AMPK는 비만 예방 및 치료를 위한 유망한 치료 표적이다(Hwang JT 등 2005; Ceddia RB 2013).
전통의약식물에서 유래한 천연물이 잠재적 항비만 제제로 점증하는 관심을 받고 있다(Shaik Mohamed Sayed UF 등 2023). Cimicifuga heracleifolia Kom.은 전통한약에서 ‘승마(升麻)’로 불리며 항염증, 진통 및 해열 특성으로 사용되어 왔다(De Smet 2002; Jang JY 등 2008). 식물화학분석에 따르면 Cimicifuga 속 식물에서 약 348개의 화합물이 확인되었으며, 여기에는 triterpene saponins, phenylpropanoids, chromones 및 flavonoids가 포함된다(Zhang Q 등 2024). 이러한 생물 활성 성분들은 항염증, 항종양, 항산화 및 신경 보호 효과를 포함한 다양한 약리 활성을 나타내고 있다(He K 등 2006; Jang JY 등 2008).
식물체에 존재하는 다양한 폴리페놀류는 특히 항비만 효과를 보유하며 AMPK 신호전달 경로를 통해 지방세포분화를 억제한다는 보고가 있다(Huang B 등 2011; Kim YH & Lee JS 2015; He L 등 2024). 여러 선행 연구에 따르면 폴리페놀류는 AMPK 신호전달 경로를 조절함으로써 지방세포 분화를 억제하고 우수한 항비만 효과를 나타내는 것으로 보고된 바 있다(Huang B 등 2011; Kim YH & Lee JS 2015; Zhao J 등 2024). 천연물 유래 화합물의 항비만 메커니즘과 관련하여, 특히 페룰산(ferulic acid)을 포함한 페놀 화합물들이 AMPK 활성화를 유도하여 지방 축적을 억제한다는 사실이 규명되었으며(de Melo TS 등 2017), 이러한 천연 화합물들은 비만 관리를 위한 다양한 분자적 대안을 제시하고 있다(Li M 등 2025). 또한 찔레꽃(Rosa multiflora) 등 다양한 식물 자원들이 AMPK 경로를 경유하여 항비만 활성을 나타낸다는 연구 결과가 축적되고 있다(Kim YH & Lee JS 2015). 그러나 Cimicifuga heracleifolia Kom.의 항비만 효과 및 지방세포 분화에 대한 작용 메커니즘은 거의 규명되지 않았다. 본 연구는 Cimicifuga heracleifolia Kom. 에탄올 추출물(CHEE)이 3T3-L1 전지방세포의 지방세포분화에 미치는 억제효과를 조사하며, AMPK 신호전달 경로와 PPARγ 및 C/EBPα와의 상호작용에 중점을 두었다. 본 연구에서는 CHEE가 AMPK 활성화를 통해 지방세포 분화를 억제하고, PPARγ와 C/EBPα의 발현을 감소시켜 궁극적으로 지질 축적을 감소시킬 것으로 사료된다.
재료 및 방법
1. 실험 재료
실험의 주 재료인 Cimicifuga heracleifolia Kom.은 옴니허브(Daegu, Korea)에서 구입하였다. 대부분의 시약은 Sigma-Aldrich Co.(St. Louis, MO, USA)에서 구입하였으나, 3T3-L1 전지방세포주는 ATCC(Rockville, MD, USA)에서 구입하였다(CL-173). 세포실험에 관련된 Dulbecco’s modified Eagle’s medium(DMEM), fetal bovine serum(FBS), bovine calf serum(BCS), 페니실린은 LONZA Co.(Basel, Switzerland)에서 구입하였고, PCR에서 활용되는 lysis buffer는 iNtRON Biotech Co.(Daejeon, Korea)에서 구입하였다. Western blot에 활용되는 polyinylidene fluoride(PVDF) membrane과 chemiluminescence enhanced chemiluminescence(ECL) detection kit는 Amersham Pharmacia Biotech Co.(Piscataway, NJ, USA)에서 구입하였고, PCR과 Western blot에 활용되는 antibody의 경우 anti-PPARγ(sc-7273)와 anti-C/EBPα(sc-166258) 항체는 Santa Cruz Biotech. Inc.(CA, USA)에서 구입하였다. 마지막으로 rabbit anti-goat IgG와 rabbit anti-mouse IgG는 Enzo Co.(Farmingdale, NY, USA)에서 구입하였다.
Cimicifuga heracleifolia Kom. 100 g을 70% 에탄올 및 증류수로 각각 80℃와 100℃에서 2시간 동안 mantle-reflux 추출기를 사용하여 추출하였다. 이후 여과한 용매를 감압 농축하여 분말 형태의 에탄올 추출물(CHEE)과 증류수 추출물(CHDW)을 얻었다. 각 용매는 회전 진공 농축기(EYELA, Tyoko, Japan)에서 60℃에서 농축하였으며, —70℃에서 급속냉동 후 동결건조기(FDU-8608, Operon, Kimpo, Korea)를 통하여 건조를 진행하였다. 최종적으로 Cimicifuga heracleifolia 추출물 분말을 dimethyl sulfoxide(DMSO)에 용해하여 실험에 사용하였다.
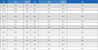
Ultra-performance liquid chromatography coupled with diode array detector(UPLC) (ACQUITY UPLC I-Class PLUS, Waters Corp., Milford, USA) 시스템은 vacuum degasser, quaternary pump, automatic sample injection system으로 구성되었다. 크로마토그래피 분리는 ACQUITY UPLC BEH C18(2.1 × 50 mm, 1.7 μm, Waters Corp., Milford, USA) 칼럼을 사용하여 수행하였으며, photodiode array detector를 320 nm에서 설정하였다. 칼럼 오븐 온도는 35℃, 주입량은 1 μL였다. 이동상은 0.1% formic acid in distilled water(A)와 acetonitrile(B)를 사용하여 0.30 mL/min의 유량으로 용리하였으며 세부 내용은 Table 1에 표기하였다.
3T3-L1 preadipocytes(5 × 103 cells/well)를 96-well plate에 분주하고 24시간 동안 안정화하였다. 이후 CH 추출물을 8, 40, 200 μg/mL의 농도로 처리하였으며, 8일간의 분화 유도 기간 동안 2일마다 시료가 포함된 신선한 배지로 교체하였다. 실험 종료일(day 8)에 배지를 제거하고 PBS에 용해된 MTT solution(5 mg/mL stock)을 serum-free 배지에 희석하여 최종 농도가 250 μg/mL가 되도록 각 well에 100 μL씩 첨가하였다. 37℃, 5% CO2 배양기 내에서 4시간 동안 반응시켜 formazan 형성을 유도한 후, 상층액을 완전히 제거하였다. 생성된 formazan 결정을 용해하기 위해 150 μL의 DMSO를 첨가하고 10분간 교반하였다. 최종 흡광도는 microplate reader(VersaMax, Molecular Device, Califonia, USA)를 사용하여 540 nm에서 측정하였으며, 세포 생존도는 시료를 처리하지 않은 대조군에 대한 상대적인 백분율(%)로 산출하였다.
3T3-L1 전지방 세포는 DMEM(2 mM L-glutamine, 1% penicillin-streptomycin, 10% FBS)에 배양하였고, 37℃, 5% CO₂ 습윤 배양기(Thermo 311 Co2 incubator, Thermo, Waltham, USA)에서 유지하였다. 지방세포 분화를 위해 3T3-L1 전지방 세포를 48-well plate 또는 10 cm dish에 접종한 후 위와 같은 조건에서 배양하였다. Confluency 도달 2일 후(0일)를 기준으로, 세포를 분화 배지(1 μM insulin, 0.5 mM 3-isobutyl-1-methylxanthine(IBMX), 5 μM dexamethasone in DMEM+10% FBS+1% penicillin)에서 2일간 배양하였다. 그 후 배지를 insulin이 함유된 배지(DMEM+10% FBS+1% penicillin)로 교체하여 2일간 더 배양하였다. 4일 후 배지를 DMEM으로 교체하였으며, 8일째 지질 축적 및 세포 생존도와 Oil Red O 염색을 측정하였다.
지방 축적 정도를 측정하기 위해 분화가 완료된 8일차 세포의 배지를 제거하고 PBS로 2회 세척하였고, 세포는 10% Formalin을 사용하여 상온에서 1시간 동안 고정하였다. Oil Red O working solution은 0.5% ORO stock solution(in isopropanol)과 증류수를 3:2 비율(v/v)로 혼합한 뒤 20분간 상온에서 방치하였으며, 사용 직전 0.45 μm syringe filter(Lab co, Gwangju, Korea)로 여과하여 불용성 침전물을 제거하였다. 고정된 세포를 60% isopropanol로 1회 세척 하여 수분을 제거한 뒤, 준비된 ORO working solution을 분주하여 상온에서 30분간 염색하였다. 염색 후 비특이적으로 결합한 염료를 제거하기 위해 증류수로 3회 반복 세척하였으며, 세포에 축적된 ORO를 100% isopropanol 200 μL를 가하여 10분간 용해시킨 뒤, microplate reader를 사용하여 490 nm에서 흡광도를 측정하였다. 지질 축적률은 시료를 처리하지 않은 대조군(control)의 흡광도를 100%로 하여 상대적인 값으로 계산하였다.
CH 추출물이 3T3-L1 지방세포 내 주요 단백질 발현에 미치는 영향을 확인하기 위해 다음과 같이 Western blot을 수행하였다. 세포를 차가운 PBS로 2회 세척하여 잔여 배지를 제거한 후, 단백질 가수분해 효소 저해제(protease inhibitor)와 인산화 저해제(phosphatase inhibitor)가 포함된 lysis buffer(iNtRON Biotech, Seongnam, Korea)를 첨가하였다. 얼음 위에서 30분간 반응시켜 세포를 완전히 균질화한 뒤, 4℃에서 17,000 rpm으로 10분간 원심분리하여 불용성 단백질을 제외한 상층액만을 회수하였다. 단백질 농도는 Bio-Rad protein assay reagent(Bio-Rad, Hercules, CA, USA)를 이용한 Bradford 법으로 정량하였으며, bovine serum albumin(BSA)을 표준물질로 사용하였다.
정량된 단백질 25 μg에 5X Laemmli sample buffer를 혼합하고 95℃에서 5분간 가열하여 단백질을 변성시켰다. 이를 12% sodium dodecyl sulfate polyacrylamide gel electrophoresis(SDS-PAGE) gel에 loading하여 전기영동으로 크기별로 분리한 후, wet transfer 방식을 통해 PVDF membrane으로 2시간 동안 전이시켰다. 비특이적 반응을 차단하기 위해 5% skim milk가 포함된 TBST(Tris-buffered saline with 0.1% Tween 20) 용액에서 상온에서 2시간 동안 blocking 과정을 거쳤다.
일차 항체인 PPARγ, C/EBPα, FAS, phospho-AMPK 및 β-actin은 TBST에 1:2,000 비율로 희석하여 4℃에서 하룻밤(overnight) 동안 반응시켰다. 이후 TBST로 10분씩 3회 반복 세척하여 비특이적으로 결합한 항체를 제거하고, 5% skim milk가 포함된 TBST에 1:5,000으로 희석된 HRP-conjugated secondary antibody(goat anti-mouse IgG 또는 goat anti-rabbit IgG)를 가하여 상온에서 1시간 동안 반응시켰다. 다시 TBST로 3회 세척한 membrane은 ECL reagent(ELPIS)로 반응시킨 뒤, 이미징시스템(Fluor Cheme E image analysis system, Cell biosciences, California, USA)을 사용하여 밴드 신호를 검출하였다. 최종적으로 각 단백질의 발현량은 내부 대조군인 β-actin을 기준으로 정규화한 뒤 상대적인 수치로 분석하였다.
CH 추출물이 3T3-L1 지방세포 내 주요 유전자의 mRNA 발현 수준에 미치는 영향을 분석하기 위해 Real-time PCR을 수행하였다. 먼저, 분화가 완료된 세포로부터 QIAzol lysis reagent(QIAZEN Sciences, Maryland, USA)를 사용하여 제조사의 지시에 따라 total RNA를 추출하였다. 추출된 RNA의 순도와 농도는 microplate reader를 사용하여 측정하였으며, 정량된 total RNA를 power cDNA synthesis kit(iNtRON Biotechnology, Seoul, Korea)를 사용하여 first-strand cDNA 합성을 위한 주형으로 사용하였다. 이후 합성된 cDNA를 바탕으로 지방세포 분화 및 지질 대사 관련 주요 인자인 PPARγ, C/EBPα, FAS, SREBP-1c 유전자의 발현량을 분석하였다. 분석에 사용된 각 유전자별 프라이머 염기서열은 Table 2에 상세히 제시하였다. Real-time PCR 반응은 SYBR Green Power Master Mix(Applied Biosystems, Foster City, CA, USA)와 Step One Plus Real-Time PCR System(Applied Biosystems, Foster City, CA, USA)을 사용하여 수행하였다. 반응 조건은 제조사의 프로토콜에 따라 수행되었으며, 각 유전자의 상대적인 발현량은 내부 표준 유전자인 GAPDH를 대조군으로 하여 2-ΔΔct 방법을 통해 산출하였다. 모든 데이터는 시료를 처리하지 않은 대조군에 대한 상대적인 배수(fold change)로 나타내어 분석의 객관성을 확보하였다.
본 연구의 모든 실험 결과는 3회 이상의 독립적인 반복 실험을 통해 얻어졌으며, 측정값은 평균 표준편차(mean±S.D.)로 표시하였며, 각 실험 결과에 대한 통계 분석은 SPSS(Statistical Package for the Social Sciences, ver. 20.0, IBM, Armonk, NY, USA) 프로그램을 사용하여 수행하였다.
대조군과 각 실험군 간의 통계적 유의성 및 두 그룹 간의 평균 차이는 Student’s t-test를 통해 검증하였으며, 통계적 유의성은 p-value가 0.5 미만(* p<0.05) 또는 0.01 미만(** p<0.01)인 경우를 기준으로 판정하여 분석의 신뢰도를 확보하였다.
결과 및 고찰
1. 3T3-L1 전지방세포에 대한 CHDW와 CHEE의 세포 생존
MTT assay를 통해 CHDW와 CHEE의 세포독성을 평가한 결과, 200 μg/mL까지의 추출물 농도에서 전지방세포의 생존도에 유의한 세포독성이 관찰되지 않았다. 따라서 모든 후속 실험에서 8∼200 μg/mL의 농도범위를 사용하였다. 이는 CHEE가 세포 독성 없이 지방세포 분화 억제 효과가 있음을 의미한다(Fig. 1).
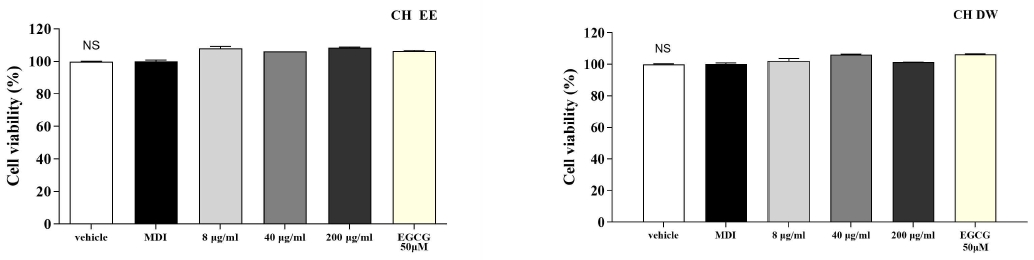
Effect of extracts from Cimicifuga heracleifolia Kom. on cell viability in preadipocytes.1) NS: Non-significant between groups as determined by Duncan’s multiple range test.2) MDI: 3-Isobutyl-1-methylxanthine, dexamethasone, insulin mix (control).3) EGCG: Epigallocatechin-3-gallate (positive control).4) CHDW: Cimicifuga heracleifolia Kom. distilled water extract.5) CHEE: Cimicifuga heracleifolia Kom. ethanol extract.
2. CHDW와 CHEE의 3T3-L1 전지방세포의 지질 축적에 미치는 영향
Oil Red O 염색을 통해 지질축적을 측정한 결과, CHEE 처리는 CHDW 처리보다 훨씬 더 강력한 항비만 효과를 나타냈다. CHEE 200 μg/mL 처리 시 지질 축적이 약 45% 감소하였으나, CHDW 200 μg/mL 처리 시에는 유의한 억제 효과가 관찰되지 않았다. 이는 에탄올 추출물(CHEE)에 높은 농도의 ferulic acid(18.25 mg/g) 및 기타 극성 활성 성분(triterpene saponins 등)이 더 높은 농도로 함유되어 있으며, 이들 성분의 AMPK 활성화 능력이 CHEE의 항비만 효과의 주된 원동력임을 시사한다(Fig. 2).
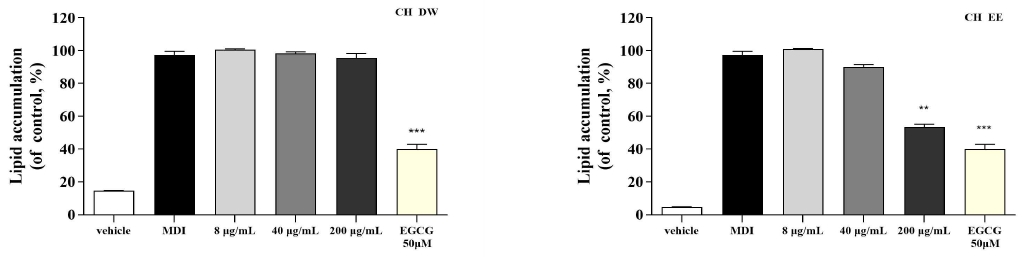
Effects of Cimicifuga heracleifolia Kom. extracts on lipid accumulation in 3T3-L1 adipocytes.1) MDI: 3-Isobutyl-1-methylxanthine, dexamethasone, insulin mix (control)2) EGCG: Epigallocatechin-3-gallate (positive control)3) CHDW: Cimicifuga heracleifolia Kom. distilled water extracts.4) CHEE: Cimicifuga heracleifolia Kom. ethanol extracts.5) Statistical differences among groups were determined by Duncan’s multiple range test (** p<0.01, *** p<0.001 vs control).
따라서 본 연구의 이후 실험(western blot, real-time PCR)은 모두 CHEE를 사용하여 수행하였다.
3. CHEE의 화학 성분 분석
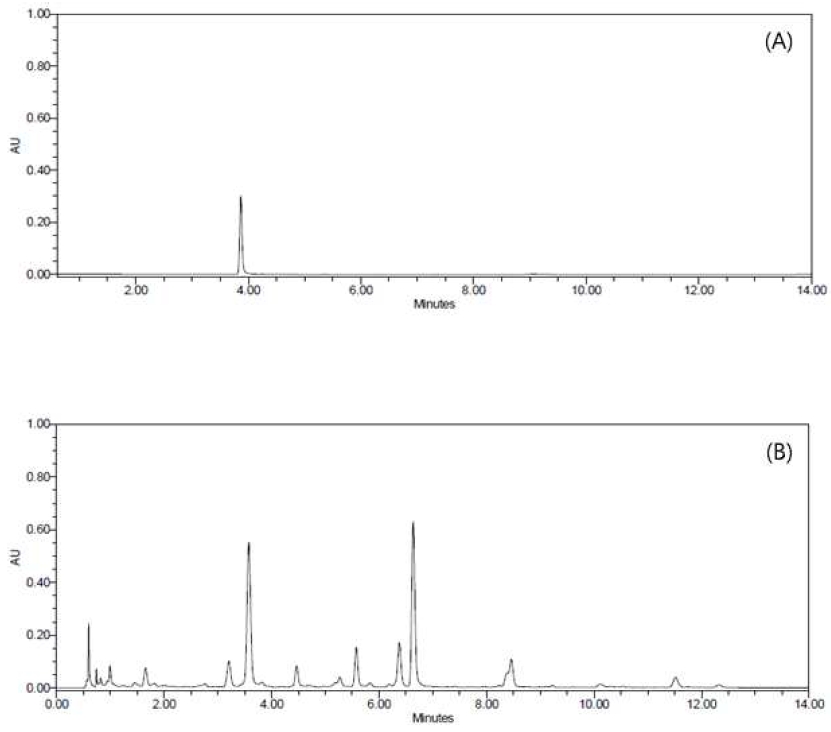
UPLC-DAD를 사용하여 CHEE의 화학 성분을 분석한 결과, ferulic acid는 약 3.90분의 retention time에서 확인되었으며, 18.25 mg/g 함유된 것으로 측정되었다. ferulic acid는 Cimicifuga 속 식물의 주요 마커 화합물이라고 볼 수는 없다. 하지만 지방 축적과 관련된 선행 연구에서 AMPK 신호전달을 직접 활성화하고 항비만 효과를 나타내는 것이 입증되었다(de Melo TS 등 2017; DiNicolantonio JJ 등 2022; Wu H 등 2024). 본 연구에서 CHEE에 함유된 ferulic acid(18.25 mg/g)를 정량한 것은, CHEE의 AMPK 활성화 능력을 평가하기 위한 지표로서의 의미가 있다. 다만, CHEE의 항비만 효과가 ferulic acid 단일 성분에만 기인한다고 보기는 어렵다. Cimicifuga heracleifolia Kom.에는 약 348개의 화합물이 함유되어 있으며, 특히 triterpene saponins과 cimigenol glycosides가 핵심 생리활성 성분으로 알려져 있다(Zhang Q 등 2024). 따라서 CHEE의 항비만 활성은 ferulic acid, triterpene saponins, cimigenol glycosides 등 다양한 활성 성분들의 상승작용을 통해 나타날 가능성이 높다(Fig. 3).
4. CHEE의 3T3-L1 세포에서 지방생성 관련 전사인자의 단백질 발현에 미치는 영향
3T3-L1 지방세포 분화 과정에서 CHEE가 지방생성 조절 메커니즘에 미치는 영향을 검토하기 위해, 핵심 전사인자 및 AMPK의 단백질 발현 수준을 Western blot으로 분석하였다.
먼저 지방세포 분화의 중추적인 역할을 하는 전사인자의 변화를 관찰한 결과, CHEE 처리는 PPARγ, C/EBPα, C/EBPβ, C/EBPδ 및 FAS의 단백질 발현을 농도 의존적으로 유의하게 감소시켰다. 특히, 지방세포 분화 후기 단계에서 지질 축적을 직접 담당하는 효소인 FAS의 발현은 CHEE 200 μg/mL 처리 시 대조군 대비 약 58% 감소하며 강력한 지방생성억제 효과를 나타냈다. 일반적으로 지방세포 분화 초기 단계에서 C/EBPβ와 C/EBPδ가 C/EBPα의 발현을 유도하고, 이는 다시 PPARγ를 활성화하여 지방생성 유전자의 발현을 촉진한다(Yeh WC 등 1995; Rosen ED 등 1999; 2002). 본 연구에서 CHEE는 초기(C/EBPβ, δ)와 후기(PPARγ, C/EBPα) 전사인자를 모두 억제하였으며, 특히 마스터 조절자인 PPARγ와 C/EBPα의 감소가 두드러졌다. 이는 CHEE가 분화 경로의 핵심 단계들을 효과적으로 차단함을 시사한다.
이러한 전사인자 억제의 상위 신호 전달 경로를 확인하기 위해 AMPK의 인산화 수준을 측정한 결과, CHEE 처리는 phospho-AMPK(p-AMPK) 수준을 농도 의존적으로 유의하게 증가시켰다. 특히 CHEE 200 μg/mL 농도에서 p-AMPK 발현이 가장 현저하게 증가하였다. 에너지 센서로 작용하는 AMPK의 활성화는 세포 내 에너지 항상성을 유지하며 지방산 합성을 억제하는 핵심 기전으로 알려져 있다(Carling D 2004; Pollard AE 2024). 선행 연구에 따르면, 활성화된 AMPK는 지방세포 분화 초기 단계에서 C/EBPα와 PPARγ의 발현을 직접적으로 억제하여 지방 생성을 차단할 수 있다(Hwang JT 등 2005; Gormand A 등 2011). 이러한 결과를 토대로 CHEE는 AMPK 활성화를 유도함으로써 PPARγ와 C/EBPα 등 핵심 전사인자의 발현을 억제하고, 결과적으로 FAS와 같은 지질 축적 효소를 감소시켜 지방세포 분화를 저해하는 것으로 판단된다. 이는 AMPK 활성을 통해 항비만 효과를 나타내는 천연물 유래 성분들의 작용 기전과 일맥상통하는 결과이다(Huang B 등 2011; He L 등 2024) (Fig. 4).
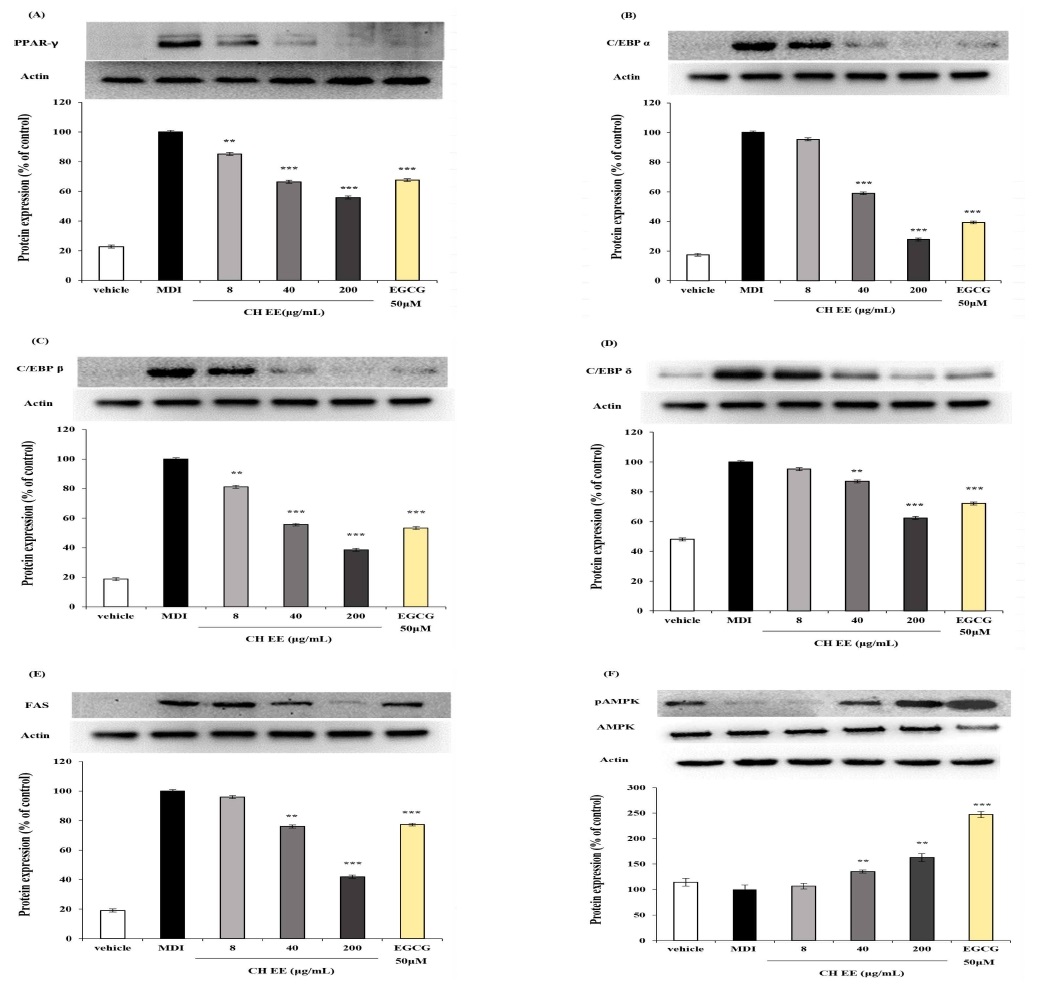
Effects of Cimicifuga heracleifolia Kom. ethanol extracts (CHEE) on protein expression of adipogenic transcription factors in 3T3-L1 cells.1) Protein expression levels of (A) PPARγ, (B) C/EBPα, (C) C/EBPβ, (D) C/EBPδ, (E) FAS, and (F) p-AMPK were determined by western blot analysis.2) Actin was used as a loading control.3) Values are expressed as a percentage of the MDI-induced control.4) MDI: 3-Isobutyl-1-methylxanthine, dexamethasone, insulin mix (control)5) EGCG: Epigallocatechin-3-gallate (positive control)6) Statistical differences among groups were determined by Duncan’s multiple range test (** p<0.01, *** p<0.001 vs control).
5. CHEE의 3T3-L1 세포에서 지방생성 관련 유전자 발현에 미치는 영향
Real-time PCR을 통해 지방생성 관련 유전자의 mRNA 발현수준을 측정한 결과, CHEE 처리는 용량의존적으로 PPARγ, C/EBPα, FAS 및 SREBP-1c의 mRNA 발현을 감소시켰다. 특히 CHEE 200 μg/mL 처리 시 PPARγ와 C/EBPα의 mRNA 발현은 대조군 대비 유의하게 감소하였으며, FAS와 SREBP-1c의 mRNA 발현 또한 유의하게 감소하였다.
본 연구의 결과들을 종합하여 봤을 때 다음과 같은 메커니즘을 전달한다. CHEE는 AMPK를 활성화하고, 활성화된 AMPK는 지방세포 분화의 초기 단계 전사인자인 C/EBPα와 PPARγ의 발현을 억제하며, 이는 궁극적으로 FAS와 SREBP-1c의 발현감소 및 지질 축적 억제로 이어진다(Rosen ED 등 1999; 2002; Ahmad B 등 2020; Pollard AE 2024).
이러한 AMPK 신호전달 경로를 통한 항비만 메커니즘은 최근의 천연물 연구에서도 강조되고 있으며(He L 등 2024; Li M 등 2025), 페룰산과 같은 폴리페놀류의 항비만 활성과도 일치한다(de Melo TS 등 2017; He L 등 2024). 나아가 본 연구의 결과는 비만 관리를 위한 천연소재의 적용 가능성을 시사하며, 승마의 과학적 검증을 통해 임상적 활용 가치를 재입증하는 것으로 볼 수 있다(Fig. 5).
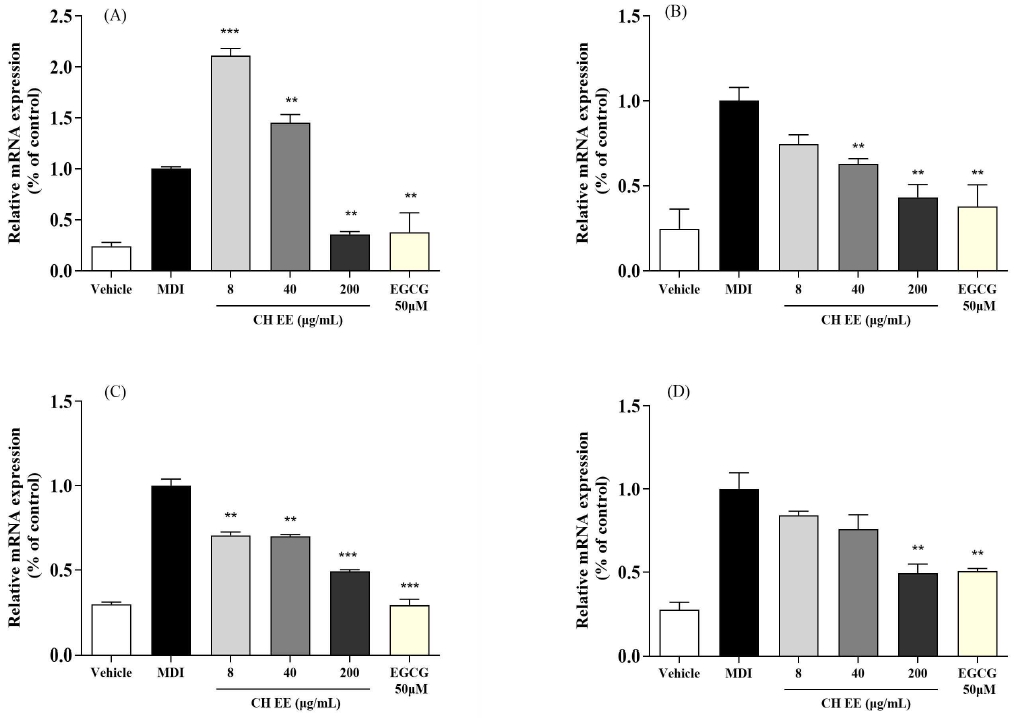
Effects of Cimicifuga heracleifolia Kom. ehanol extracts (CHEE) on the relative mRNA expression in 3T3-L1 adipocytes.1) mRNA levels of (A) PPARγ, (B) C/EBPα, (C) FAS, and (D) SREBP-1c were determined by real-time PCR.2) MDI: 3-Isobutyl-1-methylxanthine, dexamethasone, insulin mix (control)3) EGCG: Epigallocatechin-3-gallate (positive control)4) Statistical differences among groups were determined by Duncan’s multiple range test (** p<0.01, *** p<0.001 vs control).
결 론
본 연구는 승마(Cimicifuga heracleifolia Kom.) 에탄올 추출물(CHEE)의 항비만 기전을 규명하기 위해 진행되었다. 특히 페룰산(ferulic acid)이 AMPK 활성을 유도하고 AMPK는 지방 축적을 억제한다는 선행 연구 결과에 근거하여 페룰산을 CHEE의 지표 물질로 선정하고 연구를 설계하였다. 그 결과, CHEE는 세포 독성 없이 지방 축적률을 대조군 대비 약 45% 유의하게 억제하였으며, 이는 선행 연구 보고와 일치하며, CHEE가 AMPK의 인산화를 촉진함으로써 지방세포 분화를 효과적으로 조절함을 확인할 수 있었다.
구체적으로 CHEE는 분화 초기의 C/EBPβ, C/EBPδ를 억제하여 지질 축적의 핵심 전사인자인 PPARγ, C/EBPα의 단백질 및 mRNA 발현을 농도 의존적으로 억제하였으며, 지질 합성 효소인 FAS와 SREBP-1c의 발현을 하향 조절하여 지질 축적을 차단하였다.
이러한 성과는 CHEE가 페룰산을 포함한 활성 성분들을 통해 AMPK 신호전달 경로를 활성화하고 지방 생성을 억제하는 천연 기능성 소재로서의 가능성을 보여준다. 하지만, 본 연구는 페룰산 외에 승마의 또 다른 주요 활성 성분들에 대한 개별적인 정량 분석이나 효능 평가를 수행하지 못했다는 점, 그리고 AMPK 억제제를 통한 직접적인 인과관계 검증까지는 나아가지 못했다는 한계가 있다고 볼 수 있다.
따라서 향후 연구에서는 승마의 triterpene saponins 및 cimigenol glycosides에 대한 정량 분석과 각 개별 성분의 AMPK 활성화 능력을 평가할 필요가 있으며, 더불어 AMPK inhibitor를 이용한 억제 실험을 통해 신호전달 경로의 명확한 인과관계를 확립함으로써, 승마 추출물을 체중 관리 및 대사 질환 예방을 위한 소재로 개발하기 위한 심도 있는 보완 연구가 수행되어야 할 것으로 사료된다.
Acknowledgments
이 논문은 2024학년도 세명대학교 교내학술연구비 지원에 의해 수행된 연구임.
References
-
Ahmad B, Serpell CJ, Fong IL, Wong EH (2020) Molecular mechanisms of adipogenesis: The anti-adipogenic role of AMP-activated protein kinase. Front Mol Biosci 7: 76.
[https://doi.org/10.3389/fmolb.2020.00076]

-
Carling D (2004) The AMP-activated protein kinase cascade: A unifying system for energy control. Trends Biochem Sci 29(1): 18-24.
[https://doi.org/10.1016/j.tibs.2003.11.005]

-
Ceddia RB (2013) The role of AMP-activated protein kinase in regulating white adipose tissue metabolism. Mol Cell Endocrinol 366(2): 194-203.
[https://doi.org/10.1016/j.mce.2012.06.014]

-
de Melo TS, Lima PR, Carvalho KM, Fontenele TM, Solon FR, Tomé AR, de Lemos TL, da Cruz Fonseca SG, Santos FA, Rao VS, de Queiroz MG (2017) Ferulic acid lowers body weight and visceral fat accumulation via modulation of enzymatic, hormonal and inflammatory changes in a mouse model of high-fat diet-induced obesity. Braz J Med Biol Res 50(1): e5630.
[https://doi.org/10.1590/1414-431x20165630]

-
De Smet PA (2002) Herbal remedies. N Engl J Med 347(25): 2046-2056.
[https://doi.org/10.1056/NEJMra020398]

-
DiNicolantonio JJ, McCarty MF, Assanga SI, Lujan LL, O’Keefe JH (2022) Ferulic acid and berberine, via Sirt1 and AMPK, may act as cell cleansing promoters of healthy longevity. Open Heart 9(1): e001801.
[https://doi.org/10.1136/openhrt-2021-001801]

-
McCarthy MI (2010) Genomics, Type 2 diabetes, and obesity. N Engl J Med 363(24): 2339-2350.
[https://doi.org/10.1056/NEJMra0906948]

-
Gormand A, Henriksson E, Ström K, Jensen TE, Sakamoto K, Göransson O (2011) Regulation of AMP-activated protein kinase by LKB1 and CaMKK in adipocytes. J Cell Biochem 112(5): 1364-1375.
[https://doi.org/10.1002/jcb.23053]

-
He K, Pauli GF, Zheng B, Wang H, Bai N, Peng T, Roller M, Zheng Q (2006) Cimicifuga species identification by high performance liquid chromatography-photodiode array-mass spectrometric-evaporative light scattering detection for quality control of black cohosh products. J Chromatogr A 1112(1-2): 241-254.
[https://doi.org/10.1016/j.chroma.2006.01.004]

-
He L, Su Z, Wang S (2024) The anti-obesity effects of polyphenols: A comprehensive review of molecular mechanisms and signal pathways in regulating adipocytes. Front Nutr 11: 1393575.
[https://doi.org/10.3389/fnut.2024.1393575]

-
Huang B, Yuan HD, Kim DY, Quan HY, Chung SH (2011) Cinnamaldehyde prevents adipocyte differentiation and adipogenesis via regulation of peroxisome proliferator-activated receptor-γ (PPARγ) and AMP-activated protein kinase (AMPK) pathways. J Agric Food Chem 59(8): 3666-3673.
[https://doi.org/10.1021/jf104814t]

-
Hwang JT, Park IJ, Shin JI, Lee YK, Lee SK, Baik HW, Ha J, Park OJ (2005) Genistein, EGCG, and capsaicin inhibit adipocyte differentiation process via activating AMP-activated protein kinase. Biochem Biophys Res Commun 338(2): 694-699.
[https://doi.org/10.1016/j.bbrc.2005.09.195]

-
Jang JY, Lee JH, Kang BW, Chung KT, Choi YH, Choi BT (2008) Dichloromethane fraction of Cimicifuga heracleifolia decreases the level of melanin synthesis by activating the ERK or AKT signaling pathway in B16F10 cells. Exp Dermatol 18(3): 232-237.
[https://doi.org/10.1111/j.1600-0625.2008.00794.x]

-
Kim Y, Lee J (2015) Esculetin, a coumarin derivative, suppresses adipogenesis through modulation of the AMPK pathway in 3T3-L1 adipocytes. J Funct Foods 12: 509-515.
[https://doi.org/10.1016/j.jff.2014.12.004]

-
Li M, Ding L, Cao L, Zhang Z, Li X, Li Z, Xia Q, Yin K, Song S, Wang Z, Du H, Zhao D, Li X, Wang Z (2025) Natural products targeting AMPK signaling pathway therapy, diabetes mellitus and its complications. Front Pharmacol 16: 1534634.
[https://doi.org/10.3389/fphar.2025.1534634]

-
Morrison RF, Farmer SR (2000) Hormonal signaling and transcriptional control of adipocyte differentiation. J Nutr 130(12): 3116S-3121S.
[https://doi.org/10.1093/jn/130.12.3116S]

-
Pollard AE (2024) New concepts in the roles of AMPK in adipocyte stem cell biology. Essays Biochem 68(3): 349-361.
[https://doi.org/10.1042/EBC20240008]

-
Rocha VZ, Libby P (2009) Obesity, inflammation, and atherosclerosis. Nat Rev Cardiol 6(6): 399-409.
[https://doi.org/10.1038/nrcardio.2009.55]

-
Rosen ED, Hsu CH, Wang X, Sakai S, Freeman MW, Gonzalez FJ, Spiegelman BM (2002) C/EBPα induces adipogenesis through PPARγ: A unified pathway. Genes Dev 16(1): 22-26.
[https://doi.org/10.1101/gad.948702]

-
Rosen ED, Sarraf P, Troy AE, Bradwin G, Moore K, Milstone DS, Spiegelman BM, Mortensen RM (1999) PPARγ is required for the differentiation of adipose tissue in vivo and in vitro. Mol Cell 4(4): 611-617.
[https://doi.org/10.1016/S1097-2765(00)80211-7]

-
Shaik Mohamed Sayed UF, Moshawih S, Goh HP, Kifli N, Gupta G, Singh SK, Chellappan DK, Dua K, Hermansyah A, Ser HL, Ming LC, Goh BH (2023) Natural products as novel anti-obesity agents: Insights into mechanisms of action and potential for therapeutic management. Front Pharmacol 14: 1182937.
[https://doi.org/10.3389/fphar.2023.1182937]

-
Thompson D, Wolf AM (2001) The medical-care cost burden of obesity. Obes Rev 2(3): 189-197.
[https://doi.org/10.1046/j.1467-789x.2001.00037.x]

- World Health Organization (2025) Obesity and Overweight. https://www.who.int., (accessed on 10. 2. 2026).
-
Wu H, Wang Y, Tan P, Ran Y, Guan Y, Qian S, Feng X, Jiang Y, Peng Y, Sheng K, Xi H, Ji W, Guo X (2024) Ferulic acid suppresses inflammation and apoptosis in Kawasaki disease through activating the AMPK/mTOR/NF-κB pathway. Front Pharmacol 15: 1420602.
[https://doi.org/10.3389/fphar.2024.1420602]

-
Yeh WC, Cao Z, Classon M, McKnight SL (1995) Cascade regulation of terminal adipocyte differentiation by three members of the C/EBP family of leucine zipper proteins. Genes Dev 9(2): 168-181.
[https://doi.org/10.1101/gad.9.2.168]

-
Zhao J, Alimu A, Li Y, Lin Z, Li J, Wang X, Wang Y, Lv G, Lin H, Lin Z (2024) Potential anti-obesity effect of hazel leaf extract in mice and network pharmacology of selected polyphenols. Pharmaceuticals 17(10): 1349-1370.
[https://doi.org/10.3390/ph17101349]

-
Zhang Q, Wei W, Jin X, Lu J, Chen S, Ogaji OD, Wang S, Du K, Chang Y, Li J (2024) Traditional uses, phytochemistry, pharmacology, quality control and clinical studies of Cimicifugae Rhizoma: A comprehensive review. Chin Med 19(1): 66.
[https://doi.org/10.1186/s13020-024-00937-7]