당뇨환자용 특수영양조제식품 섭취가 db/db Mice 체내에 미치는 생화학적 효과
 ; Sang Hyun Cheong2
; Sang Hyun Cheong2 ; Chung-Hwa Song3
; Chung-Hwa Song3 ; Yoo-Jin Lee4
; Yoo-Jin Lee4 ; Eun-Chae Cho5
; Eun-Chae Cho5 ; Do-Hui Kim5
; Do-Hui Kim5 ; Won-Joong Lee6
; Won-Joong Lee6 ; Hyo-Jeong Hwang7
; Hyo-Jeong Hwang7 ; Yean-Jung Choi8
; Yean-Jung Choi8 ; Kyung-Ok Shin9, †
; Kyung-Ok Shin9, †
Abstract
A special nutritional formula for diabetic patients, developed by Sahmyook Foods, was administered to db/db mice and compared with the products from other companies. This study examined the effects of different concentrations on diabetic factors. The body weight increased steadily in the normal diet (ND) group, but decreased in the diabetic experimental group. Food intake and food efficiency decreased in all groups, and the liver weight increased. The blood glycated hemoglobin (HbA1c) level was lowest in the diabetic control group and the Sahmyook Diabetic Care Pro 10% (DCSD 10%) group at 1.98±0.09%. The blood insulin concentration was lowest in the DCSD 20% group at 0.27±0.37 ng/dL (p<0.05), while the blood adiponectin secretion and glucose concentration were lowest in the DCSD 10% group (p<0.0001). The liver markers alanine transaminase (ALT), aspartate transaminase (AST), and lactate dehydrogenase (LDH) levels were lowest in the diabetic control group+newcare dangplan 10% (DCGN 10%) group. The DCSD 10% group had higher serum protein levels, while the uric acid levels were lower in the DCSD 10%, DCGN 10%, and diabetic control group+greenbia dang care 10% (DCGG 10%) groups (p<0.0001). The cholesterol and low density lipoprotein cholesterol (LDL-Cholesterol) levels were lower in the experimental group than in the diabetic control group (DCG) group. The DCSD 10% group had higher serum high density lipoprotein cholesterol (HDL-Cholesterol) levels than the DCSD 20%, DCGN 10%, and DCGG 10% groups (p<0.0001). Therefore, special nutritional foods formulated for diabetic patients, which are special-purpose foods, affect various blood diabetic factors. Diabetic patients should consume specially formulated nutritional foods as a meal replacement. In addition, DCSD products, which entered the special nutritionally formulated foods market as a latecomer, are considered competitive products and not inferior to those of other companies.
Keywords:
diabetes, special nutritionally formulated foods, BMI, insulin, adiponectin서 론
당뇨병은 인슐린 결핍 또는 인슐린 저항성에 의해 구분되며, 당이 소변으로 배출되는 질환을 의미한다(Lee HB 등 2021). 당뇨병은 당대사 및 지질대사 전반에 걸쳐 만성적으로 대사상의 혼란을 야기시키는 질병이다(Kim DH 등 2013). 대한당뇨병학회의 ‘Diabetes fact sheet 2021’에 의하면, 당뇨병은 2020년 사망 원인 6위에 해당하는 질환으로서 우리나라 30세 이상 당뇨병 유병률은 2020년 16.7%로 증가 추세를 보이며, 6명 중 1명은 당뇨병을 앓고 있다고 지적하였다(Bae JH 등 2022; Lee HJ 등 2023). 당뇨병은 성인의 만성질환으로 인식되었으나, 최근 젊은 층에서도 제2형 당뇨병이 크게 증가하고 있다(Lee HJ 등 2023). 국제 당뇨병 연맹은 당뇨병 유병자가 2014년 3억 8천 명에서 2035년에는 5억 9천 명으로 증가할 것으로 예측하고 있다(Kang JR 등 2020).
당뇨병은 유전적인 요인에 의한 제1형 당뇨병과 인슐린 수용체의 민감도의 저하로 인한 제2형 당뇨병으로 나뉘는데, 제1형 당뇨병은 췌장 β-세포의 자가면역성 파괴로 인한 인슐린 결핍이 특징이다(Kim YR 등 2022). 전체 당뇨병 환자의 90% 이상이 제2형 당뇨병에 해당하며, 제 2형 당뇨병은 비만, 스트레스, 신체활동 부족, 영양과잉 섭취 및 체력 저하 등에 의한 복합적인 원인들에 의해 발병된다(Kim SH 2019). 당뇨병은 초기에 증상이 없어 진단이 쉽지 않으며, 추후에 당뇨병 진단이 되었다 하더라도 치료의 필요성을 인지하지 못하는 경우가 많다(Lee HJ 등 2023). 당뇨병의 만성적인 합병증은 망막변증, 혈액순환 장애, 신장질환 및 심혈관계질환 등의 합병증을 유발하며(Kim SH 2019; Lee HB 등 2021), 합병증이 심하면 사망에 이르기까지 한다.
대한당뇨병학회에서 발표한 당뇨병 진료지침 2014에는 영양요법, 운동요법 및 약물요법을 당뇨병 관리의 3대 원칙으로 제시하고 있다(Kim DH 등 2013). 당뇨병이 장기간 진행된 상태에서는 생활 습관의 개선만으로는 혈중 당화혈색소가 목표치에 도달하기 어렵기 때문에 경구용혈당강하제를 비롯한 인슐린제제 등의 약물치료가 요구된다. 현재 당뇨병의 치료제로써 thiazolidinedion계, sulfonylurea계 및 biguanide계 약물과 인슐린제제들이 활용되고 있지만, 위장장애, 부종, 저혈당, 산혈증, 간독성, 비만 및 심장독성 등의 부작용과 내성 문제점 등이 발생되고 있다(Kim DH 등 2013). 따라서 당뇨병 치료 및 관리를 위해 새로운 방법들이 모색되고 있으며, 부작용이 없는 특수용도 식품(건강기능식품)을 통한 당뇨병 예방 및 관리에 도움을 주고자 많은 연구가 진행되고 있다(Babashahi M 등 2015; Hariri M 등 2015; Chuang YC 등 2019; Babashahi M 등 2020).
최근 제품으로 출시되고 있는 당뇨환자용 특수영양조제식품은 치커리 식이섬유, 아가베 이눌린, 바나나잎 추출물, 돼지감자, 팔라티노스, 난소화성말토덱스트린 및 식이섬유 등의 천연 식물성 기능성 소재를 사용하여 제조되고 있으며, 이러한 성분들이 인슐린 분비에 영향을 준다. 치커리는 셀레늄이나 비타민 C, tocopherol, pyrogallol, catechin, vanilic acid, benzoic acid 등의 페놀성 물질이 많이 함유되어 있어서 높은 항산화 활성을 가지며, 식이섬유가 풍부해 장 기능 개선효과가 있고, 치커리 이눌린과 올리고당으로 인해 당뇨병 개선 및 혈당에 도움을 준다고 보고되었다(Shin S 등 2014; Coi HJ 등 2020). 아가베 이눌린은 전분을 분해하는 ptyalin이나 amylase와 같은 인체 내의 효소로는 분해되지 않고 소화관을 통과하므로 포만감을 주고 혈당을 급격히 올리는 것을 지연시키는 작용이 있다(Kim SH 2014). 바나바잎 추출물의 경우 당분해 효소의 활성을 억제하여, 소장에서의 포도당 흡수를 지연시킴으로써 식후 혈당 상승을 완화하는 효과가 있다고 보고되었다(Judy WV 등 2003; Kim NH 등 2025). 돼지감자에는 이눌린이 풍부하여 당뇨병과 류마티스의 치료를 위한 민간요법으로 사용되어 왔으며, 간으로부터 담즙의 분비를 촉진하며 변비 예방, 이뇨제, 건위제 및 강장제 효과와 같은 다양한 약리 활성을 가지는 것으로 보고되었다(Kim HN 등 2014). 팔라티노스는 설탕의 감미도의 40%에 해당하며, 충치원인균인 Streptococcus mutans로 인한 충치 및 치석은 거의 유발하지 않으며, 설탕을 섭취하는 것에 비하여 식후 포도당 및 인슐린 수준을 감소시킨다고 보고되었다(Kim HK & Kim HW 2023). 난소화성 말토덱스트린은 옥수수 전분을 건식으로 가수분해하여 얻은 식이섬유의 일종으로 식후 혈당 상승 억제, 혈중 중성 지질의 개선 및 변비 예방 등 기능성을 인정받은 원료이다(Kim YS & Cho MS 2020). 또한 식이섬유는 인체의 소화효소에 의하여 분해되지 않는 난분해성의 복합 다당류로서 장내 콜레스테롤이나 담즙산 등을 흡착하여 대변으로 배설을 촉진하며, 당뇨병 예방과의 연관성이 보고되었다(Park MH 등 2011).
따라서 본 연구에서는 천연 식물성 기능성 소재를 첨가한 삼육식품에서 개발된 특수용도식품인 당뇨환자용 특수영양조제식품 및 타사 제품을 db/db mice에게 섭취시킨 후, 농도별로 비교 실험을 통하여 혈중 당뇨병 인자에 미치는 영향을 알아보고자 실시하였다.
연구방법
1. 실험 재료 및 실험 동물
본 실험에서 사용한 시료는 삼육식품에서 개발된 당뇨환자용 특수영양조제식품인 삼육케어 당캐치 프로(Sahmyook Food, Cheonan, Choongchungnam-Do, Korea)를 동결건조시켜 사료 제조에 사용하였다. 또한 대상 뉴케어(Daesang, Seoul, Korea), 정식품 그린비아(Dr. Chung’s Food, Cheongju, Chungcheongbuk-Do, Korea) 제품도 시중 마트에서 구매하여 같은 방법으로 동결건조시켜 사료 제조에 사용하였다. 식이 조성은 Table 1과 같으며, 총 실험 기간(2025년 7월 23일∼2025년 9월 16일) 동안 대조군과 실험군 모두에게 사료와 물을 자유롭게 섭취하도록 공급하였다. 본 연구는 라온바이오(Raonbio, Yongin, Korea)에서 생후 8주령의 수컷 C57BL/6 10마리와 db/db mice 50마리를 분양받았으며, 케이지에 한 마리씩 배치하여 각 처리구 당 6마리씩 총 8주간 사육하였고, 7일의 적응기를 가진 후 실험에 사용하였다. 동물 사육실의 환경은 온도 22±2℃, 습도 50±10%, 12시간 주기의 점등 조건을 유지하였으며, 전체적인 동물 실험 디자인은 Table 2에 제시하였다. 본 연구에 사용한 실험 식이는 ㈜두열바이오텍(DooYeol Biotech, Seoul, Korea)에 의뢰하여 pellet 형태로 주문 제작하였으며, 구체적인 실험군은 정상대조군(C57BL/6; ND: Normal diet), 당뇨대조군(db/db 마우스+일반사료; DCG: Diabetic control group), 저용량 투여군(db/db 마우스+일반사료+당캐치 프로; DCSD 10%: Diabetic control group+Sahmyook diabetic care pro 10%), 고용량 투여군(db/db 마우스+일반사료+당캐치 프로; DCSD 20%: Diabetic control group +Sahmyook diabetic care pro 20%), 비교군 1 투여군(db/db 마우스+일반사료+뉴케어 당플랜; DCGN 10%: Diabetic Control Group+Newcare Dangplan 10%), 비교군 2 투여군(db/db 마우스+일반사료+그린비아 당케어; DCGG 10%: Diabetic Control Group+Greenbia Dang care 10%)으로 나누었다(Table 2). 본 연구는 삼육대학교 동물윤리위원회(Institutional Animal Care and Use Committee)의 승인을 받아 동물 실험을 진행하였으며, 실험에 관한 규정에 따라 수행하였다(SYUIACUC 2025-005).
2. 체중 변화, 식이 섭취량 및 식이 효율 측정
실험 동물의 식이 섭취량은 매일, 쥐의 개별 체중은 주 1회 일정한 시간에 측정하여 기록하였으며, 식이 섭취에 따른 갑작스러운 체중 변화를 방지하기 위해 체중 측정 4시간 전 식이 그릇을 제거한 후에 흰쥐의 체중 증가량을 확인하였다. 식이 효율(feed efficiency ratio)은 체중 증가량(g)을 식이 섭취량(g)으로 나눈 값에 100을 곱하여 계산하였다.
3. 혈액 채취 및 조직 무게 측정
실험 동물의 희생은 경구투여 24시간 후에 진행되었다. 해부 전에 조직 적출을 위해 12시간 동안 절식시킨 실험 동물을 CO2 가스를 사용하여 호흡 마취한 후, 경추 탈골을 실시하여 실험 동물을 희생시켰다. 실험 동물의 복강 해부를 진행하여 심장 박동이 유지되고 있는 상태로 심장에서 혈액을 채취하였다. 채혈한 혈액은 BD Vacutainer® SSTTM 처리가 된 tube에 넣고 실온에서 응고시킨 후, 4℃ 3,000 rpm에서 10분간 원심 분리를 진행한 후에 혈청만 취하여 —80℃ deep freezer에서 냉동 보관하였다. 흰쥐의 조직은 중량 측정을 위해 간, 신장, 비장을 적출하였으며, 생리식염수에 세척하여 전자저울을 사용하여 무게를 측정하였다.
4. 공복 혈당, 경구 내당능 검사(Oral Glucose Tolerance Test, OGTT) 및 당화혈색소 측정
혈당은 Shin MJ 등(2006)이 제시한 방법에 따라 절식 4시간 후 공복 상태에서 꼬리 정맥으로부터 채혈하여 superglucocardⅡ(ARKRAY. Inc., Japan)으로 측정하였다. 경구 내당능 검사는 실험 동물을 16시간 절식시킨 다음 꼬리 정맥에서 채혈하여 공복 시 혈당을 측정한 후, 50% glucose 용액(0.1 g glucose/100 g B.W.)을 intubation tube를 사용하여 경구 투여하고 15, 30, 60, 90, 120분 후 혈당측정기를 이용하여 혈당을 측정하였다. 당화혈색소 측정은 혈청 5 μL를 전용 희석액(1:200)으로 희석한 후, glycohemoglobin analyzer(HLC-723G7, Tosoh, Amsterdam, Netherlands)로 415 nm 흡광도에서 측정하였다.
5. 혈중 인슐린, 아디포넥틴 및 Glucose 변화 측정
혈액 내 인슐린은 ELISA kit(Millipore Co., Missouri, USA)를 이용하여 측정하였으며, 인슐린 농도는 Kwon HO 등(2020)이 제시한 방법에 따라 Rat/Mouse Insulin 96-well plate를 이용하여 실험 protocol에 따라 분석하였다. Adiponectin 단백질은 각각 Nori® Rat adiponectin ELISA Kit(Genorise, USA)를 사용하여 측정하였다. 시료는 분리한 혈청을 사용하였으며, 각 well에 standard, blank, sample을 100 μL씩 duplicate로 첨가하고 sealer를 붙여 실온에서 2시간 동안 배양하였다. 배양 후 washing buffer로 2회 세척하고, working detection antibody를 100 μL 첨가하여 실온에서 2시간 배양한 후 다시 washing buffer로 2회 세척하였다. 그 후 각 well에 Working Streptavidin-HRP 100 μL를 첨가하여 실온에 20분 배양하고, washing buffer로 4번 세척하였다. 그 후 substrate solution 100 μL를 첨가하여 30분간 반응시킨 후, stop solution 50 μL를 첨가하며 반응을 종결시켰다. 반응을 종결시킨 후에는 Multifunction microplate reader(MMR SPARK®, Tecan, Switzerland)를 이용하여 450 nm에서 흡광도를 측정하고, adiponectin 단백질 생성량은 kit 내 adiponectin standard를 사용하여 각각 검량선을 그려 산출하였다. Glucose 농도는 Jung HL & Kang HY(2014)가 제시한 방법에 따라 흰쥐의 꼬리 정맥으로부터 채취한 혈액을 자동혈당분석기 YSI-2300(Yellow Springfield Instruments Co., Yellow Springs, OH, USA)를 이용하여 측정하였다.
6. 혈중 간 기능 지표성분 측정
간 기능 지표성분인 alanine aminotransferase(ALT)와 aspartate aminotransferase(AST) 활성도 측정은 Kang HY 등(2016)의 방법에 따라 assay kit(Asanpharm Co., Seoul, Korea)을 사용하여 측정하였다. 20 μL Serum에 37℃에서 preincubation된 ALT, AST 기질액을 100 μL 혼합하여 37℃ water bath에서 ALT는 30분, AST는 60분 방치한 후, 100 μL 2,4-dinitrophenylhydrazine를 첨가하여 실온에서 20분 반응시켰다. 반응 후 0.4 N NaOH 1 mL를 가하고 효소 작용을 정지시켜 생성된 hydrazone을 UV spectrophotometer(Specord 200, AnalytikJena, Jena, Germany) 505 nm에서 흡광도를 측정하였다. LDH(lactate dehydrogenase)와 r-GTP 농도는 혈액자동분석기(DRI-CHEM 4000i, Fujifilm co., Tokyo, Japan)를 이용하여 측정하였다.
7. 혈중 단백질 측정
단백질, 알부민, 총 빌리루빈, blood urea nitrogen(BUN), uric acid 및 creatinine 분석은 혈액생화학자동분석기인 Hitachi 7020(Hitachi Medical Co., Ltd, Tokyo, Japan)을 사용하여 동시에 분석하였다.
8. 혈중 지질 측정
혈중 총 지질 함량은 Frings CS 등(1972)과 Kang JR 등(2017)이 제시한 방법에 따라 혈청 20 µL를 진한 황산으로 분해시킨 후, phospho-vanillin 시약을 첨가하여 37℃에서 15분간 반응시킨 다음 시료 무첨가군을 대조로 하여 540 nm에서 흡광도를 측정하였다. 혈중 총 콜레스테롤(total cholesterol), HDL-콜레스테롤(high density lipoprotein cholesterol), 중성지방(triglyceride) 함량은 혈액자동분석기(DRI-CHEM 4000i, Fujifilm co., Tokyo, Japan)를 이용하여 측정하였다. LDL콜레스테롤(low density lipoprotein cholesterol) 함량은 혈청 총 콜레스테롤 — {HDL — 콜레스테롤 + (중성지질 / 5)}의 계산식에 의해 산출하였다.
9. 통계 분석
실험된 모든 자료는 IBM SPSS package version 23.0(statistical package for the social science, Armonk, NY, USA) 프로그램을 이용하여 각각 평균과 표준편차를 산출하였다. 실험 처리구 간의 통계적 유의성을 검증하기 위해 one-way ANOVA test를 실시하였으며, 처리구 간의 차이를 검증하기 위해서 Duncan의 다중범위 검정법을 실시하였다. 자료의 모든 통계학적 유의수준은 p<0.0001과 p<0.05로 설정하였다.
결과 및 고찰
1. 체중 변화, 식이 섭취량 및 식이 효율
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 체중 변화, 식이 섭취량 및 식이 효율은 Fig. 1과 Fig. 2에 제시하였다. 시험 개시 전 평균 체중은 32.27±5.16 g이었고, 종료 시 체중은 37.01±1.31 g이었다. 특히 ND군은 21.8±0.94 g에서 35.30±4.05 g로 꾸준히 증가하였으나, DCG군은 34.60±2.17 g에서 36.60±4.64 g, DCSD 10%군은 33.60±2.18 g에서 37.60±5.18 g, DCGN 10%군은 34.60±37.00 g, DCGG 10%군 33.90±36.40 g로 감소하는 경향을 보였다. Streptozotocin에 의해 유도된 당뇨 쥐는 급격한 체중 감소를 보이며(Kang JR 등 2020), 이와 같은 현상은 인슐린의 작용성 감소로 혈당 조절이 어렵고, 당이 조직 내로 공급되지 못하여 에너지원을 만들기 위해 근육 및 간 조직에서의 당 신생이 활발히 일어나는 등 당 대사의 변화를 초래함으로써 유발되는 것으로 보고되었다(F Pancani 등 2007). 선행연구(Tang Y 등 2017)에서 보면, 실험동물에서 당뇨를 유발하는 streptozotocin 투여로 인한 체중 감소 원인은 생리작용 저하, 낮은 사료 섭취량 등에 의한 스트레스, 당뇨에 의한 체내 대사 작용의 이상으로 인해 섭취한 식이가 에너지 대사에 제대로 사용되지 못한 채 체외로 배출되기 때문이라고 보고되었다. 또한 당뇨유발쥐의 팽화홍삼 분말과 음료 식이군에서는 체중의 변화가 없었으며, 식이 효율은 팽화홍삼 분말 투여군에서 높았고, 음수량 팽화홍삼투여군에서 낮았다고 보고하였다(Shim GS 등 2015). 선행연구(Pain VM & Garlick PJ 1974; Shim GS 등 2015)에서는 db/db mice의 경우 췌장 내 β-세포의 파괴로 인해 인슐린의 합성의 저하로 인해 당대사 불균형 및 체단백의 감소, 체지방 감소 결과로 체중의 변화율이 없는 것으로 판단되며, db/db mice에서 상대적으로 특수영양조제식품의 투여가 체중 증가에 큰 영향을 주지 못하는 것으로 판단된다. 본 연구에서 식이 섭취량은 대조군을 비롯하여 전체적으로 감소하는 현상을 보였으며, DCGG 10%군은 식이 섭취량의 증가 및 감소 폭이 크게 변화하였다. 또한 본 연구에서 식이 효율은 ND군에서 가장 변화 폭이 심하게 나타났으며, 모든 군에서 식이 효율은 감소 현상으로 보였다.
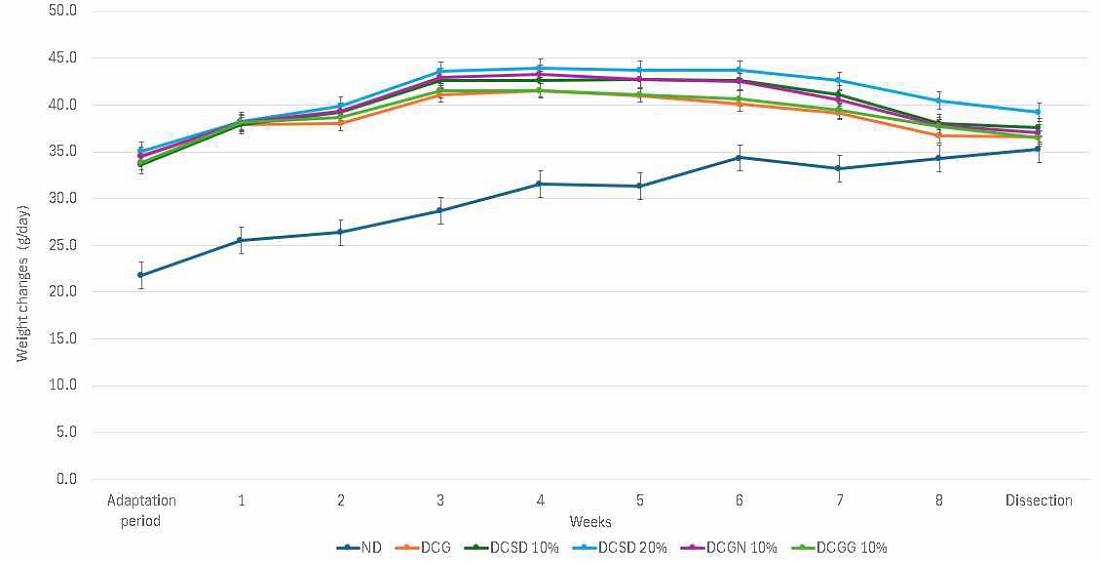
Weight changes over 8 weeks. Mean values without a common letter significantly different by Duncan’s multiple range test at p<0.05. ND: Normal diet, DCG: Diabetic control group, DCSD 10%: Diabetic control group+Sahmyook diabetic care pro 10%, DCSD 20%: Diabetic control group+Sahmyook diabetic care pro 20%, DCGN 10%: Diabetic Control Group+Newcare Dangplan 10%, DCGG 10%: Diabetic Control Group+Greenbia Dang care 10%.
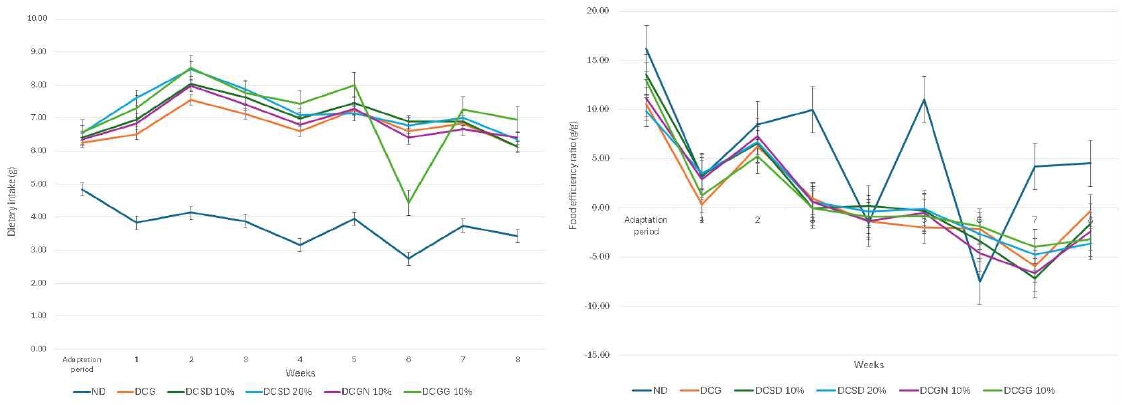
Changes in dietary intake and food efficiency ratio over 8 weeks. Mean values without a common letter significantly different by Duncan’s multiple range test at p<0.05. ND: Normal diet, DCG: Diabetic control group, DCSD 10%: Diabetic control group+Sahmyook diabetic care pro 10%, DCSD 20%: Diabetic control group+Sahmyook diabetic care pro 20%, DCGN 10%: Diabetic Control Group+Newcare Dangplan 10%, DCGG 10%: Diabetic Control Group+Greenbia Dang care 10%.
2. 조직 무게
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 간, 신장, 비장의 조직 무게는 Table 3에 제시하였다. 간 무게는 ND군 1.08±0.12 g, DCG군 2.22±0.21 g, DCSD 10%군 1.99±0.25 g, DCSD 20%군 2.09±0.24 g, DCGN 10%군 1.97±0.18 g, DCGG 10%군 1.82±0.15 g로서 대조군(ND군)에 비해 db/db mice에서 간의 무게가 유의하게 증가하였다(p<0.0001). 본 연구에서 db/db mice의 간의 무게는 증가하였으며, 선행연구(Harris EH 2005)에서도 당뇨병 환자에서 간의 비대화가 나타나며, 당뇨병으로 인해 간의 비대화가 진행된다고 보고하였다. 신장의 무게는 ND군 0.35±0.07 g, DCG군 0.46±0.04 g, DCSD 10%군 0.49±0.05 g, DCSD 20%군 0.54±0.06 g, DCGN 10%군 0.49±0.05 g, DCGG 10%군 0.52±0.05 g로서 대조군(ND군)에 비해 db/db mice에서 신장의 무게가 유의하게 증가하였다(p<0.0001). 선행연구(Mogensen CE & Andersen MJ 1973; Shim GS 등 2015)에서는 streptozotocin 유발 당뇨쥐의 경우 인슐린의 분비가 감소에 따른 당 대사의 불균형으로 인해 간, 심장 및 신장이 비대해지며, streptozotocin 유발 당뇨쥐에서 팽화홍삼 분말군과 팽화홍삼 음료 식이군 모두 대조군에 비해 비장(0.18∼0.22 g)과 신장(0.32∼0.44 g)의 장기 무게가 증가하였다고 보고하였다(Shim GS 등 2015). 본 연구에서 비장의 무게는 각 군별로 통계적으로 유의한 차이가 나타나지 않았다. 비장은 림프계에서 가장 큰 체내 기관이며, 세포성 및 체액성 면역에 중요한 역할을 한다(Kim JY 등 2024). 그러나 체내 염증반응이나 자가면역질환 등에 의해 기능 장애가 일어나면 면역체계의 불균형을 일으키는데, 본 연구에서는 다른 체내 기관에 비해 항상성 유지가 큰 것으로 사료된다.
3. 공복 혈당, 경구 내당능 검사 및 당화혈색소
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 공복 혈당, 경구 내당능 검사 및 당화혈색소는 Table 4에 제시하였다. 공복 혈당은 당뇨환자용 특수영양조제식품을 섭취한 DCSD 10%군, DCSD 20%, DCGN 10%, DCGG 10%군에서 같은 양상을 보였으며, DCG군은 383.80±113.68 mg/dL로 다른 실험군에 비해 낮은 경향을 보였다. 이는 선행연구(Kwon HO 등 2020)에서 지적했듯이 인슐린 저항성 증가에 따라 인슐린 민감성 감소로 인해 혈당의 조절이 어려워져서 공복혈당이 증가한 것을 뜻하며, 지속 시 공복혈당 장애가 유도된 것으로 판단된다. 공복 혈당은 당뇨병 발병과 합병증에 밀접한 관련이 있으므로 당뇨병 치료 시 중요한 지표로 활용되며, 공복 혈당의 상승은 말초동맥질환의 발병과 연관성이 크다고 강조하였다(Lee HI 등 2023). 선행연구(Lee HI 등 2023)에서는 밀웜 등의 추출물이 db/db mice를 이용한 실험에서 공복 혈당을 감소시켰다고 보고하였으며, 밀웜 분말을 급여한 스위스 웹스터(Swiss Webster) 마우스에서 내당능 장애가 개선되었다고 보고하였다(Samsul E 등 2020). 경구 내당능 검사 결과는 ND군을 제외하고, 494.85∼556.12 mg/dL 범위의 수치를 보였다. 본 연구에서 혈중 당화혈색소 수치는 DCSD 10%군에서 1.98±0.09%로서 DCGN 10%군(2.17±0.03%)과 DCGG 10%군(2.29±0.11%)에 비해 유의하게 낮은 수치를 보였다. 혈중 당화혈색소 수치는 당뇨병 환자에서 심장질환, 망막변증 및 신장병증 등의 당뇨합병증과 직접적인 관련이 있는 것으로 보고되고 있으며(Kwon HO 등 2016), 당화혈색소 1%를 줄이면 각각 백내장 19%, 심근경색 14%, 말초혈관 질환 43% 및 미세혈관 질환 37%를 감소시켜 당뇨로 인한 사망률이 21% 감소한다고 알려져 있다(Yun WJ 2010; Kwon HO 등 2016).
4. 혈중 인슐린, 아디포넥틴, Glucose의 변화
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 혈청 인슐린, 아디포넥틴, glucose의 변화는 Table 5에 제시하였다. 혈중 인슐린 농도는 DCG군에서 1.31±1.01 ng/dL까지 증가하였으나, DCSD 20%군에서는 0.27±0.37 ng/dL로 가장 낮은 수치를 보였다(p<0.05). 또한 DCSD 10%군(0.42±0.54 ng/dL), DCGN 10%군(0.37±0.40 ng/dL)에서는 대조군보다 낮은 수치를 보였다(p<0.05). 인슐린은 혈당 증가에 따라 췌장의 베타세포에서 분비되어 근육 및 간으로 당을 유입하고 간에서의 당신생과정(gluconeogenesis)을 억제하며 지방 조직에서는 지방생합성(de novo lipogenesis)을 촉진한다(Choi CS 2009; Kim CY & Baik IK 2023). 본 연구에서 아디포넥틴은 DCG군에서 3,868.33±1,366.04 ng/dL 수치를 보였으며, DCSD 10%군 1,770.00±190.79 ng/dL, DCSD 20%군 1,800.00±131.15 ng/dL, DCGN 10%군 1,866.67±291.43 ng/dL, DCGG 10%군 1,833.33±680.91 ng/dL의 수치를 보였다(p<0.05). 정상군(대조군)인 ND군에 비하여 실험군에서 인슐린 저항성으로 인하여 혈중 아디포넥틴이 감소하는 것을 확인하였고, DCG군에서는 인슐린 농도가 유의적으로 증가하는 것을 확인하였다. 아디포넥틴은 지방세포에서 분비되는 아디포카인(adipokine)의 일종으로 인슐린 감수성(insulin sensitivity) 조절에 기여함으로써 인슐린 저항성과 연관된다(Kim CY & Baik IK 2023). 주로 아디포넥틴은 간에서 당과 지방 생산을 억제하고 근육 조직에서 지방산 산화를 촉진함으로써 인슐린 감수성을 높이는 바람직한 영향을 미친다(Park KS 2005; Kim CY & Baik IK 2023). 비만이나 제2형 당뇨병 및 심혈관 질환 환자에 있어서 아디포넥틴 수치가 낮아지는 경향이 있으며, 이는 지방이 잘 축적되고, 대사 질환의 위험을 높이는 악순환으로 이어질 수 있다. 따라서 아디포넥틴의 농도 및 활성을 높이는 것은 인슐린 저항성 개선을 위한 치료적 전략으로 평가된다(Kim NH 등 2025). 본 연구에서 혈중 glucose 농도는 당뇨가 가장 심하게 진행된 DCG군에서 883.17±61.08 mg/dL로 가장 높은 수치를 보였으나, 당 캐치 프로를 섭취시킨 DCSD 10%군과 DCSD 20%군에서는 각각 865.17±52.41 mg/dL과 874.17±55.59 mg/dL로 낮은 수치를 보였다(p<0.05). 이는 당뇨환자용 특수영양조제식품 제조 시 함유되어 있는 치커리 식이섬유, 아가베 이눌린, 바나나잎 추출물, 돼지감자, 팔라티노스, 난소화성말토덱스트린 및 식이섬유 등의 천연 식물성 기능성 소재의 효과가 종합적으로 작용한 것으로 판단된다.
5. 혈중 간 기능 지표성분
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 혈청 중 간 기능 지표성분은 Table 6에 제시하였다. ALT 수치는 대조군에서 33.70±10.04 U/L로 정상 범위를 나타낸 반면에, DCG군에서는 118.00±20.15 U/L로 수치가 증가하기 시작하였다. DCSD 10%군에서는 147.30±80.79 U/L였으며, DCGG 10%군에서는 218.40±294.72 U/L로 유의하게 높은 수치를 보였다. ALT 수치는 간세포 내 효소인 알라닌아미노전달효소(alanine transaminase)의 혈중 농도를 나타내는데, 간세포가 파괴되면 ALT가 혈액으로 유출되어 수치가 상승하므로, 간 기능의 중요한 지표로 사용되고 있다(Lee YR & Baik IK 2024). 본 연구에서 AST 수치는 대조군에서 130.90±54.57 U/L로 정상 범위보다 높았으며, DCG군에서 274.00±147.00 U/L로서 2배 정도 상승한 수치를 보였다. DCSD 10%군에서는 471.80±406.11 U/L, DCGN 10%군에서는 248.70±173.39 U/L, DCGG 10%군에서는 312.78±294.42 U/L의 수치를 보였다. AST(aspartate aminotransferase) 수치가 높으면 간세포 손상을 의미할 수 있으나, 심장근육, 골격근 등 다른 기관에도 분포하므로 심한 운동 후에도 수치가 상승한다고 알려져 있다. 선행연구(Shin KH 등 2004; Lee YR & Baik IK 2024)에 의하면, ALT와 AST는 아미노전이 효소로서 주로 간에 존재하며, 바이러스 감염, 금속 과부하, 약물 대사로 인한 간 스트레스 혹은 손상 시에 그 농도가 특이적으로 증가한다고 보고되었다. 본 연구에서 LDH 수치는 대조군에서 364.70±134.69 U/L, DCG군에서 639.80±279.10 U/L, DCSD 10%군에서는 1,008.89±646.83 U/L, DCGG 10%군에서는 1072.29±688.07 U/L로 나타났다. LDH 수치는 젖산탈수소효소(lactate dehydrogenase)라는 효소 수치를 의미하며, LDH는 우리 몸의 거의 모든 세포에 존재한다. 또한 특정 부위의 세포가 손상되면 LDH 수치가 상승하며, 간 손상, 심근경색, 빈혈, 암 등 다양한 질병을 진단하는 데 사용한다. 간 수치 상승은 당뇨병의 발병을 높이고, 당뇨병은 지방간 등의 간질환의 발병을 높이는 밀접한 관계를 가지고 있다. 간세포가 손상되면, 인슐린 분비가 억제되고, 간에서 포도당신생작용이 과도해져서 당뇨병 발병을 증가시킨다(Kim CY & Baik IK 2023). 본 연구의 실험군에서 ALT 수치는 DCSD 10%군과 DCGN 10%군에서 가장 낮았으며, AST 수치는 DCGN 10%군과 DCGG 10%군에서 낮은 수치를 보였고, LDH 수치는 DCGN 10%군에서 가장 낮은 수치를 보였다. 이는 각각의 당뇨환자용 특수영양조제식품 제조 시에 함유된 천연 식물성 기능성 소재의 종류 및 함유량 등에 따라 차이가 나타난 것으로 사료된다. 본 연구에서는 혈중 r-GTP 농도는 대조군을 포함한 모든 군에서 관찰되지 않았다. 혈중 r-GTP 농도는 간 건강 상태와 해독 작용을 나타내는 지표로 사용되는데, 특히 약물, 음주, 비만, 지방간 및 간질환 등에 의해 수치가 상승된다(Lee EH & Chyun JH 2009). 그러나 본 연구에서는 당뇨병으로 인한 간의 산화적 손상이 크지 않아서 독성으로 인한 간 손상 정도가 증가하지 않았던 것으로 사료된다.
6. 혈중 단백질 성분
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 혈청 중 단백질 성분은 Table 7에 제시하였다. 혈중 단백질 성분은 대조군과 DCG군, DCSD 10%군, DCSD 20%군, DCGN 10%군에서는 차이가 없었으나, DCGG 10%군에서는 3.99±2.76 g/dL로 낮은 수치를 보였다(p<0.05). 당뇨가 유발된 흰쥐에서 인슐린 함량의 저하는 단백질 이화작용을 촉진하여 신장을 통해서 혈청 알부민 배설이 촉진되므로 혈중 알부민의 함량은 감소할 것을 사료된다. 혈청 알부민은 단백질 중 가장 많은 양을 차지하는 것으로 반감기가 약 20일이므로 급성 또는 경증 간 손상 시에는 대개 정상 범위(Kim KA 2009; Choi RY 등 2019)로 나타난다. 본 연구에서 총 빌리루빈 수치는 0.00∼0.04 mg/dL였으며, 빌리루빈은 헤모글로빈의 헴 분해 산물이고, 총 빌리루빈은 간담도계 장해의 지표로 사용된다(Shin HS & Lee BR 2007; Choi RY 등 2019). 혈중 빌리루빈 함량은 간 기능 장애나 황달 및 만성알코올중독 시 증가되며, STZ 투여 시 혈장 중의 빌리루빈 수치는 증가한다고 보고되었다(Shin KH 등 2004). 요산은 대조군에 비해 DCG군에서 낮아졌으며, 특히 DCGN 10%군(0.95±0.58 mg/dL)과 DCGG 10%군(1.20±0.95 mg/dL)에서 낮은 수치를 보였다. 본 연구에서 알부민, blood urea nitrogen 및 creatinine 수치는 군 간에 유의한 차이가 없었다.
7. 혈중 지질 성분
당뇨환자용 특수영양조제식품을 섭취한 db/db mice의 혈청 중 지질 성분의 변화는 Table 8에 제시하였다. 혈중 콜레스테롤 수치는 ND군에 비해서 DCG군에서 156.70±17.90 mg/dL까지 상승한 반면에, DCSD 10%군(126.20±46.08 mg/dL), DCSD 20%군(124.80±46.08 mg/dL), DCGN 10%군(113.50±64.12 mg/dL), DCGG 10%군(91.50±64.43 mg/dL)에서는 유의하게 낮은 수치를 보였다(p<0.05). 혈중 LDL-Cholesterol 수치는 DCG군(12.50±2.80)에 비해서 DCSD 10%군 8.70±3.50 mg/dL, DCSD 20%군 9.70±5.44 mg/dL, DCGN 10%군 8.20±4.92 mg/dL, DCGG 10%군 6.80±4.96 mg/dL로 유의하게 낮은 수치를 보였다(p<0.0001). 혈중 LDL-Cholesterol 수치는 혈액 내 콜레스테롤을 간에서 말초조직으로 운반하는 역할을 하는 지단백질로서 간과 말초조직에는 LDL 수용체가 있어 콜레스테롤을 흡수하게 된다(Lee YR & Baik IK 2024). 당뇨병의 병인으로 여겨지는 인슐린 저항성은 고혈당을 초래할 뿐만 아니라, 지방 조직의 유리지방산 분해 증가로 간에서 다량의 VLDL-Cholesterol이 생성되어 혈중 VLDL-Cholesterol 수치가 높아지게 된다. 또한 인슐린 저항성으로 인한 cholesterol ester transfer protein 활성화로 콜레스테롤 대신 중성지방이 풍부해진 HDL-Cholesterol이 생성되고 hepatic lipase의 작용으로 HDL-Cholesterol 수치는 낮아지는 반면, 작고 밀도가 높은 LDL-Cholesterol 수치는 증가하는 이상지혈증이 나타난다(Choi CS 2009; Kim CY & Baik IK 2023). 심뇌혈관질환을 예방하기 위해서는 혈중 LDLCholesterol 농도를 감소시키는 생활 습관 개선이나 유효성을 지닌 당뇨환자용 특수영양조제식품 등의 건강 기능성 식품의 활용 등이 필요하다. 본 연구에서 혈중 중성지방 수치는 ND(64.90±11.43 mg/dL)에 비해 4개의 실험군에서는 167.43±61.9∼356.56 mg/dL까지 2.57∼5.49배 이상 유의하게 증가하였다(p<0.05). 당뇨병과 중성지방은 인슐린 저항성이라는 원인으로 연결되어 있으며, 당뇨병에 있어서 혈중 lipoprotein lipid(LPL)에 의해 지방세포에서 지방 분해가 촉진되며, 이로 인해 혈관에 고지혈증 및 동맥경화 등의 질환 유발이 증가하게 된다(Park SH 등 2007). 본 연구에서 혈중 HDL-Cholesterol 수치는 대조군 115.80±14.29 mg/dL에 비해 DCGG 10%군에서 78.60±54.95 mg/dL로 가장 낮은 수치를 보였으나, DCSD 10%군은 103.90±38.14 mg/dL로서 다른 실험군에 비해 높은 경향을 보였다(p<0.05). 혈중 HDL-Cholesterol은 혈액 속 남은 중성지방이나 콜레스테롤을 간으로 운반 및 배출시켜 심혈관 질환 예방에 필수적이며, 수치가 낮을수록 동맥경화 위험이 높아진다(Park SH 등 2007).
요 약
본 연구에서는 삼육식품에서 개발된 특수용도식품인 당뇨환자용 특수영양조제식품을 db/db mice에게 섭취시킨 후, 타사 제품과 비교하여 농도별로 당뇨병 혈액 인자에 미치는 영향을 실험하였다. 체중은 ND군에서 꾸준히 증가하였으나, 당뇨 실험군에서는 감소하는 경향을 보였다. 혈중 당화혈색소 수치는 DCSD 10%군에서 1.98±0.09%로서 가장 낮은 수치를 보였다. 혈중 인슐린 농도는 DCSD 20%군에서는 0.27±0.37 ng/dL로 가장 낮은 수치를 보였으며(p<0.05), DCSD 10%군에서 혈중 에디포넥틴 분비량과 포도당 농도 수치가 가장 낮았다(p<0.0001). ALT, AST 및 LDH의 간 표지인자는 DCGN 10%군에서 가장 낮았다. DCSD 10%군에서 혈중 단백질 수치가 높았으며, uric acid는 DCSD 10%군, DCGN 10%군 및 DCGG 10%군에서 낮은 수치를 보였다(p<0.0001). 혈중 콜레스테롤과 LDL-Cholesterol 수치는 DCG군에 비해 실험군에서 낮은 수치를 보였으며, 혈중 중성지방 수치는 실험군에서는 2.57∼5.49배 이상 유의하게 증가하였다(p<0.05). 본 연구를 종합해 볼 때 특수용도식품인 당뇨환자용 특수영양조제식품은 체내 혈중 당뇨병 인자에 영향을 주는 것으로 판단되며, 이를 통해 당뇨환자들이 식사 대용으로 당뇨환자용 특수영양조제식품을 섭취하는 것을 권장할 수 있다. 또한 후발 주자로 특수영양조제식품에 참여한 DCSD 제품도 혈중 당화혈색소 및 포도당 수치 등을 감소시키는 것으로 나타났으며, DCSD 제품이 타제품과 비교하여 유사한 효과를 나타내고 있는 것을 증명하였으며, 경쟁력이 있는 제품으로 판단된다.
Acknowledgments
본 결과물은 삼육식품의 지원을 받아 삼육식품 중앙연구소와 함께 수행되었으며, 이에 감사드립니다.
References
- Babashahi M, Mirlohi M, Ghiasvand R, Azadbakht L (2015) Comparison of soymilk and probiotic soymilk effects on serum high-density lipoprotein cholesterol and low-density lipoprotein cholesterol in diabetic Wistar rats. ARYA Atheroscler 11(Suppl 1): 88-93.
-
Babashahi M, Mirlohi M, Ghiasvand R, Azadbakht L, Mosharaf L, Torki-Baghbadorani S (2020) Effects of probiotic soy milk fermented by Lactobacillus plantarum A7 (KC 355240) added with Cuminum cyminum essential oil on fasting blood glucose levels, serum lipid profile and body weight in diabetic wistar rats. Int J Prev Med 24(11): 8.
[https://doi.org/10.4103/ijpvm.IJPVM_541_17]

-
Bae JH, Han KD, Ko SH, Yang YS, Choi JH, Choi KM, Kwon HS, Won KC (2022). Diabetes fact sheet in Korea 2021. Diabetes Metab J 46(3): 417-426.
[https://doi.org/10.4093/dmj.2022.0106]

- Choi CS (2009) Pathogenesis of insulin resistance. Korean J Med 77(2): 171-177.
-
Choi HJ, Kim DH, Kim SY, Baek SY, Kim SJ, Kim MR (2020) Quality characteristics and antioxidant activities of ‘Sulgidduk’ added with chicory powder during storage. Food Sci Preserv 27(5): 523-533.
[https://doi.org/10.11002/kjfp.2020.27.5.523]

-
Choi RY, Ham JR, Ryu HS, Park KW, Kang KY, Lee MK (2019) The effects of defatted Tenebrio molitor Larva ferment extract on CCl4-induced liver damage in mice. J Korean Soc Food Sci Nutr 48(5): 501-508.
[https://doi.org/10.3746/jkfn.2019.48.5.501]

-
Chuang YC, Cheng MC, Lee CC, Chiou TY, Tsai TY (2019) Effect of ethanol extract from Lactobacillus plantarum TWK10-fermented soymilk on wound healing in streptozotocin-induced diabetic rat. AMB Express 9(1): 163.
[https://doi.org/10.1186/s13568-019-0886-2]

-
Frings CS, Fendley TW, Dunn RT, Queen CA (1972) Improved determination of total serum lipids by the sulfo-phospho-vanillin reaction. Clin Chem 18(7): 673-674.
[https://doi.org/10.1093/clinchem/18.7.673]

- Hariri M, Salehi R, Feizi A, Mirlohi M, Kamali S, Ghiasvand R (2015) The effect of probiotic soy milk and soy milk on anthropometric measures and blood pressure in patients with type II diabetes mellitus: A randomized double-blind clinical trial. ARYA Atheroscler 11(Suppl 1): 74-80.
-
Harris EH (2005) Elevated liver function tests in type 2 diabetes. Clin Diabetes 23(3): 115-119.
[https://doi.org/10.2337/diaclin.23.3.115]

-
Judy WV, Hari SP, Stogsdill WW, Judy JS, Naguib YMA, Passwater R (2003) Antidiabetic activity of a standardized extract (GlucosolTM) from Lagerstroemia speciosa leaves in Type II diabetics: A dose-dependence study. J Ethnopharmacol 87(1): 115-117.
[https://doi.org/10.1016/S0378-8741(03)00122-3]

-
Jung HL, Kang HY (2014) Effects of exercise intensity on PGC-1α, PPAR-γ, and insulin resistance in skeletal muscle of high fat diet-fed Sprague-Dawley rats. J Korean Soc Food Sci Nutr 43(7): 963-971.
[https://doi.org/10.3746/jkfn.2014.43.7.963]

-
Kang HY, Lee CE, Ly SY (2016) Protective effects of ethanol extract of Allium hookeri root on acute alcohol-induced intoxication in ICR mice. J Korean Soc Food Sci Nutr 45(5): 625-633.
[https://doi.org/10.3746/jkfn.2016.45.5.625]

- Kang JR, Kang MJ, Byun HW, Shin JH (2017) Effects of freeze-dried garlic powder on lipid improvement in rats fed a high fat-cholesterol diet. J Korean Soc Food Sci Nutr 46(9): 1035-1044.
-
Kang JR, Kang MJ, Kim DG, Shin JH (2020) Effects of garlic and yuza (Citrus junos) extracts on blood glucose lowering and lipid improvement in streptozotocin-induced diabetic rats. J Korean Soc Food Sci Nutr 49(1): 1-10.
[https://doi.org/10.3746/jkfn.2020.49.1.1]

-
Kim CY, Baik IK (2023) Effects of administering Platycladus orientalis leaf extract on glucose and lipid metabolism and plasma adiponectin levels in rats. J Korean Soc Food Sci Nutr 52(11): 1119-1124.
[https://doi.org/10.3746/jkfn.2023.52.11.1119]

- Kim DH, Park SC, Lee JH, Lee HY, Cho MK, Choi JY, Kim SY, Park SH (2013) Recent research trends in Korean medicine treatment of diabetes mellitus: Focusing on domestic articles from 2008 to 2013. Korean J Orient Int Med 34(3): 240-255.
- Kim HK, Kim HW (2023) Physicochemical properties of low-calorie yanggaeng containing palatinose. Journal of the Korean Society of Industry Convergence 26(6): 1025-1031.
-
Kim HN, Yu SY, Yoon WB, Jang SM, Jang YJ, Lee OH (2014) Analysis of nutritional components and physicochemical properties of hot-air dried Jerusalem Artichoke (Helianthus tuberosus L.) powder. Korean J Food Sci Technol 46(1): 73-78.
[https://doi.org/10.9721/KJFST.2014.46.1.73]

-
Kim JY, Kim S, Kim SJ, Jang SH, Yoon SR, Ryu JA, Park JM, Son JE, Jung SK (2024) The immune enhancement effect of Pinus densiflora pollen extract in splenocytes and peritoneal macrophages derived from naïve BALB/c mice. J Korean Soc Food Sci Nutr 53(6): 539-544.
[https://doi.org/10.3746/jkfn.2024.53.6.539]

- Kim KA (2009) Understanding and application of liver function tests. Korean J Med 76(2): 163-168.
-
Kim NH, Lee MH, Park YK, Lee JM (2025) Literature review on the effects of functional food ingredients for blood glucose and body fat reduction on glycemic control in insulin resistance and diabetes. J Korean Soc Food Sci Nutr 54(10): 805-811.
[https://doi.org/10.3746/jkfn.2025.54.10.805]

-
Kim SH (2014) Jerusalem Artichoke and Inulin. J Korean Diabetes 15(4): 227-231.
[https://doi.org/10.4093/jkd.2014.15.4.227]

-
Kim SH (2019) Effects of resistance exercise on blood lipid, leptin, adiponectin and insulin resistance in obese female college students. JKSSPE 24(2): 147-157.
[https://doi.org/10.15831/JKSSPE.2019.24.2.147]

-
Kim YR, Kim EY, Lee SU, Kim YW, Kim YH (2022) Effect of Euonymus alatus extracts on diabetes related markers in pancreatic β-cells and C57BL/Ksj-db/db mice. J Korean Soc Food Sci Nutr 51(9): 894-904.
[https://doi.org/10.3746/jkfn.2022.51.9.894]

-
Kim YS, Cho MS (2020) Development and optimization of a pear pound cake with resistant starch and digestion resistant maltodextrin. J Korean Soc Food Sci Nutr 49(1): 80-89.
[https://doi.org/10.3746/jkfn.2020.49.1.80]

-
Kwon HO, Koo GB, Lee YJ, Kim JH, Lee MH, In G (2020) Effect of Korean red ginseng extract (KGC05P0) on regulating insulin sensitivity, insulin and blood glucose level in hyperinsulinemia type 2 diabetic mice. J Korean Soc Food Sci Nutr 49(6): 539-546.
[https://doi.org/10.3746/jkfn.2020.49.6.539]

-
Kwon HO, Lee MH, Kim YJ, Kim E, Kim OK (2016) Beneficial effects of Acanthopanax senticosus extract in type Ⅱ diabetes animal model via down-regulation of advanced glycated hemoglobin and glycosylation end products. J Korean Soc Food Sci Nutr 45(7): 929-937.
[https://doi.org/10.3746/jkfn.2016.45.7.929]

-
Lee EH, Chyun JH (2009) Effects of chongkukjang intake on lipid metabolism and liver function in alcoholic fatty liver rats. J Korean Soc Food Sci Nutr 38(11): 1506-1515.
[https://doi.org/10.3746/jkfn.2009.38.11.1506]

-
Lee HB, Lim KM, Kim TS (2021) Correlation between metabolic health conditions and the indicators of diabetes in middle-aged women. JKSSPE 26(1): 265-277.
[https://doi.org/10.15831/JKSSPE.2021.26.1.265]

-
Lee HI, Turkyilmaz A, Lee MK (2023) Anti-hyperglycemic effects of fermented mealworm extract on type 2 diabetic mice. J Korean Soc Food Sci Nutr 52(4): 431-436.
[https://doi.org/10.3746/jkfn.2023.52.4.431]

-
Lee HJ, Lee YH, Park KO (2023) Factors associated with diabetes prevalence and diabetes awareness in Korean adults aged 30-49. Journal of Industrial Convergence 21(6): 91-97.
[https://doi.org/10.22678/JIC.2023.21.6.091]

-
Lee YR, Baik IK (2024) Effects of the administration of Crataegus pinnatifida fruit extract and ursolic acid on the biomarkers of glucose and lipid metabolism and hepatic function in adult rats. J Korean Soc Food Sci Nutr 53(10): 1014-1020.
[https://doi.org/10.3746/jkfn.2024.53.10.1014]

-
Mogensen CE, Andersen MJF (1973) Increased kidney size and glomerular filtration rate in early juvenile diabetes. Diabetes 22(9): 706-712.
[https://doi.org/10.2337/diab.22.9.706]

-
Pain VM, Garlick PJ (1974) Effect of streptozotocin diabetes and insulin treatment on the rate of protein synthesis in tissues of the rat in vivo. J Biol Chem 249(14): 4510-4514.
[https://doi.org/10.1016/S0021-9258(19)42448-4]

-
Pancani F, Lupi R, Miccoli R, Marchetti P, Del Prato S (2007) When and how to restore β-cell function? Int Congr Ser 1303: 138-145.
[https://doi.org/10.1016/j.ics.2007.03.029]

-
Park KS (2005) Relation between adiponectin and metabolic risk factors. Endocrinol Metab 20(5): 441-443.
[https://doi.org/10.3803/jkes.2005.20.5.441]

-
Park MH, Kwon CJ, Lim SH, Kim KH, Heo NK, Jang HK, Park IJ, Lee KJ (2011) Effects of dietary fiber isolated from Synurus deltoides on constipation in loperamide-induced rats. J Korean Soc Food Sci Nutr 40(12): 1715-1719.
[https://doi.org/10.3746/jkfn.2011.40.12.1715]

-
Park SH, Jang MJ, Hong JH, Rhee SJ, Choi KH, Park MR (2007) Effects of mulberry leaf extract feeding on lipid status of rats fed high cholesterol diets. J Korean Soc Food Sci Nutr 36(1): 43-50.
[https://doi.org/10.3746/jkfn.2007.36.1.043]

-
Samsul E, Soemardji AA, Kusmardiyani S, Kuncoro H (2020) Antidiabetic activity of Tenebrio molitor linn powder by oral glucose tolerance test to swiss webster male mice. Res J Chem Environ 24(2): 24-27.
[https://doi.org/10.25026/jsk.v2i4.150]

-
Shim GS, Seong KS, Lee KW, Cho CW, Lee OH, Lee JH, Han CK (2015) Effects of puffed red ginseng power and drink on blood glucose and serum lipid profile in streptozotocin-induced diabetic rats. J Korean Soc Food Sci Nutr 44(10): 1415-1421.
[https://doi.org/10.3746/jkfn.2015.44.10.1415]

- Shin HS, Lee BR (2007) The effect of 5-oxohexyl-3,7-dimethylxanthine on carbon tetrachlroride-induced hepatotoxicity in rats. Environmental Analysis Health and Toxicology 22(3): 219-225.
-
Shin KH, Cho SY, Lee MK, Lee JS, Kim MJ (2004) Effects of Aralia elata, Acanthopanacis cortex and Ulmus davidiana water extracts on plasma biomarkers in strepto-zotocin-induced diabetic rats. J Korean Soc Food Sci Nutr 33(9): 1457-1462.
[https://doi.org/10.3746/jkfn.2004.33.9.1457]

-
Shin MJ, Park MJ, Youn MS, Lee YS, Nam MS, Park IS, Jeong YH (2006) Effects of silk protein hydrolysates on blood glucose and serum lipid in db/db diabetic mice. J Korean Soc Food Sci Nutr 35(10): 1343-1348.
[https://doi.org/10.3746/jkfn.2006.35.10.1343]

-
Shin S, Park SS, Lee HM, Hur JM (2014) Effects of fermented chicory fiber on the improvement of intestinal function and constipation. J Korean Soc Food Sci Nutr 43(1): 55-59.
[https://doi.org/10.3746/jkfn.2014.43.1.055]

- Yang Y, Kim YH, Hwang HH (2017) Effect of Helianthus tuberosus juice mixed with dried bitter melon juice on hypoglycemic function in streptozotocin-induced diabetic rats. J Korean Soc Food Sci Nutr 46(8): 903-909.
-
Yun WJ (2010) Relationship between glycemic control and diabetic retinopathy. J Korean Geriatr Soc 14(4): 234-241.
[https://doi.org/10.4235/jkgs.2010.14.4.234]