Lacticaseibacillus rhamnosus L22-FR28의 고밀도 분말 생산을 위한 최적 배양 및 동결건조 조건
Abstract
Probiotic lactic acid bacteria require robust culture and freeze-drying processes to maintain high viability for functional food applications. In this study, the culture and freeze-drying conditions were optimized to produce a high-density freeze-dried powder of the Lacticaseibacillus rhamnosus L22-FR28 (KACC 92513P). The strain was cultivated in a food-grade medium containing 2.5% yeast extract, 1%-2% peptone, and the antioxidant L-cysteine, with glucose concentrations of 3% (BC3) and 5% (BC5). Cultivation was carried out in 5 L fermenters with the pH maintained at 5.7. After cultivation, the cells were harvested by centrifugation, resuspended in a cryoprotectant mixture [2% (v/v), based on culture volume], rapidly frozen, and freeze-dried to obtain probiotic powders. The freeze-dried powder produced in 5% glucose medium showed a viable cell count of 3.74 × 1011 CFU/g and a freeze-drying survival rate of 81.66%, which were significantly higher than those obtained in the 3% glucose medium (1.91 × 1011 CFU/g and 63.88%, respectively). These results suggest that the optimized culture and freeze-drying conditions established in this study enable the production of high-density, high-viability L. rhamnosus L22-FR28 powder and may be useful for manufacturing industrial-scale probiotics.
Keywords:
Lacticaseibacillus rhamnosus, freeze-drying, culture optimization, viability, probiotic production서 론
프로바이오틱 유산균은 장 건강 증진, 면역 조절, 병원균 억제 등 다양한 생리활성을 바탕으로 기능성 식품과 건강보조제의 핵심 미생물 소재로 활용되고 있다(Amin MdR 등 2025; Hajzer ZE 등 2025). 프로바이오틱의 효능은 균주의 특성, 섭취량, 섭취 기간 등 여러 요인에 의해 영향을 받지만, 특히 섭취 시점에 살아 있는 세포 수와 밀접한 관련이 있는 것으로 보고되고 있으므로(Mendonça AA 등 2022), 산업 현장에서는 배양부터 제품 유통까지 전 과정에서 충분한 생균수를 유지하는 것이 중요하다. 그러나 실제 생산 공정에서는 고농도 배양, 원심분리 및 세포 농축, 동결 및 건조, 포장과 저장 과정에서 저온·건조·산화·삼투 등 다양한 물리·화학적 스트레스가 반복적으로 작용하여 세포 생존율이 점차 감소하는 것으로 보고되고 있다(Meng XC 등 2008; Soro-Yao AA 등 2014; Fonseca F 등 2014). 이러한 생존율 저하는 최종 제품의 표시균수(label claim)와 소비자가 실제로 섭취하는 균수 사이의 차이를 확대시킬 수 있으며, 이를 보완하기 위해 제조 단계에서 과잉 접종(overage)을 적용하거나 보다 보수적인 품질 기준을 설정하는 전략이 활용되고 있다(Fenster K 등 2019; Weitzel MLJ 등 2021). 또한 동결건조 유산균의 저장 안정성은 제품의 품질 유지와 유통기한 설정에 직결되는 요소로서, 산업 현장에서 경제성 측면에서도 중요한 고려 대상이 되는데(Fenster K 등 2019; Jeong SG 등 2022), 장기 저장 안정성이 충분하지 않을 경우 유통기한 단축, 추가 품질관리 비용, 제품 폐기 위험이 증가하여 전체 공정의 경제성을 저하시킬 수 있기 때문이다(Jeong SG 등 2022). 따라서 프로바이오틱 유산균의 산업적 활용을 위해서는 배양, 동결건조, 저장 단계에서의 스트레스 요인을 최소화하고 높은 초기 생균수와 장기 저장 안정성을 동시에 확보할 수 있도록 공정 및 제형을 통합적으로 최적화하는 보존 전략을 확립할 필요가 있다(Meng XC 등 2008; Peighambardoust SH 등 2011).
Lacticaseibacillus rhamnosus는 위산과 담즙에 대한 내성, 장 점막 부착능, 면역 조절 능력 등 다양한 프로바이오틱 특성을 가지고 있어 발효 유제품과 건강기능식품에 널리 사용되는 대표적인 균주이다(Segers ME & Lebeer S 2014; Liu X 등 2025). 그러나 L. rhamnosus는 균주마다 탄소·질소원, pH, 용존산소 등 환경 요인에 대한 요구성과 산·산화 스트레스 내성이 상이하므로, 특정 균주 특성에 적합한 배지 조성과 배양 조건을 설정하는 것이 고세포밀도 배양과 후속 공정에서의 생존율 확보에 필수적이다(Feng T & Wang J 2020; Wang T 등 2020). 수확된 프로바이오틱 유산균은 산업 현장에서 가장 널리 사용되는 방법인 동결건조를 통해 분말 형태로 제조되며, 이 과정에서 sucrose와 trehalose와 같은 당류, 탈지유와 같은 단백질계 성분, glycerol과 같은 polyol 계열의 동결보호제가 흔히 사용되고 있으며(Carvalho AS 등 2004; Cui S 등 2022), 이러한 동결보호제는 수분 제거 과정에서 세포막 인지질과 단백질을 보호하고, 당류 기반의 비정질(glassy) 매트릭스를 형성함으로써 동결 및 건조 스트레스로 인한 세포 손상을 완화하는 데 기여하는 것으로 보고되고 있다(Santivarangkna C 등 2008; Peighambardoust SH 등 2011). 동결건조된 유산균 분말을 대상으로 한 연구에서 수분활성도(aw)가 약 0.1∼0.3 범위의 중간 수준으로 유지될 때 장기 저장 중 생존율이 가장 높고, 이 범위를 벗어나 aw가 증가하면 비활성화 속도가 증가하는 것으로 보고되고 있다(Passot S 등 2012; Burca-Busaga CG 등 2020). 지금까지의 선행연구들은 주로 실험실 규모에서 MRS 계열 배지와 단일 또는 단순 조합의 동결보호제를 사용하여 L. rhamnosus의 생존율에 미치는 온도, 수분활성, 보호제 조성의 영향을 평가해 왔으나, 식품등급 영양원을 기반으로 한 배지 설계와 pH 제어를 결합하여 고세포밀도 배양 조건을 확립하고, 그 조건이 동결건조 생존율과 분말 특성에 미치는 영향을 체계적으로 분석한 연구는 상대적으로 부족한 실정이다. 특히 특정 L. rhamnosus 균주를 대상으로 실제 산업 적용을 염두에 둔 배양 및 동결건조 조건을 제시한 사례는 충분하지 않다.
L. rhamnosus L22-FR28(KACC 92513P)는 농촌진흥청에서 영아 분변으로부터 분리·보존 중인 프로바이오틱 후보 균주로, 장 건강 및 대사 질환 개선을 목표로 한 기능성 평가와 제형화 연구가 현재 초기 단계에 있다. 본 연구에서는 이 균주의 향후 기능성 식품 소재로서의 활용 가능성을 염두에 두고, 식품등급 영양원을 활용한 배지 설계와 pH 제어를 통해 고세포밀도 배양 조건을 확립하는 한편, 탄소원 농도와 L-시스테인 첨가 조건에 따른 동결건조 후 세포 생존율을 비교하여 최적 배양 조성을 도출하고자 하였다. 또한 도출된 조건이 향후 파일럿 규모 이상의 스케일업 검토와 생균수를 포함한 표준화된 품질 지표를 기반으로 한 일관된 프로바이오틱 분말 제품 생산 공정 설계에 활용될 수 있도록 기초 자료를 제공하고자 하였다.
재료 및 방법
1. 균주 및 배양조건
실험에 사용한 Lacticaseibacillus rhamnosus L22-FR28 균주는 본 연구실에서 영아 분변으로부터 분리한 균주로, 국립농업과학원 농업미생물은행(KACC)에 KACC 92513P 번호로 기탁되어 있다. 실험실 보존 균주는 L. rhamnosus L22-FR28 배양액 1 mL에 100% glycerol 0.5 mL를 혼합하여 —80℃ 초저온 냉동고(DF8517, Ilshin BioBase Co., Ltd, Dongducheon, Korea)에서 보존하였다. 실험 전 활성화를 위해 동결 보존된 균주를 해동한 뒤 MRS agar(Difco, BD, Franklin Lakes, NJ, USA)에 도말하여 37℃에서 24 hr 배양하였다. 형성된 단일 집락을 동일한 배지에 2회 추가 계대 배양한 후 시드 배양에 사용하였다. 시드 배양은 활성화된 단일 집락을 MRS broth(Difco, BD, Franklin Lakes, NJ, USA)에 1%(v/v) 비율로 접종하여 37℃에서 18 hr 정치 배양하였으며, 전배양은 시드 배양액을 동일한 배지에 1%(v/v) 비율로 접종하여 같은 조건(37℃, 18 hr, 정치)에서 배양하였다. 본배양에는 동물성 성분을 배제한 식품등급 액체배지를 사용하였으며, 배지의 기본 조성(포도당, 펩톤, 효모추출물, 무기염 및 보조인자 등)은 Table 1에 제시하였다. 본배양은 식품등급 배지 3.0 L로 채운 5 L jar fermenter(KF-7L, KoBioTech Co., Ltd, Incheon, Korea)에 전배양액을 2%(v/v) 비율로 접종하여 37℃, 150 rpm, 무통기(비통기) 조건에서 배양하였다. L. rhamnosus L22-FR28을 배양하는 동안 산성화에 따른 생육 저해를 방지하기 위해 암모니아수 용액(27∼30%, Samchun, Pyeongtaek, Korea)을 첨가하여 pH를 5.7로 제어하였으며, 배양액의 pH를 측정하기 위하여 pH controller(KB250, KoBioTech Co., Ltd, Incheon, Korea)를 사용하였다. 모든 배양 실험은 독립적으로 3회 이상 반복 수행하였으며, 결과는 평균±표준편차로 나타내었다.
2. Flask 배양 생육곡선 분석 및 배양시간 최적화
Flask scale에서 L. rhamnosus L22-FR28의 최적 배양시간을 결정하기 위하여, 활성화된 균주를 MRS broth(Difco, BD, Franklin Lakes, NJ, USA)에 1%(v/v) 비율로 접종한 후 37℃에서 정치 배양하며 생육 곡선을 분석하였다. MRS broth를 공시험(blank), 배양 0∼18 hr동안 1.5∼2 hr 간격으로 회수한 배양액의 흡광도를 600 nm에서 분광광도계(GENESYS 10S, Thermo Scientific, Madison, WI, USA)를 이용하여 측정하였다. 각 시간점의 OD600 값은 L. rhamnosus L22-FR28을 flask scale로 독립적으로 3회 배양하여 측정한 값의 평균으로 산출하였다. 대수증식기 종료 시점을 판단하기 위하여 인접한 두 시점(t1, t2)사이의 구간별 절대 성장속도(ΔOD600/Δt)를 계산하였으며, 여기서 ΔOD600는 t2와 t1에서의 OD600 값의 차이, Δt는 두 시점 사이의 배양시간(hr)으로 정의하였다. 구간별 절대 성장속도가 감소하여 0에 수렴하고 OD600 증가가 정체되는 시점을 정체기(성장정지기) 진입시점으로 간주하였으며, 이 직전 구간을 대수증식기 종료 시점으로 보아 최적 배양시간으로 결정하였다. 이렇게 결정된 최적 배양시간은 이후 5 L jar fermenter 전배양 및 본배양에도 동일하게 적용하였다.
3. 배지조성 최적화
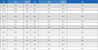
L. rhamnosus L22-FR28의 생육을 향상시킬 배지 조성을 선정하기 위하여, 질소원 및 첨가제 조성이 상이한 5종의 식품등급 배지(A∼E)를 비교하였다(Table 1). 공통 기본배지 조성은 포도당 3%(w/v), 아세트산나트륨 0.25%(w/v), 인산수소칼륨 0.2%(w/v), 황산망간 0.005%(w/v), 황산마그네슘 0.01%(w/v), Tween 80 0.1%(v/v)를 포함하도록 조성하였다. 질소원과 첨가제의 종류 및 농도는 배지 A∼E에서 각각 다르게 조합하였으며, 구체적인 조성은 Table 1에 제시하였다. 각 배지는 삼각 플라스크에 분주하여 121℃에서 15 min 동안 고압증기 멸균하여 준비하였다. 멸균된 배지를 실온에서 방랭한 후, L. rhamnosus L22-FR28 시드 배양액을 1%(v/v) 비율로 접종하여 37℃에서 24 hr 동안 정치 배양하였다. L. rhamnosus L22-FR28을 접종하지 않은 동일 배지를 공시험(blank)으로 사용하였으며, 배양 7 hr 및 24 hr에 각 플라스크에서 배양액 시료를 회수하여 흡광도(OD600)를 측정하였다. 또한 배양 7 hr 및 24 hr 시점의 배양액을 광학현미경(CX31, Olympus, Lapu-Lapu, Philippines)으로 400배 배율에서 관찰하여 세포 형태와 응집 여부를 평가하였다. 배양 7 hr 및 24 hr 시점의 OD600 값의 변화와 세포 응집 양상을 종합적으로 비교하여 L. rhamnosus L22-FR28의 생육에 가장 적합한 배지 조성을 최적 배지 조성으로 선정하였다.
4. 5 L Jar Fermenter 배양 및 탄소원 농도 최적화
Flask scale 실험에서 선정된 후보 배지 조성(B, C)을 5 L jar fermenter 배양에 적용하여 L. rhamnosus L22-FR28의 대량 배양 시 생육 양상을 비교하였다. 두 후보 배지 중 생육도가 우수한 배지를 기반으로 L-시스테인 첨가 효과를 평가하기 위해 두 조건(BC, CC)을 설정하였다. 두 조건 모두 포도당 농도는 3%(w/v)로 동일하게 유지하였으며, BC 배지는 펩톤 1.0%(w/v)와 L-시스테인 0.1%(w/v)를 포함하도록 조성하였고, CC 배지는 펩톤 2.0%(w/v)를 포함하되 L-시스테인은 첨가하지 않았다(Table 1). 5 L jar fermenter 배양은 식품등급 배지 BC 또는 CC를 3.0 L를 취하여 121℃에서 15 min동안 고압증기 멸균한 후 수행하였다. 멸균·조립을 마친 5 L jar fermenter에 전배양액을 2%(v/v) 비율로 접종한 후 본배양(37℃, 150 rpm, 무통기)하였으며, pH controller를 사용하여 암모니아수 용액을 주입함으로써 5.7로 유지하였다. 배양 0, 4, 6, 9, 12 hr 시점에서 발효조로부터 시료를 회수하여 600 nm에서 흡광도 및 생균수를 측정하였다. 생균수 측정을 위해 회수한 배양액을 0.85%(w/v) 멸균 생리식염수로 단계 희석한 후, 각 희석액을 MRS agar 평판에 도말하여 37℃에서 48 hr 배양하였다. 집락 수가 30∼300 CFU 범위에 해당하는 평판을 선택하여 생균수(CFU/mL)를 산출하였다. 배양 종료 시점(12 hr) 배양액을 광학현미경으로 400배 배율에서 관찰하여 세포 응집 정도를 정성적으로 평가하였다. 탄소원 농도 최적화를 위해 BC 배지 조성을 기반으로 포도당 농도를 3%(BC3)와 5%(BC5)로 설정하고, 각각에 대해 동일한 5 L jar fermenter 조건[37℃, 150 rpm, 무통기, pH 5.7 제어, 접종량 2%(v/v)]에서 배양하였다. 배양 중 시료를 채취하여 OD600 및 생균수를 측정하였고, 잔당(포도당) 농도는 Miller의 DNS 방법(Miller GL 1959)을 변형하여 분석하였으며, pH 변화는 pH controller로 모니터링하였다. 잔당이 거의 소모되고 OD600 및 생균수 증가가 정체되는 시점을 배양 종료 시점으로 간주하고, 포도당 농도(3%와 5%)에 따른 세포 증식과 수율을 비교하였다.
5. 동결건조 및 분말화
5 L jar fermenter에서 배양을 종료한 후, 배양액을 4℃에서 10,000 rpm, 15 min 동안 원심분리(1736R, Labogene, Lillerod, Denmark)하여 균체를 회수하였다. 회수된 cell pellet의 습중량을 측정하여 배양 조건(BC3, BC5) 간 균체 회수량(g wet weight/L)을 비교하였다. 동결보호제로는 lactose(Wisconsin Whey Protein, Darlington, WI, USA)를 사용하였으며, 해당 제제는 ㈜휴온스앤에서 제공한 표준 포뮬러이다. 각 처리군의 cell pellet에 대해 배양액 부피 기준 2%(v/v)가 되도록 동결보호제를 첨가한 뒤, 균체가 균일하게 분산되도록 잘 혼합하여 현탁액을 제조하였다. 준비된 현탁액은 —80℃에서 급속 동결한 후, 동결건조기(FDL-5S8, Esco Micro Pte. Ltd, Changi, Singapore)를 사용하여 —55℃, 0.1 mbar 조건에서 48 hr 동안 동결건조하여 프로바이오틱 유산균 분말을 제조하였다. 동결건조가 완료된 분말은 무균조작 하에 회수한 뒤, 수분활성도(aw) 0.2∼0.3 수준을 유지할 수 있는 방습 용기에 밀봉하여 4℃에서 저장하였다. 각 처리군(BC3, BC5)에 대하여 동결건조 전 균체-동결보호제 혼합물의 무게와 동결건조 후 얻은 분말의 무게를 측정하여 분말 회수율을 산출하였다.
6. 생균수 및 동결건조 생존율
L. rhamnosus L22-FR28 프로바이오틱 유산균 분말의 생균수는 분말 시료 1.0 g을 0.85%(w/v) 멸균 생리식염수에 넣고 충분히 현탁한 뒤, 동일한 희석액으로 10배 단계 희석 실시하여 측정하였다. 각 희석 단계에서 희석액 0.1 mL을 취하여 MRS agar(Difco, BD, Franklin Lakes, NJ, USA) 평판에 도말한 후, 37℃에서 48 hr 배양하였다. 배양 후 30∼300 CFU 범위에 해당하는 평판만을 선택하여 집락 수를 계수하고, 희석 배수를 고려하여 L. rhamnosus L22-FR28 분말 시료 g당 생균수(CFU/g)를 산출하였다. 모든 배양 및 분석은 독립적으로 3회 이상 반복수행하였으며, 결과는 평균±표준편차로 나타내었다.
7. 통계분석
모든 실험은 독립적으로 3회 이상 반복 수행하였으며, 얻어진 데이터는 SPSS Statistics ver. 23(IBM Corp., Armonk, NY, USA)을 이용하여 분석하였다. 결과는 평균±표준편차로 나타내었다. BC3와 BC5, BC와 CC와 같이 두 처리구만을 비교한 경우에는 독립표본 t-검정(independent-samples t-test)을 이용하여 각 배양시간별 두 처리구의 평균값 차이를 검정하였다. 모든 통계 분석에서 유의수준은 p<0.05로 설정하였다.
결과 및 고찰
1. L. rhamnosus L22-FR28 배양시간 최적화
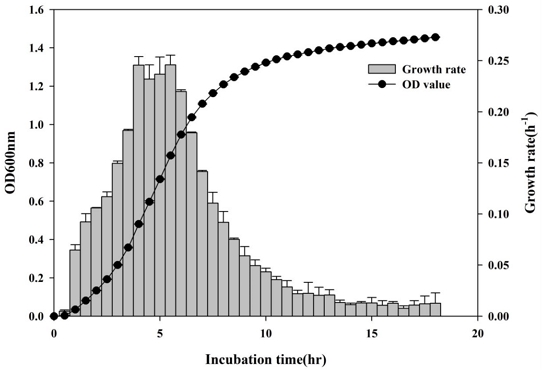
Flask scale에서 MRS broth에 배양한 L. rhamnosus L22-FR28의 생육곡선을 분석한 결과(Fig. 1), 접종 직후부터 배양 11 hr까지 OD600 값이 지속적으로 증가하였고, 배양 11∼13 hr 구간에서는 증가 폭이 점차 감소하였다. 각 시간점의 OD600 값은 독립적으로 3회 배양하여 얻은 결과의 평균값±표준편차로 나타내었다(Fig. 1). 구간별 성장속도(ΔOD600/Δt)를 산출했을 때 배양 3∼11 hr 구간에서 높은 값을 보였으며, 배양 11 hr 이후부터는 성장속도가 감소하여 배양 13 hr 시점에서는 ΔOD600/Δt가 0에 수렴하였다. 배양 13 hr 이후 OD600 값은 세 독립 배양에서 모두 plateau 양상을 보였으며 추가적인 증가는 거의 관찰되지 않았으므로, 이 시점에서 L. rhamnosus L22-FR28이 대수증식기를 종료하고 정체기에 진입한 것으로 판단하였다. 따라서 flask scale에서의 실용적인 최적 배양시간은 대수증식기 종료 직전인 배양 12 hr 전후로 설정하는 것이 적절하다고 판단하였으며, 과배양으로 인한 영양 고갈과 대사산물 축적에 따른 자기저해(self-inhibition)를 최소화하기 위해 이후 전배양 및 5 L jar fermenter 본배양에서도 12 hr를 표준 배양시간으로 적용하였다. 유산균은 MRS 배지와 같이 성장에 적합한 환경에서도 배양 후반으로 갈수록 유기산 축적, 영양소 고갈, pH 저하 등으로 인해 성장 저해를 겪으며 생육 속도가 감소하고, 정체기 이후 장시간 배양 시 세포 생존율과 기능성이 저하될 수 있으므로(Leroy F & Vuyst LD 2001; Papadimitriou K 등 2016), 프로바이오틱 생산 공정에서 생육곡선, 성장속도, pH·당 소모를 기반으로 최적 수확 시점을 설정하는 것은 후속 농축·건조 공정에서의 생존율과 기능성 유지에 중요하다고 보고되고 있다(Sin PY 등 2024). 따라서 본 연구에서 설정한 표준 배양시간 12 hr는 L. rhamnosus L22-FR28의 고세포밀도 확보와 동시에 과도한 스트레스 노출을 피하기 위한 합리적인 기준이라 사료된다. 이러한 결과는 향후 파일럿 규모 이상의 스케일업 과정에서 배양 종료 시점을 설정하는 실험적 근거를 제공하며, 공정 조건 최적화를 통해 균주의 생존율과 기능성을 유지하는 데 활용될 수 있을 것으로 판단된다.
2. 배지조성에 따른 생육특성
배지 조성에 따른 L. rhamnosus L22-FR28의 생육 특성을 평가하기 위해, 질소원과 보조인자 조성을 달리한 5종 배지(A∼E)에 균을 접종하여 배양한 후 생육과 미세구조를 비교하였다(Fig. 2). 공통 배지 조성(포도당 3%, 무기염, 보조인자 등)에 효모추출물 2.5%(w/v)를 공통으로 포함한 A∼D 배지 중에서, 배양 24 hr 기준 ΔOD600[배양 0 hr와 24 hr 사이 OD600 차이]는 B(펩톤 1.0%)에서 7.98, C(펩톤 2.0%)에서 9.30으로 가장 높았으며, 효모추출물 농도를 1.0%로 낮춘 E 배지에서는 ΔOD600이 5.96으로 가장 낮았다(data not shown). 또한 펩톤 농도 1%(B)와 2%(C) 비교에서는 ΔOD600이 1.32 증가한 반면, 효모추출물 농도를 2.5→1.0%로 감소시킨 B→E 비교에서는 ΔOD600이 2.02 감소하여, L. rhamnosus L22-FR28에서 효모추출물 농도가 생육에 미치는 영향이 펩톤 농도보다 더 큰 것으로 확인되었다. 이는 효모추출물이 아미노산, 비타민, 뉴클레오티드 등 복합 영양원을 제공하여 질소원 역할뿐 아니라 성장인자와 미량 영양소 공급원으로 작용해 유산균의 생육과 대사활성을 증진시키며, 펩톤 단독보다 높은 세포 밀도 형성에 기여한다는 선행 연구 결과와 일치한다(Liu B 등 2010; Choi GH 등 2021; Tao Z 등 2022).
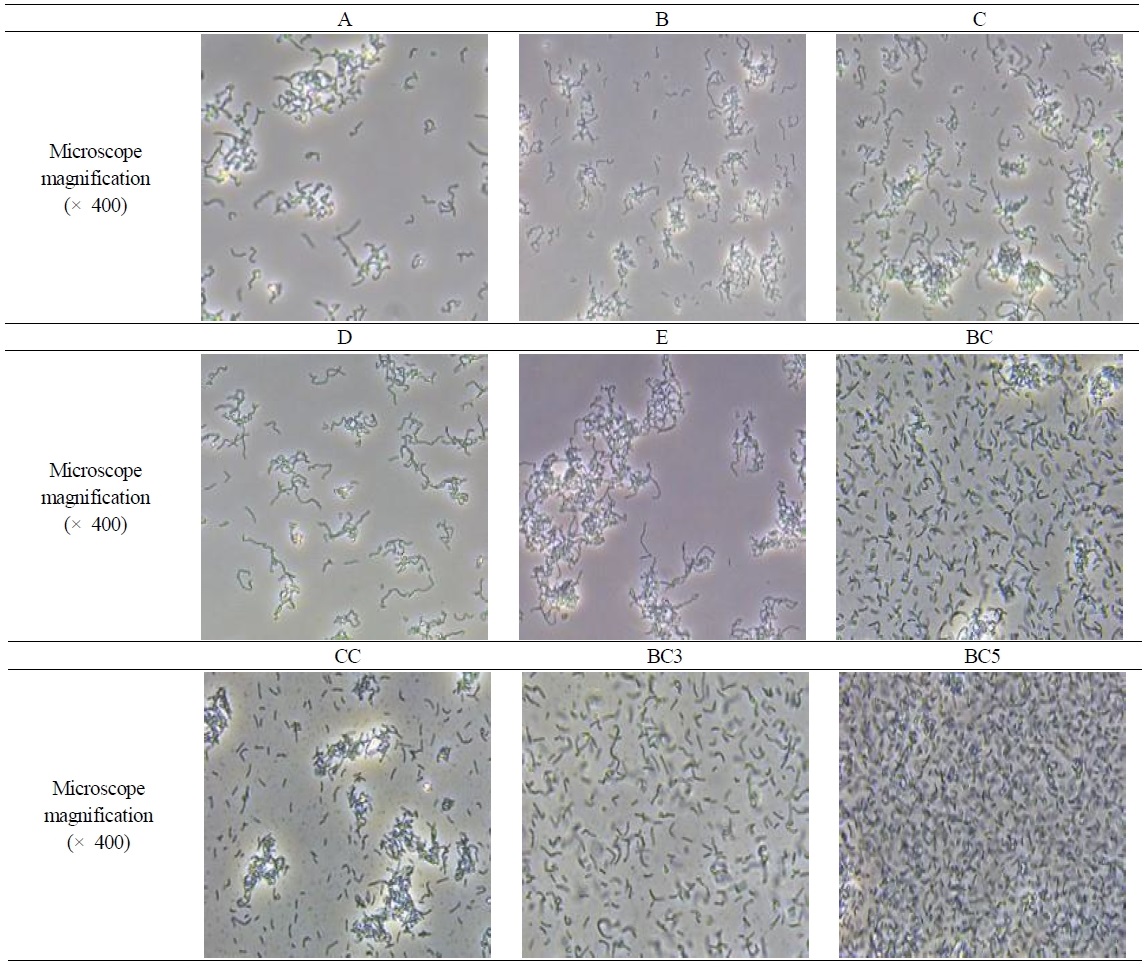
Microscopic images of L. rhamnosus L22-FR28 cultivated in different medium. (A∼E) Cultures grown in candidate medium A∼E containing different nitrogen sources and additives (see Table 1 for detailed compositions). (BC) Culture in BC medium (3% glucose, 1.0% peptone, 0.1% L-cysteine). (CC) Culture in CC medium (3% glucose, 2.0% peptone, no L-cysteine). (BC3, BC5) Cultures grown in BC medium containing 3% and 5% glucose, respectively. Cells were collected at the end of incubation and observed by light microscopy (× 400).
현미경 관찰 결과, 배양 7 hr 시점에서 B와 C 배지는 상대적으로 높은 세포 밀도와 함께 세포가 덩어리 형태로 뭉치는 자가응집(auto-aggregation) 양상이 관찰되었다(Fig. 2). 자가응집은 유산균 표면의 단백질 및 다당체에 의해 매개되며 장 상피세포 부착, 장내 정착성과 연관된 프로바이오틱 특성으로 보고된 바 있으나, 과도한 응집은 배양액 점도 증가와 국소 농도 구배를 유발해 균일한 배양과 물질 전달에 불리할 수 있다(Zawistowska-Rojek A & Tyski S 2018; Wang S 등 2024). 반면, L-시스테인을 보조인자로 첨가한 D 배지에서는 동일 시간대에 세포가 상대적으로 잘 분산된 형태로 관찰되었고, 큰 응집 덩어리의 형성 빈도가 감소하였다(Fig. 2). L-시스테인은 유산균 배양에서 환원제 및 항산화 보조제로 사용되며, 특정 조건에서 배양 중 산화 스트레스를 완화하고 세포 생존성 또는 유산균 수를 향상시킨다고 보고되어 있다(Dave RI & Shah NP 1997; Santiesteban-López A 등 2013). 본 연구의 flask scale 조건에서 L-시스테인 첨가는 ΔOD600 기준 총 생육을 뚜렷하게 증가시키지는 않았으나, 현미경 관찰을 통해 세포 응집 정도를 완화하는 정성적 경향이 확인되었으며, 후속 대형 발효조 운전 시 균일한 배양 및 수확 효율을 확보하는 데 보조적으로 활용할 수 있을 것으로 판단된다. 이러한 결과를 종합하면, L. rhamnosus L22-FR28의 고세포밀도 배양을 위해서는 펩톤 농도 증가만으로는 한계가 있으며, 효모추출물 함량을 충분히 유지하는 것이 중요하고, L-시스테인과 같은 보조 인자를 활용해 과도한 자가응집을 완화하는 것이 공정 운전 측면에서 유리할 수 있음을 시사한다. 따라서 5 L jar fermenter 실험에서는 생육이 우수한 B 및 C 배지를 기본 조성으로 선택하고, 여기에 L-시스테인을 보조인자로 첨가한 배지조성을 설정하였다.
3. L-시스테인 첨가에 따른 생육 특성
Flask scale 배양에서 생육이 우수했던 B, C 배지를 바탕으로, 펩톤과 L-시스테인 조성이 다른 두 조건(BC: 펩톤 1.0%, L-시스테인 0.1%; CC: 펩톤 2.0%, L-시스테인 무첨가)을 5 L jar fermenter 배양에 적용하여 L. rhamnosus L22-FR28의 생육 특성을 비교하였다. 배양 12 hr에서 BC의 흡광도와 생균수는 각각 1.1076, 9.70 × 10⁹ CFU/mL였고, CC는 1.0714, 7.60 × 10⁹ CFU/mL로 나타났으며(Table 2), 독립표본 t-검정(independent-samples t-test) 결과 두 조건 간 차이는 통계적으로 유의하였다(p<0.05). 따라서 동일한 포도당 농도(3%) 조건에서 효모추출물 농도를 2.5%(w/v)로 유지하면서 펩톤을 1.0%(w/v)로 설정하고, 여기에 L-시스테인 0.1%(w/v)를 보조인자로 첨가한 조건(BC)이, 펩톤을 2.0%(w/v)로 증가시키고 L-시스테인을 첨가하지 않은 조건(CC)보다 L. rhamnosus L22-FR28의 세포 밀도 향상에 유리한 것으로 판단되었다. 현미경 관찰 결과(Fig. 2), CC 배지에서는 배양 후기(12 hr) 배양액에서 다세포 응집체가 다수 관찰된 반면, BC 배지에서는 세포가 상대적으로 분산된 형태를 유지하는 경향을 보였다. 이는 flask scale 배양에서 관찰된 결과와 일치하며, L-시스테인 첨가가 L. rhamnosus L22-FR28의 과도한 자가응집을 완화하여 배양액 내에서 세포가 균일하게 분산되도록 돕는다는 것을 시사한다. 자가응집은 세포 간 부착으로 인해 국소적인 세포 밀도와 점도를 증가시키고, 산소·영양분 공급 및 대사산물 확산을 저해하여 균일한 배양을 방해할 수 있는 것으로 알려져 있으므로(Wang S 등 2024), 응집 완화는 결과적으로 대량 배양에서의 생육 환경을 개선하는 요인으로 작용할 수 있다. 본 연구에서는 배양액의 산화환원전위나 세포 표면 단백질 구조를 직접 측정하지는 않았으나, L-시스테인은 일반적으로 유산균 배양에서 환원제 및 산소 소거제(oxygen scavenger)로 사용되며, 배양 및 저장 과정에서 일부 프로바이오틱 균주의 생존성을 개선하는 것으로 보고되어 있다(Dave RI & Shah NP 1997; Rodrigues D 등 2011). 따라서 L. rhamnosus L22-FR28을 배양할 때 L-시스테인을 첨가한 조건은 배양 중 redox 스트레스를 완화하고 세포 표면 특성 및 응집 양상에 간접적으로 영향을 미쳐, 5 L jar fermenter 배양 시 관찰된 생균수 증가와 응집 감소에 기여했을 가능성이 있을 것으로 사료된다. 또한 5 L 규모 배양에서 L-시스테인 첨가 조건(BC)이 무첨가 조건(CC)보다 유의하게 높은 세포 밀도와 보다 균일한 세포 분산 상태를 보였다는 결과는, L. rhamnosus L22-FR28의 실용적 배양 조건 설정에서 L-시스테인을 0.1% 수준으로 보조 첨가하는 것이 유효한 전략임을 뒷받침한다. 하지만 본 연구에서는 ORP, ROS, 표면 단백질 구조 등을 직접 분석하지 않았으므로, L-시스테인의 구체적인 작용 기전 규명을 위해서는 향후 산화환원 지표 및 표면 단백질 관련 추가 분석이 필요하다.
4. 최적 탄소원 농도
앞서 확립한 배지 조성(BC)을 바탕으로 포도당 농도를 3%(BC3)와 5%(BC5)로 달리하여 5 L jar fermenter에서 L. rhamnosus L22-FR28을 배양한 결과, 고농도 포도당 조건에서 최종 세포 증식이 유의하게 증가하였다(Fig. 3). 두 조건 모두에서 배양 시간이 경과함에 따라 OD600와 생균수가 증가하다가 배양 후반부에 정체 양상을 보였으며, 유효 배양시간은 BC3에서 9 hr, BC5에서 10.5 hr로, 포도당 농도 5% 조건에서 대수증식기가 1.5 hr 연장되었다. OD600은 배양 3 hr에서는 BC3와 BC5 간 유의한 차이가 확인되지 않았으나, 배양 6, 7 hr에서는 BC3가 BC5보다 유의하게 높았고, 배양 9 hr에는 BC5가 BC3보다 유의하게 높게 확인되었다(p<0.05). 배양 종료 시점에서 OD600은 BC3 1.0780±0.0029, BC5는 1.4630±0.0003으로 BC5에서 유의적으로 높았다(p<0.05). 생균수도 OD600와 유사한 경향을 보여, 배양 3 hr에서 BC3(9.20 × 10⁷ CFU/mL)와 BC5(8.87 × 10⁷ CFU/mL)는 통계적으로 차이가 없었으나, 배양 6, 7, 9 hr에는 BC3가 BC5보다 유의하게 높은 값을 보였다(p<0.05). 배양 종료 시점에는 BC3 7.93 × 109 CFU/mL, BC5 1.35 × 1010 CFU/mL로 BC5에서 1.7배 높은 세포밀도가 확인되었다. 따라서 포도당 농도를 5%로 증가시키면 초기–중기 배양 단계에서는 BC3와 유사하거나 다소 낮은 생육을 보이지만, 기질 공급이 더 오래 유지되면서 대수증식기가 연장되어 최종 생체량이 유의적으로 증가하는 것으로 판단된다.
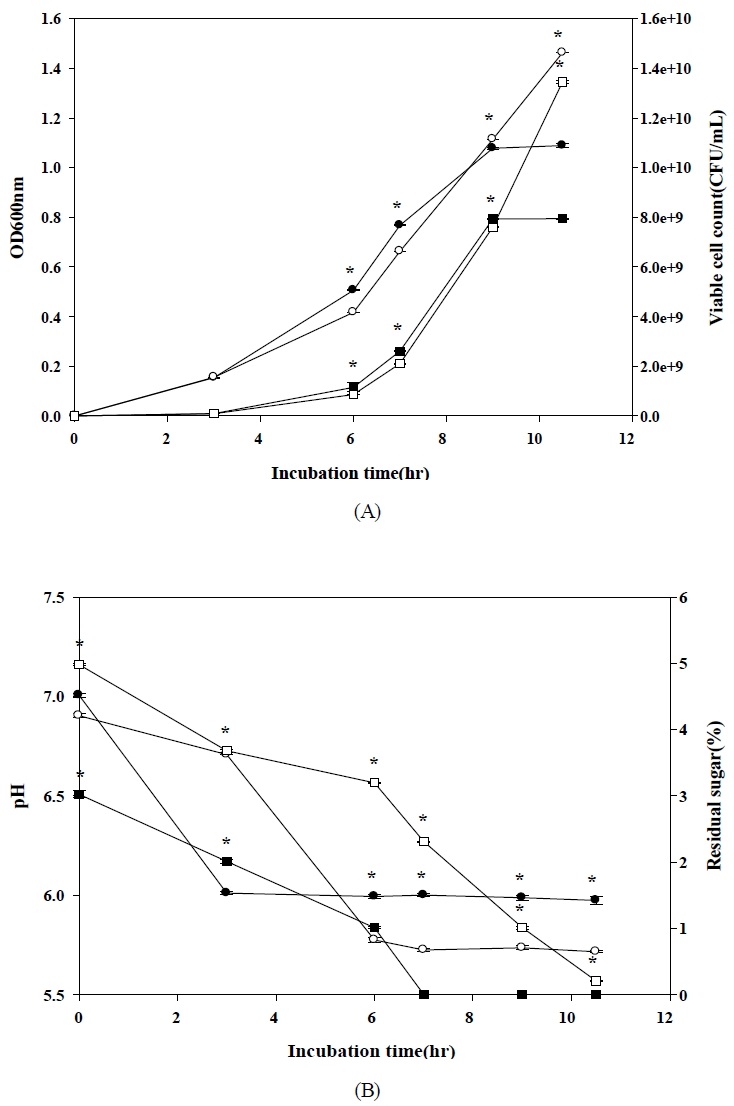
Growth curve and viable cell counts (A), and changes in pH and residual sugar (B) of L. rhamnosus L22-FR28 cultivated in BC3 and BC5 medium. (A) -●-, OD600 in BC3; -○-, OD600 in BC5; -■-, viable cell counts in BC3; -□-, viable cell counts in BC5. (B) -●-, pH in BC3; -○-, pH in BC5; -■-, residual sugar in BC3; -□-, residual sugar in BC5. Asterisks indicate significant differences between BC3 and BC5 at the same incubation time (p<0.05).
배양 시간 동안 잔당(포도당) 농도와 pH 변화를 모니터링한 결과(Fig. 3B), 두 조건 모두에서 배양이 진행됨에 따라 포도당과 pH가 감소하다가, 대수증식기 종료 이후에는 잔당과 pH 감소가 둔화되는 양상을 보였다. pH에 대한 일원분산분석 결과, 전 시간대에서 BC3와 BC5 간 pH 차이는 모두 통계적으로 유의하였다(p<0.05). 초기에는 두 조건 모두 pH 6.5 부근에서 배양이 시작되었으나, 배양이 진행될수록 BC5에서 pH가 5.7 내외까지 더 빠르게 감소하여 고농도 포도당 조건에서 유산 생성이 보다 활발하게 진행된 것으로 예상된다. 두 처리구 모두 발효 후반까지 pH 5.7∼6.0 범위로 제어되었으며, 이는 젖산균의 성장과 산 저해 간 균형에 유리한 범위로 알려져 있으며(Papadimitriou K 등 2016), 본 연구 결과에서도 두 처리 모두에서 장기간 고세포밀도 상태가 유지되는데 기여한 것으로 사료된다. 잔당(포도당) 변화에 대한 일원분산분석 결과, 모든 시간점에서 BC3와 BC5 간 잔당 농도 차이는 통계적으로 매우 유의하였다(p<0.05). 초기 잔당은 BC3가 약 3.0%, BC5가 약 5.0%로 BC5가 더 높았으며, 배양시간이 증가할수록 두 조건 모두 잔당이 감소하였다. BC3는 7 hr 이후 잔당이 거의 0.00%까지 소모된 반면, BC5는 7 hr에 2.31%, 10.5 hr에 0.23%의 잔당이 남아 있어 더 오랜 기간 동안 기질이 공급되는 양상을 보였다. 즉, BC3 조건에서는 세포가 비교적 빠르게 기질을 소모하여 6∼9 hr에 높은 OD600와 생균수를 보이나 이후 증식이 정체되는 반면, BC5 조건에서는 기질이 장시간 존재함에 따라 대수증식기가 지연 종료되고 최종 세포 밀도가 더 높게 유지되는 것으로 해석된다. 이는 유산균 고세포밀도 배양에서 충분한 기질 공급과 적절한 pH 제어가 최종 생체량과 수율을 증가시킨다는 선행 연구(Schiraldi C 등 2003; Papadimitriou K 등 2016)와도 일치한다. 따라서 L. rhamnosus L22-FR28의 고세포밀도 생산을 위해서는 포도당 농도를 5% 수준으로 설정하고 pH를 5.7 전후에서 제어하는 공정 조건이 유효한 조합으로 판단되며, 향후 파일럿 규모 이상의 스케일업에서 탄소원 공급 전략 및 pH 제어 조건을 설계하는 데 기초 자료로 활용될 수 있을 것으로 판단된다.
5. L. rhamnosus L22-FR28 동결건조 후 회수량 및 생존율
배양 조건에 따른 균체 회수량과 동결건조 분말의 생산성을 비교한 결과는 Table 3에 제시하였다. 1 L 배양액 기준으로 회수된 습중량 균체는 BC3에서 31.25±0.29 g, BC5에서 39.97±0.43 g으로 BC5가 BC3보다 약 1.28배 높았으며, 동결건조 후 회수된 건조 분말량은 BC3에서 26.57±0.49 g, BC5에서 29.45±0.38 g으로 BC5가 BC3보다 약 1.11배 높았으나 이 차이는 습중량 차이에 비해 상대적으로 작았다. 이는 동일 부피 기준으로 회수된 세포의 양은 BC5에서 더 많았지만, 동결건조 과정에서 수분과 용질이 제거된 이후의 순수 균체 고형물 비율은 두 조건에서 크게 다르지 않은 것으로 추정된다. 배양액의 생균수는 BC3에서 (7.93±0.28) × 109 CFU/mL, BC5에서 (1.35±0.04) × 1010 CFU/mL로, BC5 조건이 BC3에 비해 약 1.70 배 높은 세포 밀도를 보였다(p<0.05). 동결건조 후 분말 1 g당 생균수는 BC3에서 (1.91±0.14) × 1011 CFU/g, BC5에서 (3.74±0.12) × 1011 CFU/g으로, BC5에서 약 1.96배 높은 유효균수가 확인되었고(p<0.05), 생존율은 BC3가 63.88±3.66%, BC5가 81.66±1.26%로 BC5가 약 1.28배 높음을 확인하였다(p<0.05). 이러한 결과는 배양 단계에서 형성된 세포의 생리적 상태와 초기 생균수가 동결건조 후 생존율과 최종 제형의 유효균수에 직접적인 영향을 미친다는 선행 연구 결과와도 일치한다(Siaterlis A 등 2009; Jofré A 등 2015; Tyagi N 등 2023).
선행 연구들에 따르면, 영양 제한 조건이나 적절하지 않은 배양 환경에서 증식한 세포는 내재 저장물질 축적이 부족하고 스트레스 보호 기작이 충분히 유도되지 않아, 동결건조 및 저장 과정에서 사멸이 증가하는 경향을 보이는 것으로 보고되고 있다(Siaterlis A 등 2009; Celik OF & O’Sullivan DJ 2013). 반면 적정한 탄소·질소원 공급과 pH 제어 하에서 배양된 세포는 막 성분, 보호성 솔루트, 스트레스 관련 단백질이 상대적으로 잘 유지되어 동결건조 후 생존율이 높아지는 것으로 알려져 있으며, 동결보호제를 적용할 경우 장기 저장 중에도 높은 생존율을 유지할 수 있다는 보고가 다수 제시되어 있다(Peighambardoust SH 등 2011; Jofré A 등 2015; Noufeu T 등 2025). 본 연구에서 BC3와 BC5에 동일한 동결보호제를 적용했음에도 BC5에서 더 높은 생존율이 관찰된 것은 보호제 조성의 차이보다는 고농도 기질 조건에서 배양된 세포의 생리·대사 상태 차이가 동결건조 내성 차이에 기여했을 가능성을 시사한다. 또한 프로바이오틱 제품은 가공-유통-저장 전 과정에서 충분한 생존율이 유지되어야 하므로, 초기 균체량(CFU/g)의 극대화와 적절한 동결보호제 및 포장체계 설계가 품질 관리의 핵심 요소로 강조되고 있다(Jofré A 등 2015; Wang J & Chen L 2021). 동결건조된 유산균 분말은 일반적으로 저온·저수분활성 조건에서는 수개월 이상 안정하지만, 상온에서 고수분·고온·산소에 노출될 경우 활성이 빠르게 감소하는 것으로 보고되고 있어(Peighambardoust SH 등 2011; Jofré A 등 2015), 저장 및 유통 전 과정에서 온도와 수분활성, 산소 노출을 적정 수준으로 관리하는 것이 중요하다. 본 연구에서 확보한 BC5 조건은 1 L 배양액 기준 3.74 × 1011 CFU/g 수준의 고농도 분말 생산과 80% 이상(81.66%)의 생존율을 동시에 달성함으로써, 산업 현장에서 요구되는 프로바이오틱 유효균수 기준을 충족할 수 있는 잠재력을 보여준다. 향후에는 BC5 조건을 기반으로 파일럿 규모 이상의 스케일업 및 장기 저장 시험을 수행하여, 실제 제품 수준에서의 안정성과 적용 가능성을 추가로 검증할 필요가 있다.
결 론
영아분변 유래 유산균 Lacticaseibacillus rhamnosus L22-FR28의 산업적 활용을 목표로 배양 및 동결건조 공정을 최적화한 결과, 고농도의 생균 세포를 높은 생존율로 분말화할 수 있는 생산 조건을 확립하였다. 최적 배지 조성은 포도당 5%, 펩톤 1%, 효모추출물 2.5%, L-시스테인 0.1% 등을 포함하였으며, pH 5.7로 제어한 5 L jar fermenter에서 10∼12 hr 배양 시 1011 CFU/mL 수준의 고세포밀도 균체를 생산하였다. L-시스테인 첨가군은 무첨가군에 비해 배양 종료 시점의 생균수와 흡광도(OD600)가 높고 세포 응집이 감소하는 양상을 보여, L. rhamnosus L22-FR28의 배양 단계에서 세포 밀도와 균일한 분산 상태를 확보하는데 이점을 제공하는 것을 확인하였다. 또한 포도당 농도를 3%에서 5%로 증가시켰을 때 세포 증식과 분말 수율이 모두 향상되었으며, 동결건조 공정에서 80% 이상 생존율을 확보하였다. 최종 생산된 L. rhamnosus L22-FR28 분말은 3.72 × 1011 CFU/g 수준의 생균을 함유하여, 실제 제형 설계 시 1회 섭취량당 충분한 유효균수 확보가 가능할 것으로 판단된다. 본 연구에서 제시한 배지 및 공정 조건은 동일 균주의 특성을 유지하면서 파일럿 규모 이상의 대량생산 공정에 적용할 수 있는 잠재력을 가지며, 향후 스케일업 및 장기 저장 안정성 평가를 통해 산업적 활용성을 추가적으로 검증할 필요가 있다. 또한 본 결과는 유사한 L. rhamnosus 계열 프로바이오틱 유산균의 배양 및 분말화 공정을 개선하는 데에도 참고 자료로 활용될 수 있을 것으로 사료된다.
Acknowledgments
본 연구는 농촌진흥청 국립식량과학원 기관고유사업(과제번호: PJ01599303)의 지원에 의해 이루어진 것으로, 연구비 지원에 감사드립니다.
REFERENCES
-
Amin MdR, Biswas AP, Tasnim M, Islam MdN, Azam MdS (2025) Probiotics and their applications in functional foods: A health perspective. Appl Food Res 5(2): 101193.
[https://doi.org/10.1016/j.afres.2025.101193]

-
Burca-Busaga CG, Betoret N, Seguí L, Betoret E, Barrera C (2020) Survival of Lactobacillus salivarius CECT 4063 and stability of antioxidant compounds in dried apple snacks as affected by the water activity, the addition of trehalose and high pressure homogenization. Microorganisms 8(8): 1095.
[https://doi.org/10.3390/microorganisms8081095]

-
Carvalho AS, Silva J, Ho P, Teixeira P, Malcata FX, Gibbs P (2004) Relevant factors for the preparation of freeze-dried lactic acid bacteria. Int Dairy J 14(10): 835-847.
[https://doi.org/10.1016/j.idairyj.2004.02.001]

-
Celik OF, O’Sullivan DJ (2013) Factors influencing the stability of freeze-dried stress-resilient and stress-sensitive strains of bifidobacteria. J Dairy Sci 96(6): 3506-3516.
[https://doi.org/10.3168/jds.2012-6327]

-
Choi GH, Lee NK, Paik HD (2021) Optimization of medium composition for biomass production of Lactobacillus plantarum 200655 using response surface methodology. J Microbiol Biotechnol 31(5): 717-725.
[https://doi.org/10.4014/jmb.2103.03018]

-
Cui S, Hu M, Sun Y, Mao B, Zhang Q, Zhao J, Tang X, Zhang H (2022) Effect of trehalose and lactose treatments on the freeze-drying resistance of lactic acid bacteria in high-density culture. Microorganisms 11(1): 48.
[https://doi.org/10.3390/microorganisms11010048]

-
Dave RI, Shah NP (1997) Effect of cysteine on the viability of yoghurt and probiotic bacteria in yoghurts made with commercial starter cultures. Int Dairy J 7(8-9): 537-545.
[https://doi.org/10.1016/S0958-6946(97)00053-8]

-
Feng T, Wang J (2020). Oxidative stress tolerance and antioxidant capacity of lactic acid bacteria as probiotic: A systematic review. Gut microbes 12(1): 1801944.
[https://doi.org/10.1080/19490976.2020.1801944]

-
Fenster K, Freeburg B, Hollard C, Wong C, Rønhave Laursen R, Ouwehand AC (2019) The production and delivery of probiotics: A review of a practical approach. Microorganisms 7(3): 83.
[https://doi.org/10.3390/microorganisms7030083]

-
Fonseca F, Cenard S, Passot S (2014) Freeze-drying of lactic acid bacteria. pp 477-488. In: Cryopreservation and freeze-drying protocols. Fuller BJ, Lane N, Benson EE (eds). Springer, New York, NY, USA.
[https://doi.org/10.1007/978-1-4939-2193-5_24]

-
Hajzer ZE, Alibrahem W, Helu NK, Oláh C, Prokisch J (2025) Functional foods in clinical trials and future research directions. Foods 14(15): 2675.
[https://doi.org/10.3390/foods14152675]

-
Jeong SG, Choi IS, Kim HM, Chang JY, Park HW (2022) Supercooling pretreatment improves the shelf-life of freeze-dried Leuconostoc mesenteroides WiKim32. J Microbiol Biotechnol 32(12): 1599-1604.
[https://doi.org/10.4014/jmb.2209.09022]

-
Jofré A, Aymerich T, Garriga M (2015) Impact of different cryoprotectants on the survival of freeze-dried Lactobacillus rhamnosus and Lactobacillus casei/paracasei during long-term storage. Benef Microbes 6(3): 381-386.
[https://doi.org/10.3920/BM2014.0038]

-
Leroy F, Vuyst LD (2001) Growth of the bacteriocinproducing Lactobacillus sakei strain CTC 494 in MRS broth is strongly reduced due to nutrient exhaustion: A nutrient depletion model for the growth of lactic acid bacteria. Appl Environ Microbiol 67(10): 4407-4413.
[https://doi.org/10.1128/AEM.67.10.4407-4413.2001]

-
Liu B, Yang M, Qi B, Chen X, Su Z, Wan Y (2010) Optimizing L-(+)-lactic acid production by thermophile Lactobacillus plantarum As.1.3 using alternative nitrogen sources with response surface method. Biochem Eng J 52(2-3): 212-219.
[https://doi.org/10.1016/j.bej.2010.08.013]

-
Liu X, Liu K, Yang J, Qiao H, Kwok LY, Zhang W (2025) Exploring the metabolic dynamics, storage stability, and functional potential of Lacticaseibacillus rhamnosus Probio-M9-fermented milk. J Dairy Sci 108(2): 1339-1350.
[https://doi.org/10.3168/jds.2024-25632]

-
Mendonça AA, Pinto-Neto WP, da Paixão GA, Santos DDS, De Morais MA Jr, De Souza RB (2022) Journey of the probiotic bacteria: Survival of the fittest. Microorganisms 11(1): 95.
[https://doi.org/10.3390/microorganisms11010095]

-
Meng XC, Stanton C, Fitzgerald GF, Daly C, Ross RP (2008) Anhydrobiotics: The challenges of drying probiotic cultures. Food Chem 106(4): 1406-1416.
[https://doi.org/10.1016/j.foodchem.2007.04.076]

-
Miller GL (1959) Use of dinitrosalicylic acid reagent for determination of reducing sugar. Anal Chem 31(3): 426-428.
[https://doi.org/10.1021/ac60147a030]

-
Noufeu T, Li Y, Toure NF, Yao H, Zeng X, Du Q, Pan D (2025) Overview of glycometabolism of lactic acid bacteria during freeze-drying: Changes, influencing factors, and application strategies. Foods 14(5): 743.
[https://doi.org/10.3390/foods14050743]

-
Papadimitriou K, Alegría Á, Bron PA, de Angelis M, Gobbetti M, Kleerebezem M, Lemos JA, Linares DM, Ross P, Stanton C, Turroni F, van Sinderen D, Varmanen P, Ventura M, Zúñiga M, Tsakalidou E, Kok J (2016) Stress physiology of lactic acid bacteria. Microbiol Mol Biol Rev 80(3): 837-890.
[https://doi.org/10.1128/MMBR.00076-15]

-
Passot S, Cenard S, Douania I, Tréléa IC, Fonseca F (2012) Critical water activity and amorphous state for optimal preservation of lyophilised lactic acid bacteria. Food Chem 132(4): 1699-1705.
[https://doi.org/10.1016/j.foodchem.2011.06.012]

-
Peighambardoust SH, Tafti AG, Hesari J (2011) Application of spray drying for preservation of lactic acid starter cultures: A review. Trends Food Sci Technol 22(5): 215-224.
[https://doi.org/10.1016/j.tifs.2011.01.009]

-
Rodrigues D, Sousa S, Rocha-Santos T, Silva JP, Sousa Lobo JM, Costa P, Amaral MH, Pintado MM, Gomes AM, Malcata FX, Freitas AC (2011) Influence of L-cysteine, oxygen and relative humidity upon survival throughout storage of probiotic bacteria in whey protein-based microcapsules. Int Dairy J 21(11): 869-876.
[https://doi.org/10.1016/j.idairyj.2011.05.005]

- Santiesteban-López A, López-Malo JJ, Gomez-Diaz B, Armendariz P (2013) Effect of L-cysteine and ascorbic acid on the propagation of Lactobacillus casei in milk. Int Res J Microbiol 4: 113-118.
-
Santivarangkna C, Kulozik U, Foerst P (2008) Inactivation mechanisms of lactic acid starter cultures preserved by drying processes. J Appl Microbiol 105(1): 1-13.
[https://doi.org/10.1111/j.1365-2672.2008.03744.x]

-
Schiraldi C, Adduci V, Valli V, Maresca C, Giuliano M, Lamberti M, Cartenì M, De Rosa M (2003) High cell density cultivation of probiotics and lactic acid production. Biotechnol Bioeng 82(2): 213-222.
[https://doi.org/10.1002/bit.10557]

-
Segers ME, Lebeer S (2014) Towards a better understanding of Lactobacillus rhamnosus GG-host interactions. Microb Cell Fact 13(suppl 1): S7.
[https://doi.org/10.1186/1475-2859-13-S1-S7]

-
Siaterlis A, Deepika G, Charalampopoulos D (2009) Effect of culture medium and cryoprotectants on the growth and survival of probiotic lactobacilli during freeze drying. Lett Appl Microbiol 48(3): 295-301.
[https://doi.org/10.1111/j.1472-765X.2008.02529.x]

-
Sin PY, Tan SH, Asras MFF, Lee CM, Lee TC (2024) Probiotic growth pattern and physicochemical evaluation of water kefir fermentation. Malays Appl Biol 53(2): 21-30.
[https://doi.org/10.55230/mabjournal.v53i2.2742]

-
Soro-Yao AA, Aka S, Thonart P, Djè KM (2014) Assessment of the potential of lactic acid bacteria as dried starter culture for cereal fermentation. Open Biotechnol J 8: 1-5.
[https://doi.org/10.2174/1874070701408010001]

-
Tao Z, Yuan H, Liu M, Liu Q, Zhang S, Liu H, Jiang Y, Huang D, Wang T (2022) Yeast extract: Characteristics, production, applications and future perspectives. J Microbiol Biotechnol 33(2): 151-166.
[https://doi.org/10.4014/jmb.2207.07057]

-
Tyagi N, Gidlöf Z, Osanlóo DT, Collier ES, Kadekar S, Ringstad L, Fureby AM, Roos S (2023) The impact of formulation and freeze drying on the properties and performance of freeze-dried Limosilactobacillus reuteri R2LC. Appl Microbiol 3(4): 1370-1387.
[https://doi.org/10.3390/applmicrobiol3040092]

-
Wang J, Chen L (2021) Impact of a novel nano-protectant on the viability of probiotic bacterium Lactobacillus casei k17. Foods 10(3): 529.
[https://doi.org/10.3390/foods10030529]

-
Wang S, Li L, Yu L, Tian F, Zhao J, Zhai Q, Chen W (2024) Natural aggregation of Lactobacillus: Mechanisms and influencing factors. Food Biosci 62: 105007.
[https://doi.org/10.1016/j.fbio.2024.105007]

-
Wang T, Lu Y, Yan H, Li X, Wang X, Shan Y, Yi Y, Liu B, Zhou Y, Lü X (2020) Fermentation optimization and kinetic model for high cell density culture of a probiotic microorganism: Lactobacillus rhamnosus LS-8. Bioprocess Biosyst Eng 43(3): 515-528.
[https://doi.org/10.1007/s00449-019-02246-y]

-
Weitzel MLJ, Vegge CS, Pane M, Goldman VS, Koshy B, Porsby CH, Burguière P, Schoeni JL (2021) Improving and comparing probiotic plate count methods by analytical procedure lifecycle management. Front Microbiol 12: 693066.
[https://doi.org/10.3389/fmicb.2021.693066]

-
Zawistowska-Rojek A, Tyski S (2018) Are probiotic really safe for humans? Pol J Microbiol 67(3): 251-258.
[https://doi.org/10.21307/pjm-2018-044]