자색옥수수 포엽 추출물의 지표성분 Cyanidin-3-O-Glucoside 분석법 유효성 검증
 ; Hyo-Young Lee1
; Hyo-Young Lee1 ; Jae-Gil Lim1
; Jae-Gil Lim1 ; Jae-Hee Lee1
; Jae-Hee Lee1 ; Du-Eun Kim1
; Du-Eun Kim1 ; Hye-Jeong Kwon2
; Hye-Jeong Kwon2 ; Nam Yong Um2
; Nam Yong Um2 ; Min Namgung3
; Min Namgung3 ; Hee-Yeon Kim4, †
; Hee-Yeon Kim4, †
Abstract
Cyanidin-3-O-glucoside (C3G) was selected as a marker compound to standardize the husk extract of purple corn for potential applications in food and functional ingredient development. An analytical method for C3G was established and validated using high-performance liquid chromatography with photodiode array detection (HPLC-PDA). The method showed specificity because the retention time and spectrum of the C3G standard solution matched those of the purple corn husk extract. The method showed high specificity because the retention time and UV spectrum of the C3G standard solution were consistent with those of the purple corn husk extract. The calibration curve showed excellent linearity with a correlation coefficient (R²) greater than 0.9999. The limits of detection (LOD) and quantification (LOQ) were 0.065 μg/mL and 0.197 μg/mL, respectively. Intra-day analysis revealed accuracies ranging from 91.73% to 101.06% and precision with relative standard deviations (RSDs) of 2.54%-3.96%. Inter-day analysis showed accuracies between 96.89% and 99.25% with RSDs of 2.20%-3.53%. The recovery rates of C3G at different concentrations ranged from 97.78% to 100.94%, with RSDs below 1%. These results suggest that the established HPLC method is reliable and suitable for the quantitative analysis and standardization of C3G in purple corn husk extract.
Keywords:
purple corn, anthocyanin, C3G, HPLC-analysis, validation서 론
자색옥수수는 남아메리카 페루 등 안데스 지역이 원산지로 식물체의 알곡, 속대, 포엽, 줄기 등의 부위에 보라색이 발현되는 유색 옥수수 품종이다. 국내 자색옥수수 육성 품종은 자색 찰옥수수 품종인 청춘찰(Park KJ 등 2016), 흑진주찰(Jung TW 등 2009), 얼룩찰1호(Lee JS 등 2011) 등이 있으며 자색 찰옥수수는 일반 찰옥수수와 같이 풋옥수수로 소비하기 위하여 개발되었다. 강원특별자치도 농업기술원에서는 유색 찰옥수수 이외 안토시아닌 색소 고함량 기능성 종실용 자색옥수수를 육성하고 고유 품종을 개발하였다. 자색옥수수 색소 2호와 색소 4호는 옥수수의 이삭을 감싸고 있는 포엽과 속대, 알곡에 흑자색이 발현되는 품종으로(Choi JK 등 2017), 색소 알곡의 기능성 소재 활용을 위하여 고시형 식품원료 및 기능성 표시 식품과 병행하여 혈당개선 효과 등 기능성 식품 개발 연구를 추진하고 있다. 색소 1호와 색소 5호는 자색 포엽과 속대를 활용하기 위하여 개발된 품종이다(Kim HY 등 2021). 국내 옥수수 포엽은 식품원료로 등록되어 있지 않아 섭취 불가하며 가공 식품용도로도 사용할 수 없다. 강원 고유 품종 자색옥수수의 포엽과 속대를 식품원료 및 건강기능식품 원료로 사용하기 위하여 식약처 『식품 등의 한시적 기준 및 규격 인정 기준』 제도에 따라 포엽 및 속대 혼합추출물과 포엽 추출물을 개발하고 독성시험 수행을 통하여 자색옥수수 추출물의 안전성을 입증하였다. 포엽 및 속대 혼합 추출물은 식품공전에 “한시적 기준·규격에서 전환된 원료”로 등재되어 있고 포엽 추출물은 2024년 한시적 식품원료로 승인받았다.
자색옥수수의 함유되어 있는 주요 천연 색소인 안토시아닌은 C6-C3-C6의 기본 골격 구조를 갖는 플라보노이드 계열 화합물에 속한다. 기본 골격에 연결되어 있는 수산기의 종류와 위치, 메틸화 정도, aglycone인 안토시아니딘(anthocyanidin)에 결합된 당의 종류와 수에 따라 안토시아닌의 종류가 달라진다(Li CY 등 2008). 안토시아닌은 안토시아니딘에 당이 글리코사이드 결합을 이루는 배당체이다. 안토시아닌의 기본 구조가 되는 안토시아니딘 종류는 cyanidin, delphinidin, malvidin, pelargonidin, peonidin, petunidin 등이 있으며 식물 내 존재하는 주요 천연 안토시아닌으로 알려져 있다(Tan J 등 2019). 안토시아니딘과 결합되는 당의 종류와 위치에 따라 다양한 배당체가 존재하며 cyanidin-3-O-glucoside(C3G)는 가장 보편적으로 알려진 cyanidin의 배당체이다. 이러한 glycoside 결합으로 존재하는 안토시아닌 배당체는 다양한 생리활성을 나타낸다(Kong JM 등 2008; Khoo HE 등 2017).
자색옥수수 포엽과 속대에서 cyanidin-3-O-glucoside(C3G), pelargonidin-3-O-glucoside(Pg3G), peonidin-3-O-glucoside(P3G) 등 10종의 안토시아닌이 분리되었으며 이중 C3G의 상대적 함량은 포엽 39.8%, 속대 20.9%이었다(Li CY 등 2008). 자색옥수수 알곡 추출물에서 C3G를 포함하여 Pg3G, P3G 등 총 4종의 안토시아닌이 검출되었으며 이 중 C3G의 함량이 총안토시아닌 대비 약 39%인 것으로 확인되었다(Chuntakaruk H 등 2021). 국내 육성 품종인 “흑진주찰”의 주요 안토시아닌도 C3G이며(Kim JT 등 2020), 페루, 볼리비아, 중국 등에서 재배되는 자색옥수수의 포엽, 속대, 알곡의 주요 안토시아닌이 C3G인 것으로 보고되었다(Cai T 등 2023). 천연 안토시아닌 C3G는 강력한 항산화 및 항염증 작용을 기반으로 혈관 질환, 지방간 및 염증성 장 질환, 포도당-지질 대사 장애와 같은 만성 대사 질환을 예방하는 효능이 있다(Tan J 등 2019). 또한, 지질 합성 저해 및 지방산 산화 촉진을 통한 지질대사 조절, GLUT-1과 GLUT-4의 발현 및 인슐린 저항성 개선 효과도 검증되었다(Oumeddour DZ 등 2024). 최근 연구에 따르면 C3G 투여는 뇌를 보호하고 인지 행동 능력을 개선시키는 것으로 보고되었다(Baek H 등 2023).
국내 자색옥수수 관련 연구(Lee KY 등 2018; Kim HY 등 2021)에서 C3G의 함량 측정에 따른 품질분석 및 기능성 평가에 대하여 보고되었고, Guo LC 등(2023)과 Kim MK(2025)의 연구와 같이 자색옥수수가 아닌 다른 식물에 함유되어 있는 C3G의 정량과 분석법 밸리데이션이 보고되었으나 포엽 등 자색옥수수의 특정 부위에 대한 원료 표준화를 목적으로 수행된 C3G 분석법 밸리데이션에 대한 연구는 미흡한 실정이다. 자색옥수수 포엽 추출물은 원료명 ‘옥수수 포엽 주정 추출 분말’로 식약처 『식품 등의 한시적 기준 및 규격 인정 기준』을 인정받았다. 옥수수는 특성에 따라 품종으로 구별되지만 학명은 품종 구별 없이 모두 Zea mays L.로 같은 식물종에 속하기 때문에 원료명에 ‘자색옥수수’ 표기가 불가하다. 따라서 일반 옥수수 포엽과 구별하기 위한 지표성분 설정이 반드시 필요하며 자색옥수수와 일반 옥수수를 구별하기 위한 지표성분으로 안토시아닌 색소의 존재 여부와 그 함량을 확인할 수 있어야 한다.
천연물의 기능성 원료 개발 단계에서 원료 표준화는 원료 생산 및 제조 과정에 사용된 기술과 정보들을 기록하고 관리하여 개발된 원료의 생산 배치(Batch)와 상관없이 품질을 일정하게 유지하는 것을 의미한다. 기능성 원료의 표준화를 위하여 지표성분을 설정하고 분석법을 확립하여 원료에 대한 기준 규격 관리가 요구된다(Korea Food & Drug Administration(KFDA) 2007; Jang GW 등 2018). 지표성분은 화학적 안정성과 분석 용이성을 고려하여 원료를 대표할 수 있는 성분으로 설정하고, 원료의 효능과 성분의 효능이 유사할 시 원료의 기능 성분을 지표성분으로 설정할 수 있다. 이때 지표성분으로 설정된 기능 성분은 원료의 효능과 해당 성분의 농도 간 상관성이 보장되어야 한다. 설정된 지표성분 분석을 통하여 원료의 기준 규격을 설정하고 관리할 수 있으며, 재현성과 신뢰성이 높은 분석치를 얻을 수 있는 분석법 확립 및 과학적 검증과정이 필요하다(Kim Y 등 2012). 본 연구에서는 자색옥수수 포엽 추출물의 기능성 원료 품질관리를 위한 지표성분을 주요 안토시아닌 성분인 C3G로 설정하였다. 이에 따라 범용적 분석 장비인 HPLC를 이용한 분석법 확립 및 유효성 검증(validation)을 수행하여 자색옥수수 원료의 표준화 기반을 마련하고 기능성 식품 및 산업 소재로의 활용 가능성을 제시하고자 한다.
재료 및 방법
1. 실험재료
본 연구에는 자색옥수수 포엽 추출물을 제조하기 위하여 2023년 재배된 색소5호 품종을 사용하였다. 자색옥수수를 수확 후 수염과 외피를 제거하고 포엽을 분리한 다음 냉풍제습건조기(TJHP-1003, Joongang Precision Co., Ltd, DaeGu, Korea) 40℃에서 건조 후 분쇄하여 추출시료로 사용하였다. 포엽 건조분말시료 500 g에 30% 에탄올(Merck Co., Kenilworth, NJ, USA)을 10 L 첨가하고 12시간 동안 상온 교반하여 2회 반복 추출하였다. 추출액을 여과하여 감압농축하고 부형제로 20∼30% dextrin(GLUCIDEX-12, Roquette Freres, Lestrem, France)을 첨가한 다음 분무건조(MH-60, Mihyeon Engineering Co., Ltd, Anyang, Korea)하여 분석법 밸리데이션 시료로 사용하였다. 제조된 3 lot의 포엽 분무건조 추출물을 각각 20 mg씩 정확하게 칭량하고 0.1% citric acid(Sigma Chemical Co., St, Louis, MO, USA)를 포함한 30% 에탄올 100 mL을 가하여 최종농도가 2 mg/mL이 되도록 재용해 한 다음 직경 15mm, 기공 크기(pore size) 0.45 μm인 membrane filter(Sartorius, Goettingen, Germany에 통과시켜 HPLC 분석용 시료로 사용하였으며 모든 분석은 3회 반복 실시하였다. 분석용 시약과 용매는 HPLC 등급을 사용하였다.
2. 표준용액 조제
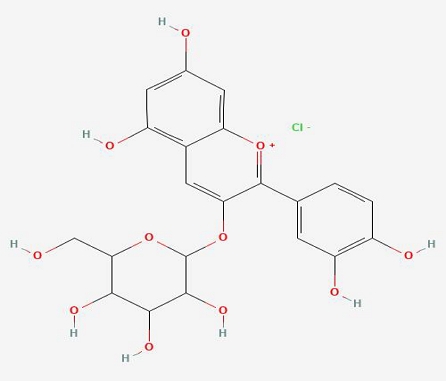
분석을 위한 표준물질인 cyanidin-3-O-glucoside(Fig. 1)는 PhytoLab(Vestenbergsgreuth, Germany)사에서 구입하여 사용하였으며 순도는 98%이었다. 표준물질 10 mg에 50 mL 0.1% citric acid가 함유된 30% 에탄올을 첨가하고 용해시켜 200 μg/mL의 농도로 표준원액을 조제하였다. 표준원액을 단계적으로 희석하여 1, 2.5, 5, 7.5, 10 μg/mL 농도의 표준용액을 조제하여 HPLC 분석에 사용하였다. 표준물질의 정량곡선을 작성하고 포엽 추출물의 제조차수별 C3G 함량을 분석하였다.
3. HPLC 분석
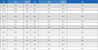
자색옥수수 포엽 추출물 및 C3G 표준용액의 분석은 Nano Space SI-2 HPLC(Shiseido, Tokyo, Japan)를 사용하였다. 컬럼은 Unison UK-C18(150 × 4.6 mm, 3 μm, Imtakt, Kyoto, Japan)을 사용하였고, 0.1% Trifluoroacetic acid(TFA, Sigma Chemical Co., St, Louis, MO, USA)와 100% acetonitrile(Sigma Chemical Co., St, Louis, MO, USA)을 이동상으로 사용하였다. 상기 이동상을 gradient 조건으로 설정하고 photo diode array 검출기(PDA, Nanosapace, Shiseido, Tokyo, Japan) 525 nm에서 분석하였다. 시료 주입량 5 μL, 컬럼 온도 35℃, 유속 1 mL/min, 분석 시간은 30분이었다(Table 1).
4. 분석법 검증(Method Validation)
정확하고 신뢰성 있는 분석 데이터 확보를 위하여 ‘의약품등 분석법의 벨리데이션 가이드(KFDA 2007)’를 참고하여 지표성분 C3G의 농도별 표준용액을 HPLC로 분석하였으며, 분석 데이터의 특이성(specificity), 직선성(linearity), 검출한계(limit of detection; LOD) 및 정량한계(limit of quantification; LOQ), 정밀성(precision), 정확성(accuracy)을 측정하였다.
특이성은 다양한 성분이 혼재된 시료 중 목표 화합물만을 선택적으로 검출할 수 있는 능력을 의미한다. 본 연구에서는 자색옥수수 포엽 추출액과 C3G 표준용액을 HPLC로 분석하여 머무름 시간(retention time; RT)과 크로마토그램을 비교함으로써, 불순물이나 분해산물에 의한 간섭 없이 분석 대상 성분이 명확히 구분되는지를 확인하였다. 직선성은 분석 대상 물질의 농도에 비례하여 분석장비에서 측정 값이 일정하게 증가하는 정도를 나타낸다. 이를 평가하기 위해 C3G 표준용액의 농도별 피크 면적을 회귀분석하여 검량선을 작성하였고, 결정계수(coefficient of determination; R2)를 산출하여 적합성을 검증하였다. 정량한계(LOQ)와 검출한계(LOD)는 각각 분석법으로 신뢰할 수 있는 최소 정량 농도와 검출 가능한 최소 농도를 의미한다. 표준 검량선의 기울기(S)와 y절편의 표준편차(σ)를 이용하여 아래의 식으로 계산하였다.
- (LOQ = 10 × σ/S, LOD = 3.3 × σ/S, σ : y절편의 표준편차, S : 검량선의 기울기)
정량한계는 설정된 분석법에서 신뢰할 수 있는 정량값을 산출할 수 있는 최소 농도를 의미하며 LOQ 값이 낮을수록 분석 물질에 대한 분석 장비의 감도가 높은 것으로 평가된다. 검출한계는 분석의 신뢰성과 정확성을 가지고 측정 가능한 분석 물질의 최소 농도 또는 그 양을 의미하고, 분석 물질의 존재 여부의 판단 기준이 되며 설정된 시험법에서 얼마나 낮은 농도의 물질을 검출할 수 있는지에 대한 민감도를 나타낸다(Clinical & Laboratory Standards Institute[CLSI] 2012; Chavan SD & Desai DM 2022).
정확성 평가는 동일 농도에서 반복 측정된 값이 실제값(true value)에 얼마나 근접한 지를 백분율로 표현하였다. 농도별 표준용액을 이용하여 일내 분석(intra-day)은 1일 3회 반복 측정하였고, 일간 분석(inter-day)은 동일한 절차를 3일 연속 수행하여 변동성을 검토하였다. 정밀성은 반복 측정 시의 일관성을 평가하는 지표로, 일내 및 일간 분석 결과를 바탕으로 평균값(mean)과 표준편차(SD)를 이용해 상대표준편차(relative standard deviation; RSD)를 산출하였다. 회수율은 시료에 일정 농도의 C3G 표준용액을 첨가한 후 실제 분석을 통해 회수된 양을 측정하여 산출하였다. 표준 검량선에서 직선성이 확인된 1, 5, 10 μg/mL 농도의 표준용액을 자색옥수수 포엽 추출물과 혼합하여 3회 반복 분석하였으며, 이를 통해 평균 회수율과 RSD 값을 계산하였다.
5. 통계분석
모든 시료는 3반복 이상 측정하여 분석하고 분석된 데이터 결과로부터 평균과 표준편차, 상대표준편차를 산출하였다.
결과 및 고찰
1. 자색옥수수 포엽 추출물의 지표성분 설정
식물 기반 기능성 물질은 체내 항산화 및 항염, 면역 증진 및 지질대사 개선 등 다양한 질병의 예방과 효과를 나타내는 천연물로 많은 연구가 진행되고 있다. 식물 내 존재하는 천연물질 등은 매우 다양하고 복잡한 구조를 이루고 있으며 생리활성을 나타내는 물질의 구명과 동정, 화학적 조성을 밝히는 것은 기능성 소재 연구의 한 분야이다(Wang H 등 2003; Kunle OF 등 2012). 식물 기반 기능성 소재 개발에서 효능 검정과 해당 원료가 갖고 있는 생리활성물질의 화학적 조성을 밝히는 연구가 함께 진행되어야 한다(Atanasov AG 등 2021). 농산물을 포함한 식물 원료는 품종, 재배지 및 재배환경, 수확시기 및 수확 후 관리, 추출 조건 등 가공처리에 따라 효능과 화합물의 함량이 달라질 수 있다(Li S 등 2008; Tiwari U & Cummins E 2013; Kumar R 등 2024). 이를 보완하기 위한 지표성분 최적 추출 및 분석법의 표준화가 필요하며(Rural Development Administration[RDA] 2020) 지표성분 함량 및 규격, 시험법 검증은 ‘건강기능식품 기능성 원료 및 기준·규격 인정에 관한 규정’을 준수하여야 한다. 따라서 기능성 원료의 표준화를 위하여 지표성분을 설정하여 일정한 품질과 기능성을 확보하고 설정된 지표성분을 기준으로 한 품질관리 방법이 요구된다(KFDA 2007; Jang GW 등 2018). 앞서 서론에서 기술한 바와 같이 지표성분은 원료가 갖는 기능 성분 중 그 원료를 대표할 수 있는 주요 화합물로 설정할 수 있으며 이때 설정된 지표성분은 분석학적 특이성과 재현성이 확보되어야 한다(Kim Y 등 2012).
자색옥수수는 보통 4월 중순∼말 파종하여 8월 중순에 수확하는데 출사(암술 출현) 후 25∼30일이 수확 적기이다. 자색옥수수 포엽은 일시에 수확된 이삭에서 포엽을 분리, 40℃ 냉풍제습 건조기에서 수분함량 5∼6% 이하로 건조시킨 후 원료로 사용된다. 현재 자색옥수수는 강원 고유 육성 품종으로 농가 계약재배를 통하여 건강기능식품 개발 원료로 공급되고 있다. 자색옥수수 추출물 제조 전 수확 직전 생체 시료를 무작위로 수확하여 건조 시킨 다음 이에 대한 지표성분을 분석하여 건조 원료에 대한 모니터링도 수행하고 있다. 향후 원료 사용량 증가와 산업화 확대 시 건조 원료의 지표성분 함량은 품질의 균일성을 보장하는 관리 기준으로 사용될 수 있으며 이는 고품질 원료의 안정적 확보와 직결되므로 계약재배 생산자와 기업 간의 원료 수매 가격 형성에 주요한 요인이 될 것이라 판단된다.
자색옥수수의 안토시아닌은 C3G, Pg3G, P3G 등 10여 종이 분리, 동정되었다고 보고되었고 실제 자체 분석 결과, C3G를 포함한 7종의 안토시아닌이 HPLC-PDA로 동시 분석이 가능하였다(Fig. 2). 선행 연구에서 밝혀진 바와 같이 자색옥수수 개발 품종 색소 1호와 색소 5호 포엽 추출물에서도 C3G, Pg3G, P3G 등이 검출되었다. 이때 검출된 안토시아닌 중 C3G의 함량은 약 1.8∼2%로 가장 높았으며 이외 주로 검출되는 Pg3G와 P3G는 각각 약 0.37%, 0.93%로 C3G 함량보다 낮게 검출되었다. 추출물을 동시 분석하였을 시 C3G는 Pg3G와 P3G에 비하여 높은 분석 감도를 나타내며 이에 따라 Pg3G와 P3G의 peak는 base line의 영향을 받아 분석 오차가 발생할 확률이 높아진다(Fig. 2(B)). 또한, 건조 원료를 분석할 경우 추출물에 비하여 Pg3G와 P3G 분석 감도는 더 낮을 것이라 예상된다. Pg3G와 P3G의 추출물 내 낮은 검출 감도와 해당 표준품 수급의 용이성 및 비용을 고려하였을 때 자색옥수수의 지표성분으로 적합하지 않았다. 따라서 자색옥수수 포엽 추출물의 지표성분은 기능성과 원료의 품질을 나타내는 대표 단일 성분으로 C3G를 설정하였으며, C3G는 다른 안토시아닌에 비하여 안정적인 것으로 알려져 있어(Haggard S 등 2018) 다성분 지표성분에 비하여 안정적인 분석 결과를 도출할 수 있을 것이라 판단된다. 자색옥수수는 건조 원료 및 추출물에 대한 지표성분 품질관리가 함께 수행되어야 하므로 범용적 장비를 사용하여 신속하고 효율적으로 정량화가 가능한 분석법 개발이 필요하다. 본 연구에서는 C3G의 정량을 위하여 적용하기 쉽고 효율성이 높은 분석법(HPLC-PDA)을 최적화하고 그 유효성을 검증하였다. 유효성이 검증된 지표성분 C3G 분석법을 통하여 제조차수별 추출물의 품질을 관리하고 기능성 원료의 산업적 활용에 있어 과학적 타당성을 제공하고자 한다.
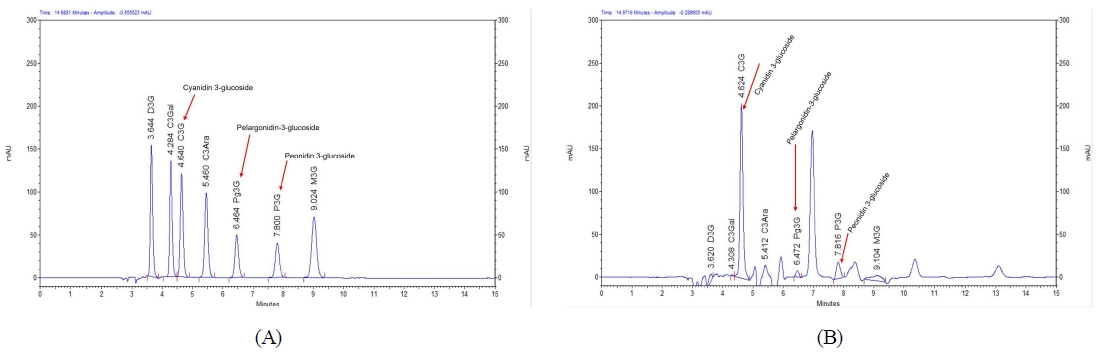
HPLC chromatograms of anthocyanin standards (A) and PCHE (B).D3G: delphinidin-3-O-glucoside, C3Gal: cyanidin-3-O-galactoside.C3G: cyanidin-3-O-glucoside, C3Ara: cyanidin-3-O-arabinoside.Pg3G: pelargonidin-3-O-glucoside, P3G: peonidin-3-O-glucoside.M3G: malvidin-3-O-glucoside.PCHE: purple corn husk extract.
2. 특이성
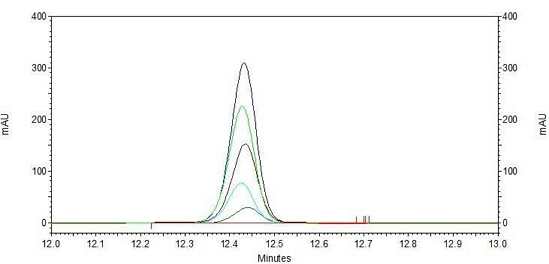
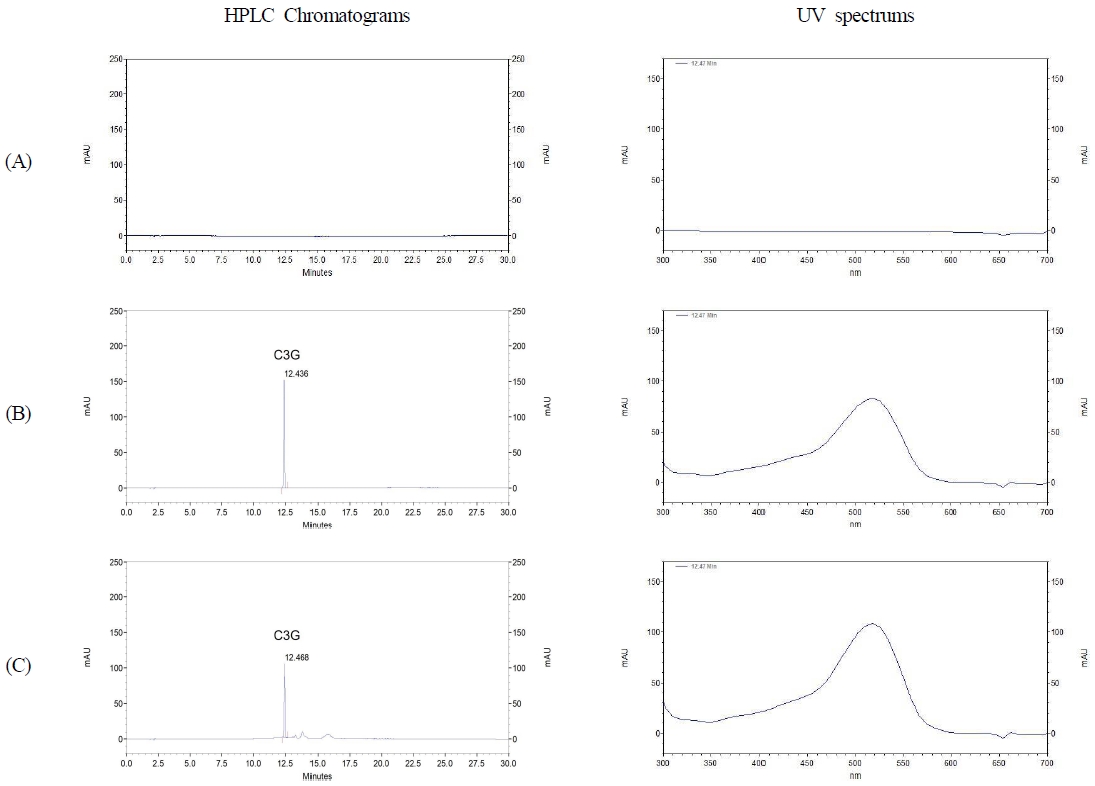
특이성 분석을 위하여 표준물질(C3G)과 포엽 추출물을 0.1% citric acid를 함유한 30% 에탄올에 재용해하여 HPLC로 분석한 다음 크로마토그램에서 해당 물질들의 분리도(resolution)와 RT값을 확인하였다. 분석 결과, C3G는 다른 성분과 간섭없이 단일 peak로 검출되었고 표준용액 농도별로 일정한 RT값에서 검출되었다(Fig. 3). 표준용액과 시험용액의 RT값은 각각 12.436분, 12.468분대로 일치하였다. 또한, 각 용액의 UV spectrum 300∼700 nm 범위에서 동일한 spectrum으로 분석되었으며 525∼530 nm에서 최대 흡수 파장을 나타내어 분석법의 특이성을 확인할 수 있었다(Fig. 4). 지표성분 분석법 밸리데이션 수행을 위하여 시료의 재용해용매로 사용된 에탄올과 증류수의 UV cutoff는 190∼210 nm이며 이 이상의 파장에서는 흡광도가 0에 가깝기 때문에 blank 용매로 적합하다(Lide DR 2005). 안토시아닌의 안정성을 위하여 첨가된 citric acid는 210∼220 nm에서 최대 흡수파장을 나타내기 때문에(Lide DR 2005) C3G 최대 흡수파장인 525∼530 nm에서는 0.1% citric acid를 함유한 30% 에탄올의 용매 peak는 검출되지 않았다. 본 분석법에서 분석 용매의 간섭없이 C3G의 높은 분리도와 정확한 RT값을 확인할 수 있었다.
3. 직선성, 정량한계, 검출한계
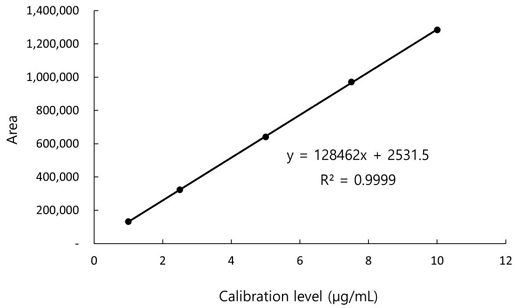
표준용액을 1∼10 μg/mL 농도로 단계적으로 희석한 다음 각 농도별 표준용액을 HPLC를 이용하여 3반복 분석하였다. 분석된 C3G의 농도를 X축, 이를 분석하여 얻어진 peak 면적을 Y축으로 하여 표준 검량곡선을 작성하였다. 이때 검량선의 기울기는 128,462이었고 Y 절편값은 2,531.5로 확인되었으며 상관계수(R2)는 0.9999로 매우 높은 직선성을 나타내어 본 분석법의 적합성을 확인할 수 있었다(Fig. 5).
상기 표준 검량선으로부터 산출된 기울기와 y절편의 표준편차로 계산된 검출한계(LOD)는 0.065 μg/mL이었고 정량한계(LOQ)는 0.197 μg/mL인 것으로 나타났다(Table 2). 검출한계는 분석 대상시료 내에 존재하는 대상물질의 검출 가능한 최저농도를 의미하며 정량한계는 분석 대상시료의 정확성과 정밀성을 가진 정량값으로 산출할 수 있는 대상물질의 최저농도를 의미한다(Kwon JG 등 2017). 본 분석법에 따라 자색옥수수 포엽 추출물에 함유되어 있는 C3G의 함량은 0.065 μg/mL 농도까지 검출이 가능하며 0.197 μg/mL 농도까지 정량이 가능하다. Kalogiouri NP 등(2022)의 연구에서 C3G의 검출한계(LOD)는 0.1 μg/mL, 정량한계(LOQ)는 0.3 μg/mL이었고, Jeong IH 등(2017)에서의 C3G 검출한계(LOD)는 0.0836 μg/mL, 정량한계(LOQ)는 0.2534 μg/mL인 것과 비교하였을 때, 본 연구의 분석법이 더 낮은 농도 범위로 C3G의 정량 및 검출이 가능하다는 것을 확인할 수 있었다. 이와 같이 같은 물질에 대한 LOD와 LOQ값을 차이는 분석장비의 종류와 감도, 분석 시 사용되는 컬럼, 용매 이동상 조건, 유속, 시료 전처리 방법에 따른 불순물의 함유 정도 등의 영향이라고 판단된다(Seo CS & Lee MY 2020; Kaviani R 2024).
4. 정확성 및 정밀성 평가
정확도는 분석법의 유효성 검증인자로 분석을 통하여 얻어진 측정값이 이미 알고 있는 특정 농도 값에 근접한 정도를 의미하는데, 근접한 정도가 100%에 가까울수록 높은 정확도를 나타낸다. 여러 가이드라인에서 정확성에 대한 허용치를 다르게 규정하고 있으며 분석 시료 농도 1 μg/g을 기준으로 AOAC(Association of Official Agricultural Chemists) 75∼120%, MFDS(Ministry of Food and Drug Safety) 70∼110%, CODEX(Codex Alimentarius Commission) 80∼110% 수준으로 제시하고 있다. 정밀도는 반복적으로 측정되는 값들 사이의 변동성을 측정하고 분석 결과의 재현성을 평가하는 항목이다. 분석값들의 표준편차(SD) 또는 상대표준편차(RSD)로 나타내며 값이 작을수록 높은 정밀도를 나타낸다(Noh JS & Myung SW 2024).
본 연구에서 정확성은 농도별 표준용액의 일내분석과 일간분석을 통하여 측정된 값(measured value)이 참값(true value)에 근접한 정도를 백분율로 나타내어 각 분석값을 회수율로 나타내었으며 측정된 값들로부터 상대표준편차(RSD)를 구하여 정밀성을 검정하였다. 농도별 표준용액(1, 5, 10 μg/mL)을 1일 3 cycle로 분석한 일내분석(intra-day) 결과, 정확성(accuracy)은 91.73∼101.06%이었고 RSD는 2.54∼3.96%이었다. 일내분석 과정을 3일 동안 분석한 일간분석(inter-day)의 정확성(Accuracy)은 96.89∼99.25%이었고 RSD는 2.20∼3.53% 범위로 나타났다(Table 3). 각각의 분석에서의 상대표준편차는 모두 5.0% 이하로 나타나 C3G 분석법의 정확성 및 정밀성, 재현성이 검증되었다.
5. 회수율 측정
자색옥수수 포엽 추출물이 혼합된 농도별 표준용액과 추출물 시험용액을 HPLC로 분석한 다음 추출물 혼합 표준용액과 추출물 시험용액의 peak area값을 확인하였다. 회수율(recovery)은 상기 분석에서 산출된 각 용액의 area 값의 차이를 구하고 이 값에 추출물 시험용액 검출 값을 나누어 측정하였다. 농도별 표준용액의 지표성분 C3G의 회수율은 97.78∼100.94%로 확인되었으며 RDS 1% 이내로 측정되어 매우 우수한 정확도와 정밀성을 나타내었다(Table 4).
6. 자색옥수수 포엽 추출물의 C3G 함량
본 연구의 분석법 검증을 통하여 C3G에 대한 HPLC 분석법이 자색옥수수 포엽 추출물에 함유되어 있는 지표성분의 정량에 적용할 수 있는 특이성, 우수한 직선성, 정확성 및 정밀성, 재현성이 있음을 확인하였다. 본 분석법으로 자색옥수수 포엽 추출물의 C3G 평균 함량은 1.86%이었으며, 기준 규격을 80∼120%로 설정하였을 때(KFDA 2008) 기준값은 1.49∼2.24%인 것을 확인할 수 있었다(Table 5).
요 약
본 연구에서는 일반 식품 및 기능성 원료 개발을 목적으로 자색옥수수 포엽 추출물의 표준화를 위하여 C3G를 지표성분으로 설정하였다. HPLC-PDA 분석을 통하여 C3G의 분석법을 확립하고 유효성 검정을 수행하였다. 분석법의 유효성 검정 결과, C3G 표준용액과 자색옥수수 포엽 추출물의 retention time 및 spectrum이 일치하는 특이성을 확인하였다. 표준 검량선의 상관계수(R2)는 0.9999로 매우 우수한 직선성을 나타내었으며 검출한계(LOD)는 0.065 μg/mL이었고 정량한계(LOQ)는 0.197 μg/mL이었다. 지표성분 C3G의 일내분석(intra-day)에서 정확성은 91.73∼101.06% 상대표준편차로 확인된 정밀성은 2.54∼3.96%이었다. 일간분석(inter-day)에서 정확성은 96.89∼99.25%이었으며 정밀성은 2.20∼3.53%인 것으로 나타나 본 시험법의 정확성(accuracy) 및 정밀성(precision)을 확인할 수 있었다. 표준품 농도별 지표성분 C3G의 회수율(recovery)은 97.78∼100.94%의 범위였으며 상대표준편차 1% 이내로 측정되었다. 이는 본 연구에서 수행된 HPLC 분석법이 자색옥수수 포엽 추출물의 지표성분인 C3G를 분석하고 표준화하는데 적합한 시험법임을 의미한다.
Acknowledgments
본 연구는 농촌진흥청 지역특화작목기술개발 「강원 자색옥수수 활용 기능성 식품 및 발효 점증 소재 개발(RS-2024-00438488)」의 연구비 지원과 강원특별자치도 농업기술원(농식품연구소)의 분석지원으로 이루어진 연구 결과로 이에 감사드립니다.
REFERENCES
-
Atanasov AG, Zotchev SB, Dirsch VM, Supuran CT (2021) Natural products in drug discovery: Advances and opportunities. Nat Rev Drug Discov 20(3): 200-216.
[https://doi.org/10.1038/s41573-020-00114-z]

-
Baek H, Sanjay, Park M, Lee HJ (2023) Cyanidin-3-O-glucoside protects the brain and improves cognitive function in APPswe/PS1ΔE9 transgenic mice model. J Neuroinflamm 20: 268.
[https://doi.org/10.1186/s12974-023-02950-3]

-
Cai T, Ge-Zhang S, Song M (2023) Anthocyanins in metabolites of purple corn. Front Plant Sci 14: 1154535.
[https://doi.org/10.3389/fpls.2023.1154535]

-
Chavan SD, Desai DM (2022) Analytical method validation: A brief review. World J Adv Res Rev 16(2): 389-402.
[https://doi.org/10.30574/wjarr.2022.16.2.1165]

-
Choi JK, Park JY, Park KJ, Kim HY, Ryu SH, Seo YH (2017) Anthocyanin-rich grain corn hybrid variety ‘Saekso 2’. Korean J Breed Sci 49(3): 289-293.
[https://doi.org/10.9787/KJBS.2017.49.3.289]

-
Chuntakaruk H, Kongtawelert P, Pothacharoen P (2021) Chondroprotective effects of purple corn anthocyanins on advanced glycation end products induction through suppression of NF-κB and MAPK signaling. Sci Rep 11: 1895.
[https://doi.org/10.1038/s41598-021-81384-4]

- Clinical and Laboratory Standards Institute (CLSI) (2012) Evaluation of Detection Capability for Clinical Laboratory Measurement Procedures; Approved Guideline-second Edition. CLSI document EP17-A2. CLSI, Wayne, PA.
-
Guo L, Qiao J, Gong C, Wei J, Li J, Zhang L, Qin D, Huo J (2023) C3G quantified method verification and quantified in blue honeysuckle (Lonicera caerulea L.) using HPLC-DAD. Heliyon 9(4): e14685.
[https://doi.org/10.1016/j.heliyon.2023.e14685]

-
Haggard S, Luna-Vital D, West L, Juvik JA, Chatham L, Paulsmeyer M, Gonzalez de Mejia E (2018) Comparison of chemical, color stability, and phenolic composition from pericarp of nine colored corn unique varieties in a beverage model. Food Res Int 105: 286-297.
[https://doi.org/10.1016/j.foodres.2017.11.038]

-
Jang GW, Park EY, Choi SH, Choi SI, Cho BY, Sim WS, Han X, Cho HD, Lee OH (2018) Development and validation of analytical method for wogonin, quercetin, and quercetin-3-O-glucuronide in extracts of Nelumbo nucifera, Morus alba L., and Raphanus sativus mixture. J Food Hyg Saf 33(4): 289-295.
[https://doi.org/10.13103/JFHS.2018.33.4.289]

-
Jeong IH, Oh MS, Jeon JS, Kim HT, Hong SR, Park KH, Yoon MH (2017) A comparative study on anthocyanin and polyphenol contents in colored agricultural products. J Food Hyg Saf 32(5): 371-380.
[https://doi.org/10.13103/JFHS.2017.32.5.371]

- Jung T, Song S, Son B, Kim J, Baek S, Kim C, Kim S, Kim S, Kim S, Park K, Shin H, Huh C (2009) A black waxy hybrid corn, “Heukjinjuchal” with good eating quality. Korean J Breed Sci 41(4): 599-602.
-
Kalogiouri NP, Karadimou C, Avgidou MS, Petsa E, Papadakis EN, Theocharis S, Mourtzinos I, Menkissoglu-Spiroudi U, Koundouras S (2022) An optimized HPLC-DAD methodology for the determination of anthocyanins in grape skins of red Greek winegrape cultivars (Vitis vinifera L.). Molecules 27(20): 7107.
[https://doi.org/10.3390/molecules27207107]

-
Kaviani R (2025) Comparison of different approaches for calculating LOD and LOQ in an HPLC-based analysis method. Pharm Sci 31(1): 106-109.
[https://doi.org/10.34172/PS.024.40452]

- Korea Food & Drug Administration (KFDA) (2007) Guideline for Standard of Health Functional Food. Korea Food & Drug Administration, Seoul, Korea. pp 6-13.
- Korea Food & Drug Administration (KFDA) (2008) Guideline of Standard of Functional Ingredient for Health Functional Food Development. Korea Food & Drug Administration, Seoul, Korea. pp 53-59.
-
Khoo HE, Azlan A, Tang ST, Lim SM (2017) Anthocyanidins and anthocyanins: colored pigments as food, pharmaceutical ingredients, and the potential health benefits. Food Nutr Res 61: 1361779.
[https://doi.org/10.1080/16546628.2017.1361779]

-
Kim HY, Park JY, Park KJ, Ryu SH, Chang EH, Goh BD, Yoon BS, Yong WS, Choi JK (2021) Major characteristics of anthocyanin-rich purple corn hybrid variety ‘Saekso 1’. Korean J Breed Sci 53(4): 534-538.
[https://doi.org/10.9787/KJBS.2021.53.4.534]

-
Kim JT, Yi G, Chung IM, Son BY, Bae HH, Go YS, Ha JY, Baek SB, Kim SL (2020) Timing and pattern of anthocyanin accumulation during grain filling in purple waxy corn (Zea mays L.) suggest optimal harvest dates. ACS Omega 5(25): 15702-15708.
[https://doi.org/10.1021/acsomega.0c02099]

-
Kim MK (2025) Validation of analysis method for cyanidin-3-glucoside (C3G) in Lonicera caerulea Fruit Extracts. Resour Sci Res 7(2): 82-91.
[https://doi.org/10.52346/rsr.2025.7.2.82]

-
Kim Y, Han SH, Jeon JY, Hwang M, Im YJ, Chae SW, Kim MG (2012) Method development of ellagic acid as marker compound for standardization of Gochang bokbunja (Rubus coreanus Miquel) as functional ingredient. J Korean Food Sci Nutr 41(11): 1554-1558.
[https://doi.org/10.3746/jkfn.2012.41.11.1554]

-
Kong JM, Chia LS, Goh NK, Chia TF, Brouillard R (2003) Analysis and biological activities of anthocyanins. Phytochemistry 64(5): 923-933.
[https://doi.org/10.1016/S0031-9422(03)00438-2]

-
Kumar R, Flint-Garcia S, Salazar Vidal MN, Channaiah L, Vardhanabhuti B, Sommer S, Wan C, Somavat P (2025) Optimization of polyphenol extraction from purple corn pericarp using glycerol/lactic acid-based deep eutectic solvent in combination with ultrasound-assisted extraction. Antioxidants 14(1): 9.
[https://doi.org/10.3390/antiox14010009]

-
Kunle OF, Egharevba HO, Ahmadu PO (2012) Standardization of herbal medicines: A review. Int J Biodivers Conserv 4(3): 101-112.
[https://doi.org/10.5897/IJBC11.163]

- Kwon JG, Sed C, Choi YH, Choi CW, Kim JK, Jeong W, Lee JE, O KH, Hong SS (2017) Validation of method determining coixol in Coix lachryma-jobi var. ma-yuen roots extract. J Korean Soc Food Sci Nutr 46(8): 952-956.
- Lee JS, Jung TW, Song SY, Son BY, Kim JT, Kim SK, Kim SL, Baek SB, Seo JH, Lee JE, Kim SJ, Kwon YU, Kim WH, Park KJ, Shin HM, Huh CS, Kang DS (2011) A bicolor waxy corn hybrid with high eating quality, ‘Eolrukchal 1’. Korean J Breed Sci 43(4): 555-558.
-
Lee KY, Hong SY, Kim TH, Kim JE, Park AR, Noh HS, Kim SC, Park JY, Ahn MS, Jeong WJ, Kim HY (2018) Inhibition of pancreatic lipase activity and adipocyte differentiation in 3T3-L1 cells treated with purple corn husk and cob extracts. J Food Hyg Saf 33(2): 131-139.
[https://doi.org/10.13103/JFHS.2018.33.2.131]

-
Li CY, Kim HW, Won SR, Min HK, Park KJ, Park JY, Ahn MS, Rhee HI (2008) Corn husk as a potential source of anthocyanins. J Agric Food Chem 56(23): 11413-11416.
[https://doi.org/10.1021/jf802201c]

- Lide DR (2005) CRC Handbook of Chemistry and Physics. 86th ed. CRC Press, USA. pp 6-195.
-
Li S, Han Q, Qiao C, Song J, Cheng CL, Xu H (2008) Chemical markers for the quality control of herbal medicines: An overview. Chin Med 3(1): 7.
[https://doi.org/10.1186/1749-8546-3-7]

- Noh J, Myung SW (2024) Understanding and comparative analysis of analytical method validation. Anal Sci Technol 37(3): 131-142.
-
Oumeddour DZ, Al-Dalali S, Zhao L, Zhao L, Wang C (2024) Recent advances on cyanidin-3-O-glucoside in preventing obesity-related metabolic disorders: A comprehensive review. Biochem Biophys Res Commun 729: 150344.
[https://doi.org/10.1016/j.bbrc.2024.150344]

-
Park KJ, Park JY, Seo YH, Ryu SH, Choi JK, Kim HY (2016) Anthocyanin-rich purple waxy corn single cross hybrid ‘Cheongchunchal’. Korean J Breed Sci 48(4): 541-546.
[https://doi.org/10.9787/KJBS.2016.48.4.541]

- Rural Development Administration (RDA) (2020) A Study on the Standardization of the Functional Material from Regional Agro-Foods. Rural Development Administration, Jeonju, Korea. pp 7-8.
-
Seo CS, Lee MY (2020) HPLC-PDA and LC-MS/MS analysis for the simultaneous quantification of the 14 marker components in Sojadodamgangki-Tang. Appl Sci 10(8): 2804.
[https://doi.org/10.3390/app10082804]

-
Tan J, Li Y, Hou DX, Wu S (2019) The effects and mechanisms of cyanidin-3-glucoside and its phenolic metabolites in maintaining intestinal integrity. Antioxidants 8(10): 479.
[https://doi.org/10.3390/antiox8100479]

-
Tiwari U, Cummins E (2013) Factors influencing levels of phytochemicals in selected fruit and vegetables during pre- and post-harvest food processing operations. Food Res Int 50(2): 497-506.
[https://doi.org/10.1016/j.foodres.2011.09.007]

-
Wang H, Chen Y, Wang L, Liu Q, Yang S, Wang C (2003) Advancing herbal medicine: Enhancing product quality and safety through robust quality control practices. Front Pharmacol 14: 1265178.
[https://doi.org/10.3389/fphar.2023.1265178]