열수 및 에탄올 키위박 추출물의 항산화 활성 평가
Abstract
The kiwi friut is well known for its health benefits and is widely incorporated into food products as a source of functional materials. However, kiwi pomace, a by-product of this process, remains largely unutilized, causing both economic and environmental concerns. Therefore, this study aimed to investigate the antioxidant activity of kiwi pomace and explore its potential as a functional ingredient. Kiwi pomace was extracted with water (KPW) and 70% ethanol (KPE), and their antioxidant activities were assessed by measuring total phenolic contents (TPC), 2,2-diphenyl-1-picrylhydrazyl (DPPH) radical scavenging activity, reducing power, and tyrosinase inhibition activity. The TPC of KPW and KPE were 15.08 and 27.80 μg gallic acid equivalents (GAE)/mL, respectively. The DPPH radical scavenging activity results for KPW and KPE were 99.51% and 95.95%, respectively, with corresponding reducing power values of 45.89 μM and 53.04 μM, respectively. In contrast, the extracts exhibited negligible tyrosinase inhibitory activity, suggesting limited application in melanin-related antioxidative mechanisms. Overall, these results indicate that KPW and KPE possess antioxidant potential and could be used as functional materials in food or nutraceutical applications.
Keywords:
kiwi, kiwi pomace, antioxidant, functional food, functional nutraceutical서 론
최근 현대사회에서 만성 질환 예방을 위한 균형 잡힌 식품 섭취의 중요성에 대한 소비자들의 인식이 크게 높아졌다(Mazzoni L 등 2021). 특히, 과일과 채소 섭취의 중요성이 강조되고 있으며, 과일과 채소는 비타민, 카로티노이드 및 미네랄 등의 다양한 생리활성 물질을 함유하고 있다(Latocha P 2017). 또한, 과일 및 채소 섭취는 전반적인 건강 증진뿐만 아니라 위장 질환, 고혈압, 피부 질환, 면역 기능 향상 및 심장 질환 등 만성 질환의 위험을 낮추며, 이를 함유한 식품의 소비는 증가하는 추세이다(Paredes-López O 등 2010).
키위(Actinidia chinensis)는 중국을 포함한 이탈리아, 한국, 미국, 유럽 등의 나라에서 널리 재배되고 있는 Actinidiaceae과에 속하는 다년생 덩굴 식물이다(Pinto D 등 2020). 키위는 폴리페놀, 플라보노이드, 아미노산, 비타민 등의 다양한 생리활성 화합물을 함유하고 있어(Ma T 등 2017) 이에 대한 연구가 활발히 이루어지고 있으며, 현재 키위 추출물의 항산화, 항염증, 항균 및 폐암 세포 증식 억제 효과에 대해 보고되었다(Park YS 등 2009; Chung HJ 등 2015; Kim DI 등 2018). 건강에 대한 관심이 높아지면서, 건강하고 영양가 있으며 고품질의 식품을 선호하는 소비자의 선호도가 변화함으로써 영양가가 높은 키위에 대한 수요가 높아지는 추세이다(Singletary K 2012). 키위는 생과일뿐만 아니라 주스, 잼 그리고 와인 등 다양한 형태로 가공되어 섭취된다(Carbone K 등 2020).
전 세계적으로 키위의 재배 및 가공 산업이 많이 성장하였으며, 특히 가공 과정에서 키위를 사용하고 발생하는 키위 찌꺼기, 껍질, 씨앗 등이 포함된 다량의 부산물이 생성되며(Kheirkhah H 등 2019), 키위 주스의 경우 제조 후 남는 키위 주요 부산물은 전체 과일의 약 20∼40% 비율을 차지한다(Martin-Cabrejas MA 등 1995). 이러한 부산물을 폐기물로 처리 시 폐기물 처리의 막대한 비용 부담 및 환경 영향에도 문제를 발생시킬 수 있기에 이들 부산물의 업사이클링은 환경오염을 저감할 뿐만 아니라 산업적 부가가치 창출 측면에서도 중요하다(Yang HS 등 2025). 과일 가공에서 발생하는 부산물에는 껍질, 씨앗, 줄기 및 열매를 포함하기에 영양가가 높은 것으로 나타났다(Ayala-Zavala JF 등 2011). 이처럼 과일 부산물은 기능성 물질이 풍부하며, 이를 회수하여 부가 가치화 또는 지속 가능한 제품을 생산에 활용하면 유익할 것이다(Moshtaghian H 등 2021). 부산물 내에 존재하는 화합물은 화장품 및 기능성 소재로 사용될 수 있으며(Garcia-Salas P 등 2010; Baiano A 2014), 여러 연구에서 과일이나 식품 부산물의 가치화 및 기능성 소재 활용의 연구가 많이 진행되었다(Ignat I 등 2011; Herrero M 등 2015). 현재 키위 부산물을 활용한 연구는 제한적이며, 키위 부산물에서 다양한 추출 방법을 통해 생리활성 물질을 분리하고자 하는 연구가 진행 중이지만, 키위박(kiwi pomace)에 대한 기능성 소재로서의 체계적인 연구는 부족한 실정이다.
이에 본 연구는 키위박을 열수 및 70% 에탄올로 각각 추출하여, 항산화 활성과 기능성 소재로서의 가능성을 평가하였다. 이를 통해 버려지는 키위박의 활용도를 높이고자 하였고, 항산화 활성을 기반으로 기능성 소재로서의 적용 가능성을 탐색하고자 하였다.
재료 및 방법
1. 실험 재료
본 실험 과정에서 사용한 키위박은 키위를 통째로 압착하고 잔존하는 키위 껍질, 과육 및 씨의 혼합 형태로 경남농업기술원에서 제공받았다. 키위박 추출물을 희석하기 위해 사용한 dimethyl sulfoxide(DMSO)는 Junsei Chemical Co., Ltd.(Chuo-ku, Tokyo)에서 구입하였으며, 항산화 활성 측정에 필요한 2,2-phenyl-1-picryl-hydrazyl(DPPH), Folin-Ciocalteu phenol reagent, Na2CO3, gallic acid, 그리고 tyrosinase 저해 활성을 측정하기 위해 사용한 sodium phosphate monobasic dehydrate, sodium phosphate dibasic, L-tyrosine, mushroom tyrosinase 및 양성 대조군으로 사용한 vitamin C와 arbutin는 Sigma-Aldrich Co.(St. Louis, MO, USA)에서 구입하였다. 또한, 실험 중 사용한 에탄올과 환원력 측정에 필요한 potassium phosphate monobasic, potassium phosphate dibasic anhydrous는 Daejung Chemicals & metal Co., Ltd.(Siheung, Korea)에서 구입하였다.
버려지는 키위박 자체 중량의 10배수의 열수 또는 70%의 에탄올을 넣고 열수 추출물은 100±2℃ 그리고 70% 에탄올 추출물은 80±2℃에서 3 hr 동안 추출기(MS-DM609; Misung, Korea)를 이용해 환류 추출을 진행한 뒤 5 μm 종이 필터로 여과하였으며, 그 후 진공동결건조기(LP 20; Ilshinbiobase, Dongducheon, Korea)를 사용하여 동결건조하였다. 추출 수율은 동결건조된 추출물의 무게를 원재료의 건조 중량 대비 백분율로 환산하여 계산하였고, 키위박 추출물의 추출 수율은 열수 추출 수율은 5.29%(w/w-dry weight), 70% 에탄올 수율은 4.25%(w/w-dry weight)로 나타났다(Table 1). 각 추출물은 동결건조 후 —20℃에 보관하여 사용하였으며, 키위박 추출물은 KPW(kiwi pomace extracted with water)와 KPE(kiwi pomace extracted with 70% ethanol)로 명명하였다.
총 페놀 함량은 일반적으로 사용되고 있는 Folin-Denis법(Singleton VL 등 1999)을 응용하여 KPW와 KPE의 총 페놀 함량을 측정하였다. 2 mL microcentrifuge tube에 KPW와 KPE를 200 μL씩 첨가하고, 94.5% 에탄올 200 μL와 증류수 1,000 μL를 첨가하였으며, 각각의 혼합시료에 100 μL의 50% Folin-Ciocalteu phenol reagent(FCP)을 가하여 5 min 동안 반응시켰다. 이후 200 μL 5%(w/v) Na2CO3를 200 μL 추가로 가하고 빛이 차단된 상태에서 1 hr 동안 반응시켰다. 반응 후 최종 반응물은 96-well plate에 200 μL씩 분주하여 microplate reader(VersaMax, Molecular Devices, BaneBio, Sunnyvale, CA, USA)를 사용하여 흡광도값 725 nm로 설정하여 측정하였다. 총 페놀 함량은 표준물질인 gallic acid(GA)를 DMSO에 용해하여 나타낸 표준 검량곡선을 사용하였으며, 표준곡선의 방정식은 y=0.377x—0.0416에 대입하여 gallic acid equivalent(GAE)로 환산 후 μg GAE/mL로 나타내었다.
DPPH(2,2-diphenyl-1-picryl hydrazyl)의 환원에 의한 자유 라디칼 소거 활성을 평가하기 위해 DPPH 라디칼 소거 활성 분석을 통해 KPW와 KPE의 항산화 활성을 평가하였으며, 양성대조군으로는 항산화 효과가 우수한 vitamin C를 사용하여 비교하였다. Xiong Q 등(1996)의 실험법을 기반으로 DPPH 시약을 200 μM의 농도가 되도록 94.5% 에탄올에 용해시킨 후 96-well plate에 DPPH 190 μL를 넣어준 뒤 KPW와 KPE를 각각 10, 50, 100, 200, 400 그리고 800 μg/mL로 단계 희석하여 10 μL를 넣고 빛을 차단하여 30 min 동안 반응시켰다. 처리군과 비교하기 위해 대조군은 DPPH 190 μL를 넣어준 뒤 용매 10 μL를 넣어 비교하였고, 양성대조군 vitamin C는 50 μg/mL 농도로 처리하여 반응을 시킨 후 microplate reader(VersaMax, Molecular Devices, BaneBio, Sunnyvale, CA, USA)를 사용하여 517 nm의 흡광도를 측정하였다. 추출물과 양성 대조군의 DPPH 라디칼 소거 활성은 다음식을 이용하여 계산하였다.
KPW와 KPE의 환원력을 측정하기 위해 copper ion reduction 실험을 진행하였다. KPW와 KPE 농도는 각각 10, 50, 100, 200, 400 그리고 800 μg/mL로 단계 희석하여 실시하였으며, 96-well plate에 추출물 각각 40 μL, 10 mM potassium phosphate buffer(pH 7.39) 60 μL, 0.625 mM 농도의 neocuproine 용액 80 μL 그리고 100 μM의 농도로 CuCl2를 증류수에 녹인 용액을 20 μL를 분주한 후 25℃에서 1 hr 동안 반응시켰다(Aruoma OI 등 1993). 또한, 양성대조군인 vitamin C의 농도는 50 μg/mL 농도로 처리하여 반응을 시킨 후 454 nm로 설정한 microplate reader(VersaMax, Molecular Devices, BaneBio, Sunnyvale, CA, USA)로 흡광도를 측정하였다. Copper ion의 환원력 결과값은 copper(Ⅰ)/neocuproine의 extinction coefficient(7.95 × 103 M-1cm-1)를 사용하여 나타내었다.
KPW와 KPE의 tyrosinase 저해 활성은 L-tyrosine을 기질로 하여 저해 활성을 평가하였다. 양성 대조군으로 tyrosinase 저해 활성이 있는 것으로 알려진 arbutin과 비교 분석하여 실시하였다. 96-well plate에 KPW와 KPE를 각각 10, 50, 100, 200, 400 그리고 800 μg/mL로 단계 희석한 추출물을 20 μL, 1.5 mM L-tyrosine 40 μL, 0.1 M sodium phosphate buffer(pH 6.5) 220 μL를 넣어준 뒤 1,500 U tyrosinase 20 μL를 첨가하여 37℃ incubator에서 15 min 반응시킨 후, microplate reader(VersaMax; Molecular Devices, Sunnyvale, CA, USA) 에서 490 nm로 설정한 흡광도를 측정하였다(Shon MS 등 2016). 또한, 처리군과 비교하기 위해 대조군은 추출물 대신 DMSO 20 μL를 첨가하였고, 양성대조군 arbutin은 50 μg/mL 농도로 처리하여 분석하였으며, 저해 활성은 아래와 같은 식으로 계산하였다.
모든 실험은 3회 이상 반복하였고 실험 결과는 평균±표준편차로 표현하였으며, 얻어진 결과의 통계 처리는 SPSS software(Ver. 18, SPSS Inc., Chicago, IL, USA)를 이용하여 분산분석을 실시하였다. 각 구간의 유의성 차이는 Duncan’s multiple range test를 통해 유의성 차이 95%(p<0.05)로 분석하였다.
결과 및 고찰
1. 키위박 추출물의 총 페놀 함량 측정
식물에 존재하는 phytochemical 중에서도 페놀성 화합물은 다양한 생리활성이 보고되어 널리 활용되고 있으며, 천연 항산화 소재로서의 작용도 우수하다고 보고되었다(Sato M 등 1996). 페놀성 화합물은 자유 라디칼을 소거하는 주요한 역할을 한다는 연구가 많이 보고되어 있으며(Madsen HL 등 1996; Moller JKS 등 1999), 천연 항산화제로서의 기능이 잘 알려진 2차 대사산물인 안토시아닌 및 플라보노이드 등과 같은 페놀성 화합물이 다량 함유되어 있으며, 이는 항산화 활성에 있어 중요한 인자로 작용한다(Kim EJ 등 2012; Catel-Ferreira 등 2015). KPW와 KPE의 총 페놀 함량은 800 μg/mL의 농도에서 측정하였으며 표준물질로는 gallic acid를 사용하여 검량하였다. 그 결과 KPW의 총 페놀 함량은 15.08±0.35 μg GAE/mL로 나타났으며, KPE의 총 페놀 함량은 27.80±0.65 μg GAE/mL를 나타내었다(Table 2). Ilie GI 등(2022)에서 키위 부산물과 껍질의 총 페놀 함량을 측정하였을 때 키위 부산물은 3.79±0.15 mg GAE/g DW를 나타내었고, 키위 껍질은 9.71±0.28 mg GAE/g DW를 나타내었다. 또한, 키위 열매의 선행 연구(Jin DE 등 2014)에서 80% 에탄올 추출물의 총 페놀 함량은 3.16 mg GAE/g을 나타내었고, 열수 추출물의 총 페놀 함량은 1.33±0.14 mg GAE/g을 나타내었다. 선행 연구와 본 연구 결과 키위에 함유된 다양한 항산화 성분이 키위 열매뿐만 아니라 가공 과정에서 발생하는 키위 부산물에도 다량 함유하고 있음을 확인하였다. 따라서 버려지는 키위박을 활용하여 기능성 소재로의 사용 가능성을 시사한다.
2. 키위박 추출물의 DPPH 라디칼 소거 활성 평가
DPPH은 안정적인 자유 라디칼로, 항산화제가 전자나 수소를 공여할 경우 hydrazine으로 환원된다(Contreras-Guzmán ES & Strong GC 1982). 이러한 DPPH 라디칼을 이용한 소거 활성 평가는 항산화 활성 측정에 널리 사용되는 대표적 분석법으로 항산화 물질에 의해 DPPH의 색이 환원되어 탈색되는 원리를 이용한다(Ancerewicz J 등 1998). 키위박 추출물의 항산화 활성을 평가하기 위해 DPPH 라디칼 소거 활성을 실시하여 KPW와 KPE의 항산화 활성을 평가하였다. KPW와 KPE의 DPPH 라디칼 소거 활성을 각각 10, 50, 100, 200, 400 그리고 800 μg/mL 농도로 평가하였다. 그 결과 KPW는 11.40%, 18.99%, 27.08%, 45.23%, 70.73% 그리고 99.51%를 나타내었고, KPE는 11.89%, 27.27%, 44.75%, 72.03%, 92.26% 그리고 95.95%를 나타내었다. 양성대조군인 vitamin C의 50 μg/mL 농도와 KPW와 KPE를 비교하였을 때, vitamin C와 유사한 수준의 DPPH 라디칼 소거 활성을 나타냈다(Fig. 1). Wang Y 등(2018)의 키위 과일 껍질, 과육 및 씨앗을 추출물로 제조하여 DPPH 라디칼 소거 활성을 평가하였을 때, 키위 껍질은 95.16%, 과육은 90.37% 그리고 씨앗은 83.45%의 DPPH 라디칼 소거 활성을 나타내었다. 키위 부위별 추출물과 키위 부산물의 DPPH 라디칼 활성의 결과에서 키위를 사용하고 버려지는 부산물에서도 높은 수준의 항산화 활성을 나타냄을 확인할 수 있었다. 또한, 키위 이외에도 감귤을 착즙하거나 과피를 제거한 후 생성되는 부산물을 열수 및 에탄올로 추출하여 DPPH 라디칼 소거 활성을 측정하였을 때, 1,000 μg/mL 농도에서 통과 에탄올 추출물 72.51%, 통과 열수 추출물 48.54%, 과육 에탄올 추출물 41.87% 그리고 과육 열수 추출물 23.42% 순으로 높은 DPPH 라디칼 소거 활성을 나타내었다(Song YW 등 2013). 이러한 결과를 바탕으로 과육뿐만 아니라 과피를 포함하는 통과 산물에 유효한 항산화 성분이 많이 함유되어 있기에 이를 이용해 항산화 기능성 소재로서 높은 활용 가치가 있을 것으로 사료된다.
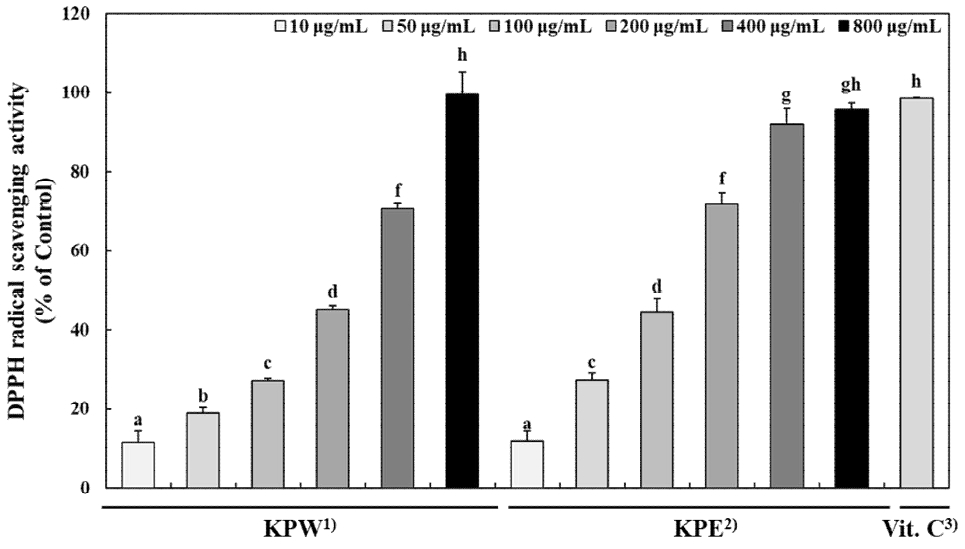
The DPPH radical scavenging activities of KPW and KPE.The DPPH radical scavenging activities of kiwi pomace extracted with water (KPW) or 70% ethanol (KPE) were measured at concentrations of 10, 50, 100, 200, 400 and 800 µg/mL. Vitamin C was used as a positive control at a concentration of 50 µg/mL. According to Duncan’s multiple range test (p<0.05), groups with a same letter are not significantly different.
3. 키위박 추출물의 환원력 측정
환원력 측정은 항산화 활성을 나타내는 여러 가지 메커니즘 중 유리기 및 활성 산소종에 전자를 공여하는 기전으로 항산화 활성을 평가할 수 있다(Siddhuraju P 등 2002). 본 연구에서 키위박 추출물의 환원력을 측정하고자 Cu(Ⅱ)이 Cu(Ⅰ)로 환원시키는 원리를 이용하여 환원력을 측정하였다. KPW와 KPE의 환원력을 측정하기 위해 각각 10, 50, 100, 200, 400 그리고 800 μg/mL 농도로 평가하였다. 그 결과 KPW와 KPE 모든 농도에서 Cu(Ⅱ)을 Cu(Ⅰ)으로 환원시켰으며, 10, 50, 100, 200, 400 그리고 800 μg/mL 농도에서 KPW는 2.51, 14.69, 27.66, 43.58, 46.48 그리고 45.89 μM의 결과를 나타내었고, KPE는 5.13, 25.44, 43.17, 48.18, 49.61 그리고 53.04 μM을 나타내었다(Fig. 2). 키위박 추출물과 같은 농도로 양성 대조군인 vitamin C와 비교하였을 때, 50 μg/mL에서 KPW와 KPE는 vitamin C보다 높은 활성을 나타내었다. 또한, 키위 이외에도 착즙 후 발생하는 가공 부산물을 활용한 오미자 착즙 후 박을 에탄올 추출물과 오미자의 열매 및 씨 각각의 환원력을 측정하였을 때, 0.44% (오미자 착즙 후 박 추출물), 0.28% (오미자 씨 추출물) 그리고 0.12% (오미자 열매 추출물) 순으로 높은 환원력을 나타내었다(Kim MS 등 2017). 이러한 결과를 바탕으로 가공 후의 박에서도 항산화 성분이 잔존하거나 오히려 농축되어 있을 수 있음을 시사한다.
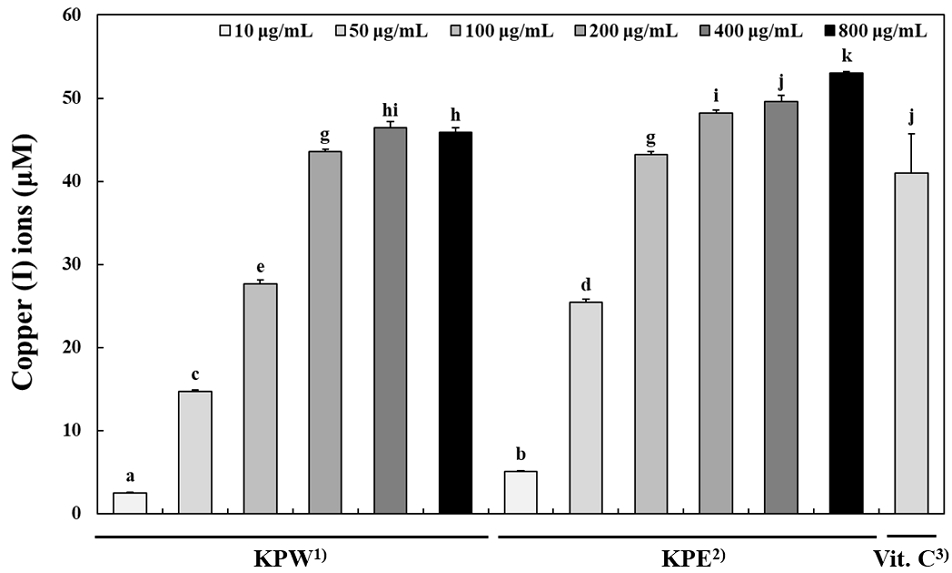
The copper (Ⅱ) reduction potential of KPW and KPE.The copper (II) reduction potentials of kiwi pomace extracted with water (KPW) or 70% ethanol (KPE) were measured at concentrations of 10, 50, 100, 200, 400, and 800 µg/mL. Vitamin C was used as a positive control at a concentration of 50 µg/mL. According to Duncan’s multiple range test (p<0.05), groups with a same letter are not significantly different.
4. 키위박 추출물의 Tyrosinase 저해 활성 평가
피부 가장 바깥쪽에 위치하는 표피의 기저층에 존재하는 melanocyte에서 tyrosinase는 tyrosine을 산화시켜 멜라닌 생합성에 관여하며, tyrosinase 효소 활성을 저해하는 것은 피부 미백과 노화 방지에 중요하게 작용한다(Choi SJ 등 2011; Park DB 등 2025). 키위박 추출물을 10, 50, 100, 200, 400 그리고 800 μg/mL 농도에서 tyrosinase 저해 활성을 측정하기 위해 L-tyrosine을 기질로 하여 tyrosinase 저해 활성을 평가하였다. 그 결과 KPW는 10, 50, 100, 200, 400 그리고 800 μg/mL 농도에서 70.6%, 6.61%, 6.24%, 5.04%, 3.67% 그리고 3.35%이었다. 동일한 농도로 KPE의 결과는 8.24%, 8.39%, 8.92%, 6.53%, 2.34% 그리고 —0.64%를 나타냈다(Fig. 3). 50 μg/mL의 농도에서 양성 대조군으로 잘 알려진 arubutin과 비교한 결과, KPW와 KPE 모두 낮은 저해 활성을 보였다. 키위 추출물의 tyrosinase 저해 활성 평가한 선행 연구(Jung SW 등 1995)에서 키위 추출물의 tyrosinase 저해 활성 효과가 0.7%를 나타냈으며, 이는 키위 추출물이 tyrosinase 저해 활성이 미미하다는 것을 확인하였다. 따라서 선행 연구와 본 연구 결과 키위와 키위박 모두 tyrosinase 저해 활성 효과는 미미하였으며, 이는 키위의 높은 항산화 활성이 미백 관련한 기전에 영향을 미치지 않음을 확인하였다. 또한, 과일 주스 생산 후 발생하는 부산물을 활용한 블랙커런트를 추출물로 제조하여 tyrosinase 저해 활성을 평가한 선행연구(Plainfossé H 등 2020)에서 L-tyrosine을 기질로 tyrosinase 효소 저해 활성은 낮은 수준의 활성을 나타내었다. Tyrosinase 효소는 melanin 합성 경로에 있어 중요하게 작용하여 멜라닌의 생성 속도를 결정하는 효소로 tyrosinase의 생성은 멜라닌 양을 조절하여 멜라닌 합성으로 이어진다(Ando H 등 2007). 이러한 결과를 바탕으로 가공 후 박은 미백 활성 측면에서는 가공 전 원료에 비해 유의미한 효능이 관찰되지 않아, 기능성 미백 소재로의 활용 가능성은 제한적인 것으로 판단된다.
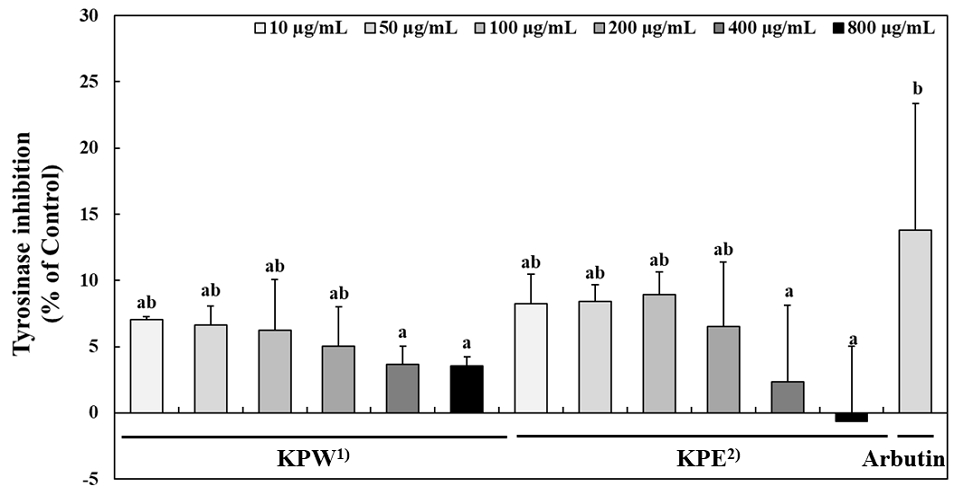
The tyrosinase inhibition activity of KPW and KPE.The tyrosinase inhibitory activities of kiwi pomace extracted with water (KPW) or 70% ethanol (KPE) were tested at concentrations of 10, 50, 100, 200, 400, and 800 µg/mL. Arbutin was used as a positive control at a concentration of 50 µg/mL. According to Duncan’s multiple range test (p<0.05), groups with a same letter are not significantly different.
요 약
본 연구에서 상업적 가공 과정에서 발생하는 키위박의 활용 가치를 탐색하고자 키위박으로부터 열수(KPW) 및 70% 에탄올(KPE) 추출물을 제조하고 이들의 항산화 활성을 측정하고자 총 페놀 함량, DPPH 라디칼 소거 활성, Cu(Ⅱ) 이온에 대한 환원력 및 tyrosinase 저해 활성을 측정하였다. KPW와 KPE의 총 페놀 함량은 각각 15.08 μg GAE/mL 그리고 27.80 μg GAE/mL를 나타내었으며 이는 이후 항산화 실험 결과와 상관관계를 보였다. DPPH 라디칼 소거 활성에서 가장 높은 농도인 800 μg/mL에서 KPW는 99.51% 그리고 KPE는 95.95%의 활성으로 동일 농도의 양성대조군인 vitamin C와 유사한 수준의 소거 활성을 나타냈다. 환원력 평가 결과, Cu(Ⅱ)에서 Cu(Ⅰ)로의 환원력은 KPW 45.89 μM, KPE 53.04 μM로 모두 높은 환원력을 나타냈다. 또한, tyrosinase 저해 활성은 미미하여, 미백 관련 효능에는 제한적인 효과를 나타냈다. 이상의 결과는 버려지는 키위박의 부가가치를 높이는 동시에, 항산화 기반의 건강기능성식품 및 기능성 화장품의 소재로서의 적용시켜 키위박의 높은 활용가능성을 제시한다.
References
-
Ancerewicz J, migliavacca E, Carrupt PA, Testa B, Brée F, Zini R, Tillement JP, Labidalle S, Guyot D, Chauvet-Monges AM, Crevat A, Le Ridant A (1998) Structure-property relationships of trimetazidine derivatives and model compounds as potential antioxidants. Free Radic Bio Med 25(1): 113-120.
[https://doi.org/10.1016/S0891-5849(98)00072-0]

-
Ando H, Kondoh H, Ichihashi M, Hearing VJ (2007) Approaches to identify inhibitors of melanin biosynthesis via the quality control of tyrosinase. J Invest Dermatol 127(4): 751-761.
[https://doi.org/10.1038/sj.jid.5700683]

-
Aruoma OI, Murcia A, Butler J, Halliwell B (1993) Evaluation of the antioxidant and prooxidant actions of gallic acid and its derivatives. J Agric Food Chem 41(11): 1880-1885.
[https://doi.org/10.1021/jf00035a014]

-
Ayala-Zavala JF, Vega-Vega V, Rosas-Domínguez C, Palafox-Carlos H, Villa-Rodriguez JA, Siddiqui MW, Dávila-Aviña JE, González-Aguilar GA (2011) Argo-industrial potential of exotic fruit byproducts as a source of food additives. Food Res Int 44(7): 1866-1874.
[https://doi.org/10.1016/j.foodres.2011.02.021]

-
Baiano A (2014) Recovery of biomolecules from food wastes: A review. Molecules 19(9): 14821-14842.
[https://doi.org/10.3390/molecules190914821]

-
Carbone K, Amoriello T, Iadecola R (2020) Exploitation of kiwi juice pomace for the recovery of natural antioxidants through microwave-assisted extraction. Agriculture 10(10): 435.
[https://doi.org/10.3390/agriculture10100435]

-
Catel-Ferreira M, Tnani H, Hellio C, Cosette P, Lebrun L (2015) Antiviral effects of polyphenols: Development of bio-based cleaning wipes and filters. J Virol Methods 212: 1-7.
[https://doi.org/10.1016/j.jviromet.2014.10.008]

-
Choi SJ, Cho EA, Cho EH, Jeong YJ, Ku CS, Ha BJ, Chae HJ (2011) Screening of functional materials from solvent fractions of apple flower leaf extract. Korean Society for Biotechnology and Bioengineering Journal 26(2): 165-171.
[https://doi.org/10.7841/ksbbj.2011.26.2.165]

-
Chung HJ, Kim CJ, Choi YS (2015) Comparison of antioxidant and nitrite scavenging activites of different colored kiwis cultivated in Korea. J Korean Soc Food Cult 30(2): 220-226.
[https://doi.org/10.7318/KJFC/2015.30.2.220]

-
Contreras-Guzmán ES, Strong FC (1982) Determination of tocopherols (vitamin E) by reduction of cupric ion. J AOAC Int 65(5): 1215-1221.
[https://doi.org/10.1093/jaoac/65.5.1215]

-
Garcia-Salas P, Morales-Soto A, Segura-Carretero A, Fernández-Gutiérrez A (2010) Phenolic-compound-extraction systems for fruit and vegetable samples. Molecules 15(12): 8813-8826.
[https://doi.org/10.3390/molecules15128813]

-
Herrero M, Sánchez-Camargo A del Pilar, Cifuentes A, Ibáñez E (2015) Plants, seaweeds, microalgae and food by-products as natural sources of functional ingredients obtained using pressurized liquid extraction and supercritical fluid extraction. TrAC Trends Anal Chem 71: 26-38.
[https://doi.org/10.1016/j.trac.2015.01.018]

-
Ignat I, Volf I, Popa VI (2011) A critical review of methods for characterisation of polyphenolic compounds in fruits and vegetables. Food Chem 126(4): 1821-1835.
[https://doi.org/10.1016/j.foodchem.2010.12.026]

-
Ilie GI, Milea ȘA, Râpeanu G, Cîrciumaru A, Stănciuc N (2022) Sustainable design of innovative kiwi byproducts-based ingredients containing probiotics. Foods 11(15): 2334.
[https://doi.org/10.3390/foods11152334]

-
Jin DE, Kim HJ, Jeong H, Jo TN, Kwon OJ, Choi SH, Heo HJ (2014) Nutritional components of zespri green kiwi fruit (Actinidia delicosa) and neuronal cell protective effects of the n-hexane fraction. Korean J Food Sci Technol 46(3): 369-374.
[https://doi.org/10.9721/KJFST.2014.46.3.369]

- Jung SW, Lee NK, Kim SJ, Han DS (1995) Screening of tyrosinase inhibitor from plants. Korean J Food Sci Technol 27(6): 891-896.
-
Kheirkhah H, Baroutian S, Quek SY (2019) Evalution of bioactive compounds extracted from Hayward kiwifruit pomace by subcritical water extraction. Food Bioprod Process 115: 143-153.
[https://doi.org/10.1016/j.fbp.2019.03.007]

-
Kim DI, Kim HJ, Lee JH, Han SJ, Kim HE, Park KS, Kim HJ, Nam JH, Chi GY, An BJ (2018) Anti-inflammation effect of hardy kiwifruit (Actinidia arguta) extract in lipopolysaccharide-stimulated macrophages by suppressing NF-kappaB pathway. Food Sci Preserv 25(5): 564-573.
[https://doi.org/10.11002/kjfp.2018.25.5.564]

-
Kim EJ, Choi JY, Yu M, Kim MY, Lee S, Lee BH (2012) Total polyphenols, total flavonoid contents, and antioxidant activity of Korean natural and medicinal plants. Korean J Food Sci Technol 44(3): 337-342.
[https://doi.org/10.9721/KJFST.2012.44.3.337]

-
Kim MS, Sung HJ, Park YJ, Shon HY (2017) Evaluation of anti-oxidant, anti-microbial and anti-thrombosis activities of fruit, seed and pomace of Schizandra chinensis Baillon. J Life Sci 27(2): 131-138.
[https://doi.org/10.5352/JLS.2017.27.2.131]

-
Latocha P (2017) The nutritional and health benefits of kiwiberry (Actinidia arguta): A review. Plat Foods Hum Nutr 72(4): 325-334.
[https://doi.org/10.1007/s11130-017-0637-y]

-
Ma T, Sun X, Zhao J, You Y, Lei Y, Gao G, Zhan J (2017) Nutrient compositions and antioxidant capacity of kiwifruit (Actinidia) and their relationship with flesh color and commercial value. Food Chem 218: 294-304.
[https://doi.org/10.1016/j.foodchem.2016.09.081]

-
Madsen HL, Nielsen BR, Bertelsen G, Skibsted LH (1996) Screening of antioxidative activity of spices. A comparison between assays based on ESR spin trapping and electrochemical measurement of oxygen consumption. Food Chem 57(2): 331-337.
[https://doi.org/10.1016/0308-8146(95)00248-0]

-
Martin-Cabrejas MA, Esteban RM, Lopez-Andreu FJ, Waldron K, Selvendran R (1995) Dietary fiber content of pear and kiwi pomaces. J Agric Food Chem 43(3): 662-666.
[https://doi.org/10.1021/jf00051a020]

-
Mazzoni L, Ariza Fernández MT, Capocasa F (2021) Potential health benefits of fruits and vegetables. Appl Sci 11(19): 8951.
[https://doi.org/10.3390/app11198951]

-
Moller JKS, Madsen HL, Aaltonen T, Skbsted LH (1999) Dittany (Origanum dictamnus) as a source of water-extractable antioxidants. Food Chem 64(2): 215-219.
[https://doi.org/10.1016/S0308-8146(98)00143-5]

-
Moshtaghian H, Bolton K, Rousta K (2021) Challenges for upcycled foods: Definition, inclusion in the food waste management hierarchy and public acceptability. Foods 10(11): 2874.
[https://doi.org/10.3390/foods10112874]

-
Paredes-López O, Cervantes-Ceja ML, Vigna-Pérez M, Hernández-Pérez T (2010) Berries: Improving human health and healthy aging, and promoting quality life: A review. Plant Foods Hum Nutr 65(3): 299-308.
[https://doi.org/10.1007/s11130-010-0177-1]

- Park DB, Lee YJ, Kim WS, Kim YT (2025) Anti-skin aging and antihypertensive activities of different solvent extracts from Sargassum thunbergii. Korean J Fish Aquat Sci 58(2): 140-145.
- Park YS, Lee GS, Korsak T, Park YJ, Oh DM, Heo BG (2009) Chemical composition of kiwifruits, their anti-microbial activity and their hyperplasia inhibition effect of against lung cancer cells. J East Asian Soc Diet Life 19(2): 202-209.
-
Pinto D, Delerue-Matos D, Rodrigues F (2020) Bioactivity, phytochemical profile and pro-healthy properties of Actinidia arguta: A review. Food Res Int 136: 109449.
[https://doi.org/10.1016/j.foodres.2020.109449]

-
Plainfossé H, Trinel M, Verger-Dubois G, Azoulay S, Burger P, Fernandez X (2020) Valorisation of Rives nigrum L. pomace, an agri-food by-product to design a new cosmetic active. Cosmetics 7(3): 56.
[https://doi.org/10.3390/cosmetics7030056]

-
Sato M, Ramarathnam N, Suzuki Y, Ohkubo T, Takeuchi M, Ochi H (1996) Varietal differences in the phenolic content and superoxide radical scavenging potential of wines from different sources. J Agric Food Chem 44(1): 37-41.
[https://doi.org/10.1021/jf950190a]

-
Shon MS, Kim RH, Kwon OJ, Roh SS, Kim GN (2016) Beneficial role and function of fisetin in skin health via regulation of the CCN2/TGF-β signaling pathway. Food Sci Biotechnol 25(Suppl 1): 133-141.
[https://doi.org/10.1007/s10068-016-0110-y]

-
Siddhuraju P, Mohan PS, Becker K (2002) Studies on the antioxidant activity of Indian Laburnum (Cassia fistula L.): A preliminary assessment of crude extracts from stem bark, leaves, flowers, and fruit pulp. Food Chem 79(1): 61-67.
[https://doi.org/10.1016/S0308-8146(02)00179-6]

-
Singletary K (2012) Kiwifruit: Overview of potential health benefits. Nutrition Today 47(3): 133-147.
[https://doi.org/10.1097/NT.0b013e31825744bc]

-
Singleton VL, Orhofer R, Lamuela-Raventós RM (1999) Analysis of total phenols and other oxidation substrates and antioxidants by means of Folin-Ciocalteu reagent. Methods Enzymol 299: 152-178.
[https://doi.org/10.1016/S0076-6879(99)99017-1]

-
Song YW, Moon KS, Cho SK (2013) Antioxidant activity and nutrient content of ethanol and hot-water extracts of Citrus unshiu pomace. J Korean Soc Food Sci Nutr 42(9): 1345-1350.
[https://doi.org/10.3746/jkfn.2013.42.9.1345]

-
Wang Y, Li L, Liu H, Zhao T, Meng C, Liu Z, Liu X (2018) Bioactive compounds and in vitro antioxidant activities of peel, flesh and seed powder of kiwi fruit. Int J Food Sci Technol 53(9): 2239-2245.
[https://doi.org/10.1111/ijfs.13812]

-
Xiong Q, Kadota S, Tadata T, Namba T (1996) Antioxidative effects of phenylethanoids from Cistanche deserticola. Biol Pharm Bull 19(12): 1580-1585.
[https://doi.org/10.1248/bpb.19.1580]

-
Yang HS, Hwang KA, Choi AJ, Kim MA, Kim DH, Im PR (2025) A study on consumer perception and demand for products from agri-food by-products upcycling products according to their interest in environmental issues. J Korean Soc Food Sci Nutr 54(2): 164-177.
[https://doi.org/10.3746/jkfn.2025.54.2.164]