
기능성 식품 소재로서 자연산 및 재배 번행초(Tetragonia tetragonoides)의 항산화 및 항염증 활성 평가
Abstract
This study examined and compared the antioxidant and anti-inflammatory activities of Tetragonia tetragonoides (Tt) extracts obtained from wild and freshwater-cultivated sources, with the aim to assess their potential as functional food ingredients. Antioxidant capacity was evaluated by measuring total polyphenol, tannin, and flavonoid contents, as well as 2,2′-azino-bis (3-ethylbenzothiazoline-6-sulfonic acid) (ABTS) and 1,1-diphenyl-2-picrylhydrazyl (DPPH) radical scavenging activities. The wild Tt extract showed significantly higher levels of antioxidant compounds and stronger radical scavenging activity compared to the cultivated extract (p<0.05). The cytotoxicity and anti-inflammatory effects were assessed using RAW 264.7 macrophage cells. Neither extract exhibited cytotoxicity up to a concentration of 100 μg/mL. Furthermore, treatment with 50 μg/mL of either extract significantly reduced lipopolysaccharide (LPS, 1 μg/mL)-induced inflammatory responses. Notably, the cultivated Tt extract more effectively suppressed nitric oxide (NO) production and cyclooxygenase-2 (COX-2) protein expression, while the wild Tt extract more strongly inhibited the production of pro-inflammatory cytokines, including tumor necrosis factor-alpha (TNF-α), interleukin-6 (IL-6), and interleukin-1 beta (IL-1β). These results suggest that Tetragonia tetragonoides possesses strong antioxidant and anti-inflammatory properties, with distinct functional profiles depending on the environment where it is grown. The findings support the potential use of both wild and cultivated Tetragonia tetragonoides as natural resources for the development of functional foods and health-promoting products.
Keywords:
Tetragonia tetragonoides, antioxidant activity, anti-inflammatory activity, polyphenols, RAW 264.7 cells서 론
염증은 생명체의 생로병사 과정에서 중요한 병리적 요소로 작용하며(Fullerton JN & Gilroy DW 2016), 화학적 또는 물리적 자극에 대한 인체의 방어 기전으로서 급성 염증은 조직 손상을 회복시키는 데 핵심적인 역할을 한다. 그러나 염증이 장기간 지속될 경우 다양한 만성 질환의 원인으로 작용할 수 있다(Furman D 등 2019). 염증 반응은 자극에 따라 prostaglandin(PG), leukotriene(LT) 등의 생리활성 물질이 생성되면서 시작되며(Das UN 2021), 그 과정에서 면역 반응의 핵심 세포인 대식세포는 병원체를 탐식하는 동시에 tumor necrosis factor-alpha(TNF-α), interleukin-6(IL-6), interleukin-1 beta(IL-1β) 등의 염증성 사이토카인을 분비하여 초기 염증 반응을 유도한다(Chen L 등 2018; Medzhitov R 2021). 또한, 대식세포는 inducible nitric oxide synthase(iNOS)와 cyclooxygenase-2 (COX-2)의 발현을 유도하여 NO(nitric oxide)와 PGE2(prostaglandin E2) 등의 염증 유발 인자를 생성하며, 이 중 NO는 면역 조절, 혈관 확장, 신경 전달 등 다양한 생리적 기능을 갖지만 과도하게 생성될 경우 조직 손상, 유전자 변이 및 신경독성 등을 유발할 수 있다(Okin D & Medzhitov R 2012; Low M 등 2024).
최근 건강에 대한 관심이 높아짐에 따라 부작용이 적은 항염증 활성을 가진 천연 소재에 대한 수요가 증가하고 있으나, 여전히 다양한 기능성 천연자원에 대한 연구는 미흡한 실정이다(Gandhi GR 등 2021; Gouda NA 등 2023). 번행초(Tetragonia tetragonoides)는 전통적으로 해풍과 염분이 강한 해안 지역에서 자생하며 식용 및 약용으로 활용되어 온 염생 식물로(Yoon JA 2020), 최근 다양한 생리활성이 보고되면서 기능성 소재로서의 관심이 높아지고 있다(Lee MA 등 2008; Chung HJ 등 2015). 특히, 번행초 추출물은 streptozotocin(STZ)으로 유도된 제1형 당뇨 동물 모델에서 혈당 강하 효과를 나타내었으며(Choi GY 등 2017), α-amylase, α-glucosidase, aldose reductase 등 당대사 관련 효소에 대한 저해 활성이 보고되었다(Choi HJ 등 2008). 이 외에도 항염증 및 종양 억제 효과(Choi HJ 등 2015), 미백 활성(Jo JB 등 2016), 항산화 기능(Park YK & Nam UH 2002) 등이 보고된 바 있으며, 최근에는 RAW 264.7 대식세포를 이용한 실험에서 번행초 추출물이 lipopolysaccharide(LPS)로 유도된 산화 스트레스 및 염증 반응을 효과적으로 억제하는 것이 확인되었다(Kong JH 등 2020). 이러한 결과는 번행초가 항산화 및 항염증 기능을 지닌 천연물 소재로서의 활용 가능성을 시사하며, 생육 환경에 따른 기능성 성분 함량의 차이가 생리활성에 영향을 줄 수 있음을 보여준다.
이에 본 연구에서는 천연 자원으로서의 가치를 지닌 번행초를 대상으로, 자연산과 담수 환경에서 재배된 시료 간의 항산화 및 항염증 활성을 비교하여 기능성 식품소재로서의 번행초 대량생산 가능성을 평가하고자 한다. 특히 바닷가에서 자생한 번행초와 담수 환경 하에 재배한 번행초의 생리활성 차이를 분석함으로써, 번행초의 기능성 원료로서의 산업적 활용 가능성 방향을 제시하고자 한다.
재료 및 방법
1. 시료 전처리 및 보관
자연산 및 재배 번행초(Tetragonia tetragonoides)는 각각 제주 가파도 지역과 동일 지역 내 실험용 담수 재배지에서 수확하였다. 수확한 시료는 이물질 제거를 위해 흐르는 물에 세척한 뒤, 60℃에서 열풍 건조(hot-air drying)하였다. 완전히 건조된 시료는 분쇄기(미니분쇄기, HMF-3100S, Hanil Electric Co., Seoul, Korea)를 이용하여 균질하게 분말화하였으며, 40 mesh 체를 통과시켜 입자 크기를 표준화하였다.
분말화된 시료는 —80℃에서 24 h 동안 예비 냉동한 후, 동결건조기(FD8508, Ilshin Lab Co., Ltd, Dongducheon, Korea)를 이용하여 완전히 수분을 제거하였다. 동결건조된 시료는 밀봉 가능한 갈색 폴리에틸렌 병에 담아 4℃ 냉장 조건에서 보관하였으며, 실험 전까지 빛과 습기로부터 차단된 상태로 유지하였다.
2. Tetragonia tetragonoides 추출물 제조
동결건조한 Tetragonia tetragonoides 분말 10 g에 95% ethanol 20 mL를 첨가한 후, 고속균질기(Homogenizer, 10,000 rpm, 2 min)로 균질화하였다. 이어서 3,000 rpm에서 15 min 간 원심분리하고, 상등액을 여과하여 액상 시료로 사용하였다. 추출물은 —20℃에 보관하여 실험에 사용하였다.
3. 시약 및 기기
세포 배양에 사용된 Roswell Park Memorial Institute(RPMI)-1640 배지와 fetal bovine serum(FBS), 단백질 분석에 사용된 acrylamide:bis 30%, 29:1 solution(A0418-050), protease inhibitor, radioimmunoprecipitation assay(RIPA) buffer는 모두 GenDEPOT(Baker, TX, USA)에서 구입하였다. Streptomycinpenicillin은 Gibco™(Waltham, MA, USA)에서, bicinchoninic acid(BCA) protein assay kit는 Thermo Fisher Scientific(Waltham, MA, USA)에서, polyvinylidene fluoride(PVDF) membrane과 Immobilon Western Chemiluminescent HRP Substrate는 Millipore(Burlington, MA, USA)에서 구매하였다. Griess reagent 및 기타 일반 시약은 Sigma-Aldrich(St. Louis, MO, USA)에서 구입하여 사용하였다.
Western blot 분석에 사용된 1차 항체 중 COX-2 항체(ab15191)는 Abcam(Cambridge, UK)에서, β-actin 항체(SC-47778)는 Santa Cruz Biotechnology(Dallas, TX, USA)에서 구매하였다. 2차 항체인 horseradish peroxidase(HRP)-conjugated goat anti-rabbit IgG (H+L)-HRP(SA002-500) 및 goat anti-mouse IgG (H+L)-HRP (SA001-500)는 GenDEPOT(Baker, TX, USA)에서 구입하였다. TNF-α, IL-6, IL-1β 측정을 위한 ELISA 키트는 Koma Biotech Inc.(Seoul, Korea)에서 구매하여 사용하였다.
4. 총 폴리페놀, 타닌, 및 플라보노이드 함량 분석
총 폴리페놀 함량은 Folin O & Denis W(1912)의 방법을 변형하여 분석하였다. 시료 25 μL에 증류수 500 μL와 2 N Folin–Ciocalteu’s phenol reagent(50 μL; Sigma-Aldrich, St. Louis, MO, USA)를 첨가한 뒤, 실온에서 3 min 동안 반응시켰다. 이후 20% 탄산나트륨(Na2CO3) 용액 500 μL를 가하고 암실에서 1 h 동안 반응시킨 후, 725 nm에서 흡광도를 측정하였다. 표준물질로는 gallic acid(Sigma-Aldrich)를 사용하였으며, 다양한 농도의 gallic acid로 작성한 검량선의 회귀식은 y=0.0014x+0.0362(R2=0.9966)였다. 시료의 흡광도 값을 해당 검량선에 적용하여 총 폴리페놀 함량을 mg gallic acid equivalents (GAE)/g dry weight로 산출하였다.
총 타닌 함량은 Duval B & Shetty K(2001)의 방법을 기반으로 측정하였다. 시료 200 μL에 증류수 200 μL와 95% ethanol 200 μL를 첨가하고, 이어서 5% Na2CO3 200 μL와 1 N Folin–Ciocalteu reagent 100 μL를 순차적으로 첨가하였다. 반응 혼합물은 암실에서 1 h 동안 반응시킨 후, 725 nm에서 흡광도를 측정하였다. 표준물질로는 tannic acid(Sigma-Aldrich)를 사용하였으며, 검량선은 y=0.0197x+0.4205(R2=0.9999)로 작성되었다. 이를 바탕으로 총 타닌 함량은 mg tannic acid equivalents(TAE)/g dry weight로 환산하였다.
총 플라보노이드 함량은 Zhishen J 등(1999)의 방법을 변형하여 분석하였다. 시료 100 μL에 증류수 400 μL와 5% sodium nitrite(NaNO2) 30 μL를 첨가하고 상온에서 5 min 간 반응시켰다. 이어서 10% aluminum chloride(AlCl3·6H2O) 30 μL를 첨가하고 6 min 간 반응시킨 후, 1 M sodium hydroxide(NaOH) 200 μL와 증류수 240 μL를 순차적으로 추가하였다. 최종 반응 혼합물은 510 nm에서 흡광도를 측정하였으며, 표준물질로는 catechin(Sigma-Aldrich)을 사용하였다. 검량선의 회귀식은 y=0.0014x+0.0417(R2=0.9994)로 작성되었으며, 총 플라보노이드 함량은 μg catechin equivalents (CE)/g dry weight 단위로 환산하였다.
5. ABTS 및 DPPH 라디칼 소거능 분석
ABTS 라디칼 소거능은 Re R 등(1999)의 방법을 변형하여 측정하였다. ABTS 용액은 7.0 mM ABTS(2,2′-azino-bis (3-ethylbenzothiazoline-6-sulfonic acid); Sigma-Aldrich, USA)와 2.45 mM potassium persulfate를 혼합하여 암실에서 상온으로 13 h 반응시켜 생성하였다. 이 ABTS 용액은 phosphate-buffered saline(PBS, pH 7.4)를 이용해 734 nm에서의 흡광도가 0.700±0.02가 되도록 조정하였다. 이후 액상 시료 200 μL와 희석된 ABTS 용액 800 μL를 혼합하여 암실에서 실온으로 5 min 간 반응시킨 뒤, 734 nm에서 흡광도를 측정하였다. 대조군(control)은 동일한 조건에서 시료 대신 추출용매(95% ethanol)를 처리한 용액을 사용하였다. ABTS 라디칼 소거능은 다음 식을 이용하여 계산하였다:
DPPH 라디칼 소거능은 Blois MS(1958)의 방법을 변형하여 측정하였다. 앞선 시료 준비와 동일하게, 95% ethanol 20 mL에 시료 10 g을 혼합하여 10,000 rpm에서 2 min 간 균질화한 후, 3,000 rpm에서 15 min 간 원심분리하고 여과하여 액상 시료를 얻었다. 이후 시료 100 μL에 0.2 mM DPPH(1,1-diphenyl-2-picrylhydrazyl; Sigma-Aldrich, St. Louis, MO, USA) 용액 100 μL를 혼합하여 실온에서 30 min 동안 반응시킨 후, 517 nm에서 흡광도를 측정하였다. DPPH 분석에서도 control은 DPPH 용액에 추출용매만을 처리한 것을 기준으로 하였다. DPPH 라디칼 소거능은 다음과 같이 산출하였다:
6. 세포 배양
RAW 264.7 대식세포는 RPMI-1640에 10% heat-inactivated FBS와 100 U/mL penicillin-streptomycin을 첨가한 배지에서 배양하였다. 실험은 세포의 안정성을 확보하기 위해 10∼12회 계대 배양된 세포를 사용하였으며, 모든 세포는 37℃, 5% CO2 조건의 가습된 인큐베이터(BB15 CO2 Incubator, Thermo Fisher Scientific, Waltham, MA, USA)에서 배양하였다.
7. 세포 생존율 측정
RAW 264.7 세포의 생존율은 MTT[3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetra-zolium bromide] 분석을 통해 평가하였다. 세포는 2 × 104 cells/mL의 농도로 96-well plate에 분주하였으며, 37℃, 5% CO2 조건의 인큐베이터(BB15 CO2 Incubator, Thermo Fisher Scientific, Waltham, MA, USA)에서 3 h 동안 안정화시켰다. 이후 자연산 및 재배 번행초 추출물을 각각 50 μg/mL 농도로 처리한 후 24 h 동안 배양하였다. 또한 자연산 및 재배 번행초 추출물을 각각 처리하여 1 h 동안 배양한 뒤 lipopolysaccharide(LPS, 1 μg/mL)를 처리하여 24 h 추가 배양하였다. 배양 후 well 당 20 μL의 MTT 용액(0.5 mg/mL)을 첨가하고, 37℃, 5% CO2 조건의 인큐베이터에서 4 h 동안 반응시켰다. 반응 종료 후 상등액을 제거하고, 생성된 formazan 결정은 DMSO로 용해시킨 뒤, microplate reader (Synergy H1, BioTek, Winooski, VT, USA)를 이용하여 540 nm에서 흡광도를 측정하였다.
8. 일산화질소(Nitric Oxide, NO) 생성량 측정
RAW 264.7 대식세포는 DMEM 배지에 현탁한 후, 2 × 105 cells/mL의 농도로 24-well plate에 분주하고, 37℃, 5% CO2 조건의 인큐베이터(BB15 CO2 Incubator, Thermo Fisher Scientific, Waltham, MA, USA)에서 3 h 동안 안정화시켰다. 이후 세포에 자연산 및 재배 번행초 추출물을 각각 처리하여 1시간 동안 배양한 뒤 lipopolysaccharide(LPS, 1 μg/mL)를 처리하여 24 h 추가 배양하였다. 배양 후 상등액을 수거하여 NO 생성을 측정하였다. 측정은 배양액 100 μL와 동일 부피의 Griess 시약(1% sulfanilamide, 0.1% naphthylethylene-diamine dihydrochloride in 2.5% phosphoric acid)을 혼합한 후, 실온에서 10 min 간 반응시킨 뒤 microplate reader(Synergy H1, BioTek, Winooski, VT, USA)를 이용하여 540 nm에서 흡광도를 측정하였다. 배양액 내 NO 농도는 sodium nitrite(NaNO2)로 작성한 표준곡선을 기반으로 산출하였다. 검량선 공식은 y=0.0167x+0.0448(R²=0.9998)이며, 여기서 y는 흡광도, x는 NO 농도(μM)를 나타낸다.
9. COX-2 단백질 발현 분석
COX-2 단백질 발현을 분석하기 위해 RAW 264.7 대식세포를 DMEM 배지에 현탁하여 6×105 cells/mL의 농도로 60 mm 세포 배양접시에 분주하였고, 37℃, 5% CO2 조건의 인큐베이터(BB15 CO2 Incubator, Thermo Fisher Scientific, Waltham, MA, USA)에서 3 h 동안 배양하여 안정화시켰다. 이후 자연산 또는 재배 번행초 추출물(50 μg/mL)을 처리하여 1 h 동안 배양한 뒤, LPS (1 μg/mL)를 처리하여 24 h 추가 배양하였다. 배양 후 배지를 제거하고, 세포를 ice-cold PBS로 세척한 뒤 lysis buffer를 첨가하여 단백질을 추출하였다. 추출된 단백질은 원심분리 후 상등액을 수거하여 새로운 튜브에 옮겼으며, 일부는 단백질 정량에 사용하고, 나머지는 —20℃에 보관하였다.
총 단백질 농도는 bicinchoninic acid(BCA) protein assay kit를 이용하여 정량하였으며, 50 μg의 단백질을 8% sodium dodecyl sulfate–polyacrylamide gel electrophoresis(SDS–PAGE)를 통해 분리한 후 Trans-Blot Turbo Transfer System(Bio-Rad Laboratories, Hercules, CA, USA)을 이용하여 polyvinylidene fluoride(PVDF) membrane에 전이시켰다. 5% skim milk가 포함된 Tris-buffered saline with 0.1% Tween-20(TBST)로 1 h 차단한 뒤, COX-2 1차 항체(1:1,000 희석)를 4℃에서 overnight 반응시켰다. 이후 TBST로 10 min 간격으로 3회 세척한 뒤, horseradish peroxidase (HRP)-conjugated 2차 항체(1:1,000 희석)를 상온에서 1 h 반응시켰다. 다시 TBST로 3회 세척한 후, 암실에서 Immobilon Western Chemiluminescent HRP Substrate로 반응시켜 밴드를 발현시켰고, KwikQuant Imager(Kindle Biosciences LLC, CT, USA)를 이용하여 이미지를 촬영하였다. 단백질 발현 수준은 β-actin을 기준으로 정규화하였으며, ImageJ 소프트웨어(NIH, USA)를 활용하여 밴드 강도를 정량 분석하였다.
10. TNF-α, IL-1β, IL-6 생성량 측정
RAW 264.7 세포를 24-well plate에 분주한 후 3 h 동안 안정화시켰다. 이후 LPS(1 μg/mL) 단독 또는 번행초 추출물(50 μg/mL)과 함께 24 h 동안 처리하였다. 이후 세포 배양 상등액을 수거하여, TNF-α, IL-1β, IL-6의 농도를 각각의 enzyme-linked immunosorbent assay(ELISA) kit를 사용하여 정량하였다.
분석에는 Mouse TNF-α ELISA kit, Mouse IL-1β ELISA kit, Mouse IL-6 ELISA kit(R&D Systems, Minneapolis, MN, USA)를 사용하였으며, 제조사의 지침에 따라 96-well plate에 샘플 또는 표준물질을 분주한 후, 각 키트에 지정된 캡처 항체와 검출 항체를 순차적으로 반응시켰다. 반응 후 substrate solution을 가하여 20 min 간 실온에서 암실 내 반응시킨 후, stop solution을 첨가하고 450 nm에서 흡광도(OD)를 측정하였다. 사이토카인 농도는 표준물질의 검량선을 기반으로 산출하였다.
11. 통계 분석
모든 실험은 3회 반복하여 수행하였으며, 결과는 평균±표준편차(mean±standard deviation, S.D.)로 표기하였다. 통계 분석은 SPSS software (version 23.0; SPSS Inc., Chicago, IL, USA)를 이용하여 수행하였으며, 각 처리군 간의 유의성 검증을 위해 일원분산분석(one-way ANOVA) 및 독립표본 t-검정(independent t-test)을 실시하였다. ANOVA 후에는 Tukey 또는 Duncan의 다중 비교 검정(post hoc test)을 적용하여 그룹 간 차이를 평가하였다. 통계적 유의성은 p 값이 0.05 미만인 경우로 판단하였다(p<0.05). 모든 그래프는 GraphPad Prism(Version 5.01; GraphPad Software, Boston, MA, USA)을 사용하여 작성하였다.
결과 및 고찰
1. 총 폴리페놀, 타닌 및 총 플라보노이드 함량
Tetragonia tetragonoides 추출물의 총 폴리페놀, 타닌, 및 플라보노이드 함량은 Table 1에 제시하였다. 식물성 페놀 화합물은 hydroxyl기를 포함한 방향족 구조를 가지며, 라디칼 소거 및 항산화 활성을 나타내는 주요 생리활성 성분으로 알려져 있다(Kim BG 등 2016). 본 연구에서 담수 재배된 번행초의 총 폴리페놀 함량은 517.95±19.43 mg GAE/g이었으며, 이는 자연산 번행초(764.86±5.74 mg GAE/g)에 비해 유의하게 낮은 수치를 나타내었다(p<0.05). 이와 같은 경향은 자연 환경에서의 자외선, 염분, 건조, 병해충 등 다양한 스트레스 요인이 페놀성 화합물의 생합성을 자극할 수 있음을 시사하며, Woo KS 등(2015)은 식물 생육 단계나 발아 시간에 따른 페놀 함량의 변동 가능성을 보고한 바 있다. Lee MA 등(2008) 또한 추출 용매에 따라 번행초에서 얻어지는 총 페놀 함량이 상이하며, dichloromethane, ethanol, methanol, butanol 순으로 증가하는 경향을 보인다고 보고하였다. 이러한 결과는 번행초에 존재하는 페놀성 화합물이 상대적으로 비극성 또는 중간 극성 용매에서 더 효율적으로 추출될 수 있음을 시사한다.
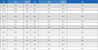
Comparison of total polyphenol, tannin, and flavonoid contents between wild and cultivated Tetragonia tetragonoides
타닌은 항산화 및 항균 활성을 가지며, 해양 식물이나 염생 식물에 특히 풍부한 것으로 알려져 있다(Woo KS 등 2015). 본 연구 결과, 자연산 번행초의 타닌 함량은 180.01±39.84 mg TAE/g으로, 재배 번행초(127.81±37.10 mg TAE/g)보다 유의하게 높았다(p<0.05). 이는 해안가의 염분 환경이 타닌의 생합성에 긍정적인 영향을 미쳤을 가능성을 보여주며, 실제로 Ksouri R 등(2007)은 염 스트레스가 식물 내 페놀 및 타닌류 축적을 촉진한다고 보고하였다.
플라보노이드는 폴리페놀의 하위 그룹에 속하는 항산화 화합물로(Alam F 등 2022; Li H 등 2024; Jomova K 등 2025), hydroxyl기를 통해 라디칼을 안정화시키며 항산화 활성을 발휘한다(Panche AN 등 2016). 본 연구에서 플라보노이드 함량은 catechin equivalents(CE) 기준으로 산출하였으며, 자연산 번행초는 925.69±8.17 μg CE/g, 재배 번행초는 412.60±9.23 μg CE/g으로 확인되었다(p<0.05). 특히 자연산 시료는 약 2배 이상의 플라보노이드를 함유하고 있었다. 이는 flavonoid가 자연환경에서 유도되는 산화 스트레스에 대응하기 위해 증가할 수 있음을 보여주며, Pietta PG(2000)는 quercetin, kaempferol, catechin 등 다양한 플라보노이드가 ABTS 및 DPPH 라디칼에 대한 소거 활성을 나타낸다고 보고하였다.
Folin-Ciocalteu 법은 환원성 물질(예: 단백질, 당류 등)에도 반응할 수 있어 실제 페놀 함량이 과소 또는 과대 추정될 수 있으며(Naczk M & Shahidi F 2006; Ainsworth EA & Gillespie KM 2007), 반면 알루미늄 클로라이드 착염법은 catechol 구조를 가진 특정 플라보노이드에 특이적으로 반응하여 플라보노이드 함량을 상대적으로 높게 나타낼 수 있다(Kim DO 등 2003). 또한 총 폴리페놀과 플라보노이드를 각각 mg GAE/g, μg CE/g의 단위로 표기함에 따라 단위 간 변환을 고려하지 않으면 오해가 발생할 수 있다. 유사하게 정량법 차이에 따른 함량 역전 현상은 다른 연구들에서도 보고된 바 있으며(Dai J & Mumper RJ 2010; Ignat I 등 2011), 본 연구 결과는 번행초에 상대적으로 플라보노이드가 풍부하게 존재함을 시사한다.
아울러 염생 식물은 고염 환경에 의한 산화 스트레스에 대응하기 위해 항산화 화합물의 생합성을 강화하는 기전을 발달시켜 왔다(Ahn BK 등 2021). 고염 조건에서 기공 폐쇄 및 광합성 장애로 인해 ROS가 축적되며, 이로 인해 페놀 및 플라보노이드 함량이 증가하는 것으로 알려져 있다(Sies H 등 2024). 실제로 Hsueh TP 등(2021)은 고온·건조한 환경에서 자란 Artemisia capillaris가 항염증 관련 성분을 더 많이 축적한다고 보고하였으며, 이는 환경 스트레스가 생리활성 물질의 축적을 유도할 수 있음을 지지한다. 이러한 결과는 자연산 번행초가 극한 환경에 대응하기 위해 항산화 성분을 풍부하게 축적하고 있음을 나타내며, 기능성 소재로서의 활용 가능성이 높음을 시사한다. 향후에는 HPLC 기반 개별 성분 정량 및 정제된 표준화 방법을 통한 보완 연구가 필요할 것이다.
2. ABTS 및 DPPH 라디칼 소거 활성
인체 대사 과정에서 생성되는 유해한 자유 라디칼은 세포 손상 및 노화, 염증, 각종 질환을 유발할 수 있으며, ABTS⁺ 및 DPPH 라디칼은 이러한 반응을 대표적으로 모사하는 실험적 모델이다(Chung HJ 등 2015; Ryu JY 등 2018). Tetragonia tetragonoides 추출물의 항산화 활성을 평가하기 위해 ABTS 및 DPPH 라디칼 소거능을 측정하였으며, 그 결과는 Fig. 1에 제시하였다. ABTS 라디칼 소거능은 ABTS 용액과 과황산칼륨의 반응을 통해 생성된 청록색의 양이온 라디칼(ABTS⁺)이 항산화제에 의해 소거됨으로써 탈색되는 정도를 기반으로 평가된다(Kim KH 등 2013). 분석 결과, 자연산 번행초 추출물은 34.83±12.71%의 ABTS 라디칼 소거 활성을 나타내었으며, 이는 담수 재배 번행초의 9.98±3.04%에 비해 유의하게 높은 수치였다(p<0.05). ABTS 라디칼 소거능은 자유 라디칼(free radical)에 전자를 공여함으로써 산화 스트레스를 저감하고, 식품에서는 저장성 향상, 인체에서는 세포 손상 예방 및 질병 억제에 기여하는 항산화 지표로 활용된다(Kim JE 등 2009).
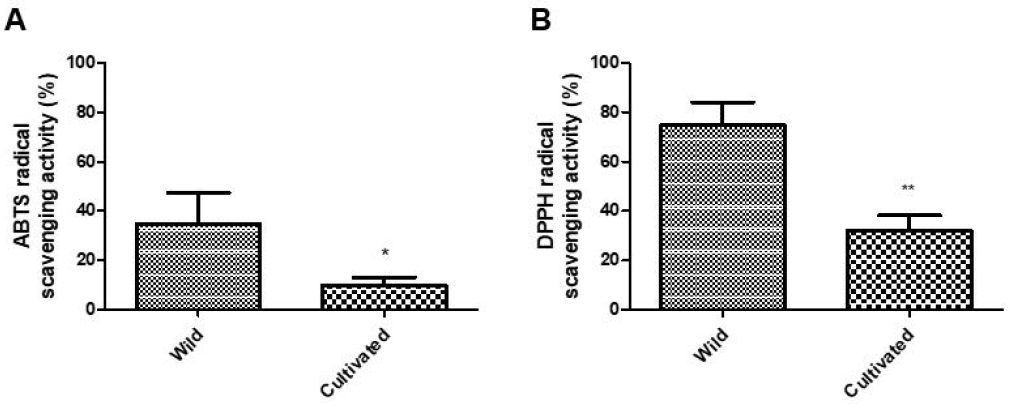
Antioxidant activities of Tetragonia tetragonoides extracts assessed by ABTS and DPPH radical scavenging assays. Antioxidant activities of wild and cultivated Tetragonia tetragonoides (Tt) extracts were evaluated using ABTS and DPPH radical scavenging assays. Ethanol extracts (95%) of wild-harvested and freshwater-cultivated T. tetragonoides powders were tested under identical conditions. Data are expressed as the mean±standard deviation (S.D.) of three independent experiments. Wild: wild T. tetragonoides extract-treated group; Cultivated: cultivated T. tetragonoides extract-treated group. *p<0.05, **p<0.01 vs. Wild.
DPPH 라디칼 소거능은 항산화 활성을 평가하는 대표적인 방법으로, 자색의 DPPH 라디칼이 환원되면서 탈색되는 정도를 측정하는 방식이다. 자연산 번행초는 74.81±7.57%의 DPPH 라디칼 소거 활성을 보였으며, 이는 담수 재배 번행초의 32.12±4.98%보다 유의하게 높은 수치였다(p<0.05). DPPH 라디칼 소거능은 항산화제가 지질 과산화 반응 등에서 자유 라디칼에 전자를 공여하여 연쇄적인 산화 반응을 차단함으로써 항노화, 항염증, 만성질환 예방 등의 생리활성을 나타내는 것으로 보고되어 있다(Woo KS 등 2015). 한편, Park GH 등(2011)의 연구에 따르면 감귤류 추출물의 DPPH 라디칼 소거 활성은 약 41.9∼58.2% 수준으로 보고된 바 있으며, 이는 본 연구에서 확인된 자연산 번행초의 소거 활성(74.81±7.57%)보다 낮은 수치이다. 이는 자연산 번행초가 항산화 활성이 우수한 천연 소재로 활용될 수 있음을 시사한다.
또한, Lee ES 등(2023)은 번행초 추출물이 농도 의존적으로 ROS 생성을 억제함을 보고한 바 있으며, 이러한 선행연구 결과는 번행초가 항산화 활성을 지니고 있음을 뒷받침하며, 본 연구에서 확인된 라디칼 소거 활성 결과와도 그 경향이 유사하다. 다만, 본 연구에서는 라디칼 소거 활성의 농도 의존성을 직접적으로 평가하지는 않았다.
결과적으로, 자연산 번행초는 담수 재배 번행초에 비해 유의하게 높은 ABTS 및 DPPH 라디칼 소거 활성을 나타냈으며, 이는 본 식물에 함유된 총 폴리페놀, 타닌, 플라보노이드 등 항산화 관련 성분의 상대적 풍부함에 기인한 것으로 사료된다. 이러한 결과는 번행초가 천연 항산화 소재로서 기능성 식품 및 건강보조소재로의 활용 가능성이 높음을 시사한다.
3. 번행초가 RAW 264.7 세포 생존률에 미치는 영향
RAW 264.7 마우스 유래 대식세포에서 번행초 추출물의 세포독성을 평가하기 위해 MTT 분석을 수행하였다. 자연산 및 재배 번행초 추출물을 각각 50 μg/mL의 농도로 24시간 처리한 결과, 두 시료 모두에서 유의한 세포 독성이 관찰되지 않았다(Fig. 2). 더불어, 고농도인 100 μg/mL 처리 조건에서도 세포 생존률에 유의한 감소가 나타나지 않아, 본 실험에 사용된 번행초 농도 범위는 RAW 264.7 세포에 대해 세포독성이 없는 것으로 판단된다. 이에 따라 후속 실험에서는 50 μg/mL의 농도를 기준으로 생리활성 평가를 진행하였다.
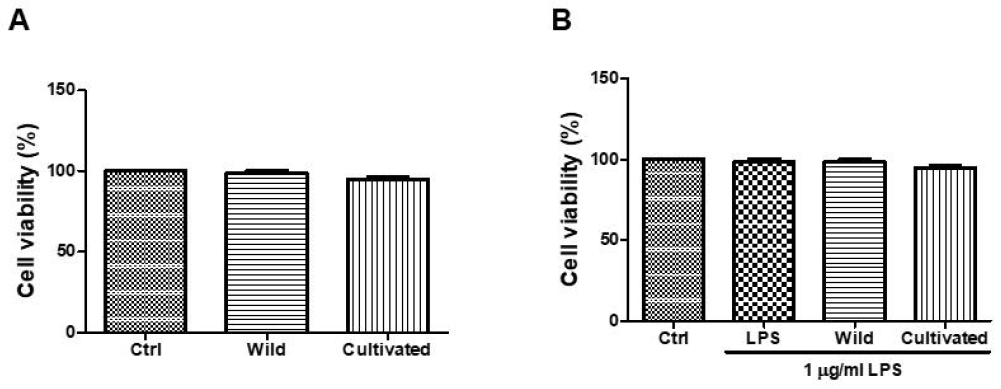
Effect of Tetragonia tetragonoides extracts on RAW 264.7 cell viability. Effects of wild and cultivated Tetragonia tetragonoides (Tt) extracts on the viability of RAW 264.7 cells. Cells were pretreated with 50 μg/mL of wild or cultivated T. tetragonoides ethanol extracts for 1 h, followed by stimulation with lipopolysaccharide (LPS, 1 μg/mL) for 24 h. Cell viability was assessed using the MTT assay. Data are expressed as mean±standard deviation (S.D.) from three independent experiments. Ctrl: untreated control group (no LPS); Wild: wild T. tetragonoides extract-treated group; Cultivated: cultivated T. tetragonoides extract-treated group.
4. 번행초의 일산화질소(NO) 생성 억제 효과
염증 반응에서 유도형 산화질소합성효소(inducible nitric oxide synthase, iNOS)에 의해 생성되는 일산화질소(NO)는 혈관 확장, 혈관 투과성 증가, 부종, 조직 손상 등 염증 반응의 주요 매개체로 작용한다(Lind M 등 2017; Anavi S & Tirosh O 2020). NO는 또한 병원체에 대한 방어 작용과 항종양 효과 등 생리적으로 유익한 기능을 수행하지만, 과도한 NO 생성은 만성 염증성 질환 및 면역계의 이상 반응을 유발할 수 있다(Okin D & Medzhitov R 2012; Low M 등 2024). 이러한 이유로 항염증 활성 평가 시 NO 생성 억제 효과는 핵심적인 지표로 활용되며, 천연물 유래 생리활성 소재의 탐색에서도 필수적으로 평가되고 있다(Bramorski Mohr ET 등 2025).
본 연구에서는 RAW 264.7 대식세포에 lipopolysaccharide(LPS, 1 μg/mL)를 처리하여 염증 반응을 유도한 뒤, 자연산 및 재배 번행초 추출물을 각각 50 μg/mL 농도로 24시간 처리하여 NO 생성 억제 효과를 평가하였다. 세포 배양 상등액에서의 nitrite 농도는 Griess 반응을 통해 정량하였으며, 그 결과는 Fig. 3에 제시하였다.
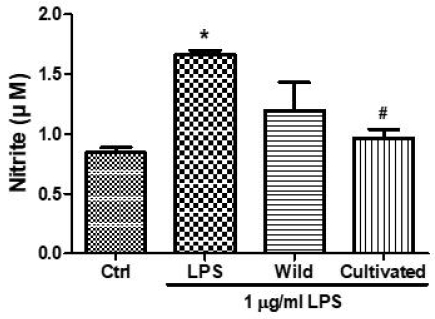
Inhibition of nitric oxide production by Tetragonia tetragonoides extracts in LPS-stimulated RAW 264.7 cells. Inhibitory effects of wild and cultivated Tetragonia tetragonoides (Tt) extracts on nitric oxide (NO) production in LPS-stimulated RAW 264.7 cells. Cells were treated with LPS (1 μg/mL) in the presence or absence of 50 μg/mL wild or cultivated T. tetragonoides extracts for 24 h. NO levels in the culture supernatant were quantified using the Griess assay. Data are expressed as the mean±standard deviation (S.D.) of three independent experiments. Ctrl: untreated control group (no LPS); Wild: wild T. tetragonoides extract-treated group; Cultivated: cultivated T. tetragonoides extract-treated group. *p<0.05 vs. control; #p<0.05 vs. LPS-treated group.
LPS 단독 처리군에서는 NO 생성이 유의하게 증가하였으며(p<0.05 vs. control), 재배 번행초 처리군은 LPS 처리군 대비 NO 생성이 유의하게 감소하였다(p<0.05 vs. LPS). 자연산 번행초 또한 억제 효과를 보였으나 통계적으로는 유의한 수준의 억제력을 나타내지 않았다. 특히 재배 번행초는 NO 생성량을 약 40% 이상 감소시키는 것으로 나타나, 자연산 번행초에 비해 상대적으로 높은 항염 활성을 보였다. 이와 같은 결과는 담수 환경에서 자란 번행초가 더 많은 항염증 관련 생리활성 물질을 함유하고 있을 가능성을 시사하며, 염증성 질환의 예방 및 조절을 위한 천연 기능성 소재로서의 활용 가능성을 보여준다.
5. 번행초의 TNF-α, IL-1β, IL-6 생성 억제 효과
활성화된 대식세포는 TNF-α, IL-1β, IL-6, IL-10 등의 전염증성 및 염증성 사이토카인을 분비하며, 이는 염증 반응의 주요 조절인자로 작용한다(Chen L 등 2018; Medzhitov R 등 2021). 특히 TNF-α와 IL-6는 면역 조절, 급성기 반응, 조혈 작용 등 다양한 생리적 기능을 가지며, 과도한 분비 시 조직 손상 및 만성 염증성 질환의 발생과 연관된다(Furman D 등 2019). TNF-α는 다른 면역세포의 활성화를 유도하고, 혈관내피세포에서의 세포접착 분자 발현을 통해 백혈구의 염증 부위 유입을 촉진하는 한편, 전신 반응으로 발열, 식욕 감소, C-반응성 단백질(CRP) 상승 등을 유도할 수 있다(Frasca D 등 2017).
본 연구에서는 RAW 264.7 대식세포에 LPS (1 μg/mL)를 처리하여 염증 반응을 유도한 후, 자연산 및 재배 번행초 추출물(50 μg/mL)을 처리하여 염증성 사이토카인의 생성 억제 효과를 평가하였다. 세포 배양 상등액을 수거하여 TNF-α, IL-1β, IL-6의 농도를 ELISA 분석을 통해 정량하였으며, 그 결과는 Fig. 4에 제시하였다.
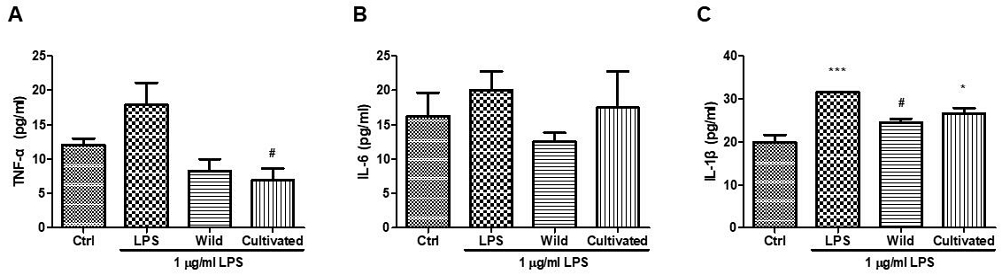
Suppression of pro-inflammatory cytokine production by Tetragonia tetragonoides extracts in LPS-stimulated RAW 264.7 cells. Effects of wild and cultivated Tetragonia tetragonoides (Tt) extracts on LPS-induced cytokine production in RAW 264.7 cells. Cells were treated with LPS (1 μg/mL) in the presence or absence of 50 μg/mL wild or cultivated T. tetragonoides extracts and incubated for 24 h. The concentrations of TNF-α, IL-6, and IL-1β in the culture supernatant were quantified using ELISA, as described in the Materials and Methods. Data are presented as the mean±standard deviation (S.D.) of three independent experiments. Ctrl: untreated control group (no LPS); Wild: wild T. tetragonoides extract-treated group; Cultivated: cultivated T. tetragonoides extract-treated group. *p<0.05, ***p<0.001 vs. control; #p<0.05 vs. LPS-treated group.
통계 분석 결과, 번행초 추출물 처리 시 IL-6의 생성이 LPS 단독 처리군 대비 다소 감소하는 경향을 보였으나 통계적으로 유의한 차이는 나타나지 않았다. 반면, TNF-α 및 IL-1β 생성에 있어서는 번행초 추출물의 유의한 억제 효과가 일부 확인되었다. 특히 자연산 번행초 처리군에서는 TNF-α(p<0.05)와 IL-1β(p<0.05)의 발현이 LPS 처리군에 비해 유의하게 감소하였으며, 이는 자연산 시료가 염증 반응의 주요 매개인자인 사이토카인의 생성을 효과적으로 억제할 수 있음을 시사한다. 재배 번행초 역시 TNF-α 생성을 유의하게 억제하였으나(p<0.05), 자연산 시료에 비해 억제 효과는 상대적으로 낮았다. 이러한 결과는 번행초 추출물이 염증성 사이토카인 생성을 조절할 수 있는 생리활성을 지니며, 자생 환경에 따른 생리활성 성분의 차이가 기능성에도 영향을 줄 수 있음을 의미한다.
6. 번행초의 COX-2 단백질 발현 저해 효과
염증 매개 인자인 NO와 PGE₂는 각각 iNOS(inducible nitric oxide synthase)와 COX-2(cyclooxygenase-2)의 활성에 의해 생성되며, 이들 효소의 발현 수준은 염증 반응의 주요 분자적 지표로 활용된다. 본 연구에서는 LPS(1 μg/mL)로 자극한 RAW 264.7 대식세포를 대상으로 번행초 추출물(50 μg/mL)의 COX-2 단백질 발현 억제 효과를 Western blot 분석을 통해 평가하였다.
Fig. 5에 나타난 바와 같이, LPS 단독 처리군에서는 COX-2 단백질 발현이 현저히 증가하였으나, 재배 번행초 추출물 처리군에서 β-actin 대비 COX-2 발현이 유의하게 감소하였다. Densitometric 정량 분석 결과, 재배 번행초는 약 46%의 COX-2 단백질 발현 억제 효과를 보이며 통계적으로 유의한 억제 효과를 나타냈다(p<0.05 vs. LPS).
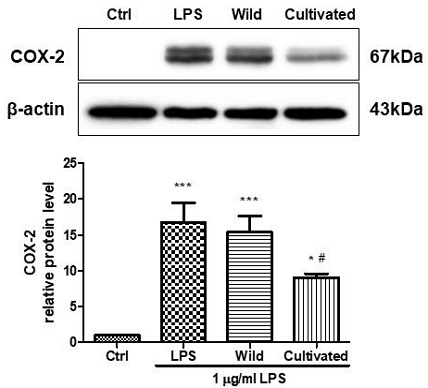
Inhibitory effects of Tetragonia tetragonoides extracts on COX-2 protein expression in LPS-stimulated RAW 264.7 cells.Inhibitory effects of wild and cultivated Tetragonia tetragonoides (Tt) extracts on COX-2 protein expression in LPS-stimulated RAW 264.7 cells. RAW 264.7 cells (6 × 105 cells/mL) were pre-incubated for 3 h and subsequently stimulated with lipopolysaccharide (LPS, 1 μg/mL) in the presence of 50 μg/mL wild or cultivated T. tetragonoides extracts for an additional 24 h. Protein levels of COX-2 were analyzed by Western blotting, and β-actin was used as an internal loading control. Band intensities were quantified by densitometric analysis using ImageJ software and normalized to β-actin. Data are presented as the mean±standard deviation (S. D.) from three independent experiments. Ctrl: untreated control group (no LPS); Wild: wild T. tetragonoides extract-treated group; Cultivated: cultivated T. tetragonoides extract-treated group. *p<0.05, ***p<0.001 vs. control; #p<0.05 vs. LPS-treated group.
이러한 결과는 번행초 추출물이 염증 반응에 중요한 역할을 하는 COX-2 단백질의 발현을 효과적으로 억제함으로써 염증 신호 전달 경로를 차단할 수 있음을 시사한다. 특히 재배 번행초가 자연산 번행초에 비해 다소 높은 COX-2 단백질 발현 억제 효과를 보였다는 점은, 생육 환경에 따라 식물의 항염증 활성이 달라질 수 있음을 시사한다. 유사하게, Laftouhi A 등(2023)은 Thymus vulgaris, Mentha pulegium, Rosmarinus officinalis와 같은 식용 및 약용 식물들이 고온 및 가뭄 스트레스 하에서 플라보노이드, 알칼로이드, 탄닌 등의 2차 대사산물 함량이 증가함을 보고하였다. 이는 환경 스트레스가 생리활성 물질의 축적을 유도할 수 있음을 뒷받침한다. 따라서 번행초 역시 생육 조건에 따라 항염 효과에 차이를 보일 수 있으며, 이러한 특성은 재배 기반의 기능성 원료 개발에 실질적인 활용 가능성을 제시한다.
요 약
본 연구에서는 자연산과 담수 재배 번행초(Tetragonia tetragonoides) 추출물의 항산화 및 항염증 활성을 비교·분석하였다. 자연산 번행초는 총 폴리페놀, 타닌, 플라보노이드 함량이 재배 번행초보다 유의하게 높았으며, ABTS 및 DPPH 라디칼 소거능 또한 뛰어나 우수한 항산화 활성을 보였다. 세포 기반 염증 억제 실험에서 재배 번행초는 COX-2 단백질 발현 및 NO 생성을 유의하게 억제하였고, 자연산 번행초는 TNF-α, IL-6, IL-1β 등 염증성 사이토카인 생성을 효과적으로 감소시켰다. 이러한 차이는 생육 환경에 따른 기능성 성분의 축적 차이에서 기인하는 것으로 사료되며, 번행초가 항산화 및 항염증 활성을 동시에 가지는 유망한 천연소재임을 시사한다. 특히 본 연구는 재배 환경에서도 일정 수준의 항염 효과가 유지됨을 입증함으로써, 번행초의 대량 재배 및 기능성 식품소재로서의 산업적 응용 가능성을 제시하였다는 점에서 의의가 있다.
References
-
Ahn BK, Min KC, Cho SH, Lee DG, Kim A, Lee SH (2021) Isolation of lactic acid bacteria with anti-MRSA bacteriocin activity and characterization of the bacteriocin product. Microbiol Biotechnol Lett 49(2): 131-137.
[https://doi.org/10.48022/mbl.2012.12008]

-
Ainsworth EA, Gillespie KM (2007) Estimation of total phenolic content and other oxidation substrates in plant tissues using Folin-Ciocalteu reagent. Nat Protoc 2(4): 875-877.
[https://doi.org/10.1038/nprot.2007.102]

-
Alam F, Mohammadin K, Shafique Z, Amjad ST, Asad MHHB (2022) Citrus flavonoids as potential therapeutic agents: A review. Phytother Res 36(4): 1417-1441.
[https://doi.org/10.1002/ptr.7261]

-
Anavi S, Tirosh O (2020) iNOS as a metabolic enzyme under stress conditions. Free Radic Biol Med 146: 16-35.
[https://doi.org/10.1016/j.freeradbiomed.2019.10.411]

-
Blois MS (1958) Antioxidant determinations by the use of a stable free radical. Nature 181(4617): 1199-1200.
[https://doi.org/10.1038/1811199a0]

-
Bramorski Mohr ET, Lubschinski TL, Oliveira JMD, Giarola Fragoso de Oliveira P, Garcia Mendes Borba B, Demarchi IG, Dalmarco EM (2025) Thiazolidines derivatives and their anti-inflammatory activity in LPS-induced RAW 264.7 macrophages: A systematic review and meta-analysis. Nat Prod Res 39(10): 2895-2911.
[https://doi.org/10.1080/14786419.2024.2394103]

-
Chen L, Deng H, Cui H, Fang J, Zuo Z, Deng J, Li Y, Wang X, Zhao L (2018) Inflammatory responses and inflammation-associated diseases in organs. Oncotarget 9(6): 7204-7218.
[https://doi.org/10.18632/oncotarget.23208]

- Choi HJ, Kang JS, Choi YW, Jeong YK, Joo WH (2008) Inhibitory Activity on the Diabetes Related Enzymes of Tetragonia tetragonioides. Korean J Biotechnol Bioeng 23(5): 419-424.
-
Choi HJ, Yee ST, Kwon GS, Joo WH (2015) Anti-inflammatory and Anti-tumor Effects of Tetragonia tetragonoides Extracts. Microbiol Biotechnol Lett 43(4): 391-395.
[https://doi.org/10.4014/mbl.1509.09001]

-
Choi GY, Kim HD, Bae JH (2017) Quality characteristics of sponge cakes occurred with percentages of persimmon leaves powder added. Culi Sci & Hos Res 13(4): 269-278.
[https://doi.org/10.20878/cshr.2007.13.4.022]

-
Chung HJ, Kim CJ, Choi YS (2015) Comparison of antioxidant and nitrite scavenging activities of different colored kiwis cultivated in Korea. J Korean Soc Food Cult 30(2): 220-226.
[https://doi.org/10.7318/kjfc/2015.30.2.220]

-
Dai J, Mumper RJ (2010) Plant phenolics: Extraction, analysis and their antioxidant and anticancer properties. Molecules 15(10): 7313-7352.
[https://doi.org/10.3390/molecules15107313]

-
Das UN (2021) Essential fatty acids and their metabolites in the pathobiology of inflammation and its resolution. Biomolecules 11(12): 1873.
[https://doi.org/10.3390/biom11121873]

-
Duval B, Shetty K (2001) The stimulation of phenolics and antioxidant activity in pea (Pisum sativam) elicited by genetically transformed anise root extract. J Food Biochem 25(5): 361-377.
[https://doi.org/10.1111/j.1745-4514.2001.tb00746.x]

-
Folin O, Denis W (1912) On phosphotungstic-phosphomolybdic compounds as color reagents. J Biol Chem 12(2): 239-243.
[https://doi.org/10.1016/s0021-9258(18)88697-5]

-
Frasca D, Blomberg BB, Paganelli R (2017) Aging, obesity, and inflammatory age-related diseases. Front Immunol 8: 1745.
[https://doi.org/10.3389/fimmu.2017.01745]

-
Fullerton JN, Gilroy DW (2016) Resolution of inflammation: a new therapeutic frontier. Nat Rev Drug Discov 15(8): 551-567.
[https://doi.org/10.1038/nrd.2016.39]

-
Furman D, Campisi J, Verdin E, Carrera-Bastos P, Targ S, Franceschi C, Ferrucci L, Gilroy DW, Fasano A, Miller GW, Miller AH, Mantovani A, Weyand CM, Barzilai N, Goronzy JJ, Rando TA, Effros RB, Lucia A, Kleinstreuer N, Slavich GM (2019) Chronic inflammation in the etiology of disease across the life span. Nat Med 25(12): 1822-1832.
[https://doi.org/10.1038/s41591-019-0675-0]

-
Gandhi GR, Jothi G, Mohana T, Vasconcelos ABS, Montalvão MM, Hariharan G, Sridharan G, Kumar PM, Gurgel RQ, Li HB, Zhang J, Gan RY (2021) Anti-inflammatory natural products as potential therapeutic agents of rheumatoid arthritis: A systematic review. Phytomedicine 93: 153766.
[https://doi.org/10.1016/j.phymed.2021.153766]

-
Gouda NA, Alshammari SO, Abourehab MAS, Alshammari QA, Elkamhawy A (2023) Therapeutic potential of natural products in inflammation: Underlying molecular mechanisms, clinical outcomes, technological advances, and future perspectives. Inflammopharmacology 31(6): 2857-2883.
[https://doi.org/10.1007/s10787-023-01366-y]

-
Hsueh TP, Lin WL, Dalley JW, Tsai TH (2021) The Pharmacological Effects and Pharmacokinetics of Active Compounds of Artemisia capillaris. Biomedicines 9(10): 1412.
[https://doi.org/10.3390/biomedicines9101412]

-
Ignat I, Volf I, Popa VI (2011) A critical review of methods for characterization of polyphenolic compounds in fruits and vegetables. Food Chem 126(4): 1821-1835.
[https://doi.org/10.1016/j.foodchem.2010.12.026]

-
Jo JB, Lee EH, Cho YJ (2016) Beauty Food Activities of lsolated Phenolic Compounds from Tetragonia tetragonioides. J Korean Soc Food Sci Nutr 45(3): 333-341.
[https://doi.org/10.3746/jkfn.2016.45.3.333]

-
Jomova K, Alomar SY, Valko R, Liska J, Nepovimova E, Kuca K, Valko M (2025) Flavonoids and their role in oxidative stress, inflammation, and human diseases. Chem Biol Interact 413: 111489.
[https://doi.org/10.1016/j.cbi.2025.111489]

-
Kim BG, Park NY, Lee SH (2016) Quality Characteristics and antioxidative activity of muffins added with coffee ground residue water extract and powder. J Korean Soc Food Sci Nutr 45(1): 76-83.
[https://doi.org/10.3746/jkfn.2016.45.1.076]

-
Kim DO, Jeong SW, Lee CY (2003) Antioxidant capacity of phenolic phytochemicals from various cultivars of plums. Food Chem 81(3): 321-326.
[https://doi.org/10.1016/s0308-8146(02)00423-5]

-
Kim JE, Joo SI, Seo JH, Lee SP (2009) Antioxidant and α-glucosidase inhibitory effect of tartary buckwheat extract obtained by the treatment of different solvents and enzymes. J Korean Soc Food Sci Nutr 38(8): 989-995.
[https://doi.org/10.3746/jkfn.2009.38.8.989]

-
Kim KH, Kim DM, Byun MW, Yun YS, Yook HS (2013) Antioxidant activity of panax ginseng flower-buds fermented with various microorganisms. J Korean Soc Food Sci Nutr 42(5): 663-669.
[https://doi.org/10.3746/jkfn.2013.42.5.663]

- Kong JH, Lee KY, Rho DH, Lee JC, An WG, Lee BK (2020) Antioxidant and anti-inflammatory activities of Tetragonia tetragonoides water extract. Herb Formula Sci 28(2): 137-145.
-
Ksouri R, Megdiche W, Debez A, Falleh H, Grignon C, Abdelly C (2007) Salinity effects on polyphenol content and antioxidant activities in leaves of the halophyte Cakile maritima. Plant Physiol Biochem 45(3-4): 244-249.
[https://doi.org/10.1016/j.plaphy.2007.02.001]

- Laftouhi A, Eloutassi N, Ech-Chihbi E, Rais Z, Abdellaoui A, Taleb A, Beniken M, Nafidi H-A, Salamatullah AM, Bourhia M, Taleb M (2023) The impact of environmental stress on the secondary metabolites and the chemical compositions of the essential oils from some medicinal plants used as food supplements. Sustainability 15(10): 7842.
- Lee ES, Park JW, Moon KH, Seo YW (2023) Antioxidant activity of native korean halophyte extracts and their anti-biofilm activity against Acinetobacter baumannii. J Life Sci 33(12): 1015-1024.
-
Lee MA, Choi HJ, Kang JS, Choi YW, Joo WH (2008) Antioxidant activities of the solvent extracts from Tetragonia tetragonioides. J Life Sci 18(2): 220-227.
[https://doi.org/10.5352/jls.2008.18.2.220]

-
Li H, Zeng Y, Zi J, Hu Y, Ma G, Wang X, Shan S, Cheng G, Xiong J (2024) Dietary flavonoids consumption and health: An umbrella review. Mol Nutr Food Res 68(12): e2300727.
[https://doi.org/10.1002/mnfr.202300727]

- Lind M, Hayes A, Caprnda M, Petrovic D, Rodrigo L, Kruzliak P, Zulli A (2017) Inducible nitric oxide synthase: Good or bad? Biomed Pharmacother 93: 370-375.
-
Low M, Suresh H, Zhou X, Bhuyan DJ, Alsherbiny MA, Khoo C, Münch G, Li CG (2024) The wide spectrum anti-inflammatory activity of andrographolide in comparison to NSAIDs: A promising therapeutic compound against the cytokine storm. PLoS One 19(7): e0299965.
[https://doi.org/10.1371/journal.pone.0299965]

-
Medzhitov R (2021) The spectrum of inflammatory responses. Science 374(6571): 1070-1075.
[https://doi.org/10.1126/science.abi5200]

-
Naczk M, Shahidi F (2006) Phenolics in cereals, fruits and vegetables: Occurrence, extraction and analysis. J Pharm Biomed Anal 41(5): 1523-1542.
[https://doi.org/10.1016/j.jpba.2006.09.034]

-
Okin D, Medzhitov R (2012) Evolution of inflammatory diseases. Curr Biol 22(17): R733-R740.
[https://doi.org/10.1016/j.cub.2012.07.029]

- Panche AN, Diwan AD, Chandra SR (2016) Flavonoids: An overview. J Nutr Sci 5: e47.
- Park GH, Lee SH, Kim HY, Jeong HS, Kim EY, Yun YW, Nam SY, Lee BJ (2011) Comparison in antioxidant effect of four citrus fruits. J Food Hyg Safety 26(4): 355-360.
- Park YK, Nam UH (2002) Studies on the Anti-oxidative effects of Tetragonia tetragonioides. Kor J Herbol 17(2): 191-202.
- Pietta PG (2000) Flavonoids as antioxidants. J Nat Prod 63(7): 1035-1042.
- Re R, Pellegrini N, Proteggente A, Pannala A, Yang M, Rice-Evans C (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radical Biol Med 26(9-10): 1231-1237.
-
Ryu JY, Park HJ, Lee SL, Koh SY, Lim HJ, Kim HA, Cho SK (2018) Quality characteristics of madeleine added with halla gold kiwifruit fermented by lactic acid bacteria. Food Sci Preserv 25(2): 205-211.
[https://doi.org/10.11002/kjfp.2018.25.2.205]

-
Sies H, Mailloux RJ, Jakob U (2024) Fundamentals of redox regulation in biology. Nat Rev Mol Cell Biol 25(9): 701-719.
[https://doi.org/10.1038/s41580-024-00730-2]

-
Woo KS, Song SB, Ko JY, Lee JS, Jung TW, Jeong HS (2015) Changes in antioxidant contents and activities of adzuki beans according to germination time. J Korean Soc Food Sci Nutr 44(5): 687-694.
[https://doi.org/10.3746/jkfn.2015.44.5.687]

-
Yoon JA (2020) Quality characteristics and antioxidant activity of aponge cake added with Tetragonia tetragonoides powder. J Korean Soc Food Sci Nutr 49(9): 953-960.
[https://doi.org/10.3746/jkfn.2020.49.9.953]

-
Zhishen J, Mengcheng T, Jianming W (1999) The determination of flavonoid contents in mulberry and their scavenging effects on superoxide radicals. Food Chem 64(4): 555-559.
[https://doi.org/10.1016/s0308-8146(98)00102-2]

