매실주의 에틸카바메이트 분석
Abstract
This study aimed to develop and validate an analytical method for ethyl carbamate (EC) in Maesilju. For accurate analysis of EC in Maesilju, an internal standard (d5-EC) and neutralization (pH=7) were performed. The limit of quantification (LOQ) was 3.65 ppb while the recovery rate ranged from 92.54% to 103.59%. Intra- and inter-day precision ranged from 0.87% to 1.99% and 2.67% to 5.64%, respectively. Maesilju samples comprised 10 homemade and five commercial ones. Samples contained EC at levels between 118.48 and 2,640.42 ppb. The average content of homemade Maesilju was higher than those of commercial ones. Based on manufacturers’ labeling of commercial samples and information on homemade samples, various factors such as ingredients and soaking time of Maesil affected EC level in Maesilju. EC contents showed a positive correlation with age of Maesilju.
Keywords:
Ethyl carbamate, Maesilju, recovery, precision서 론
식품을 제조ㆍ가공하는 과정에서 생성 및 잔류되는 유해물질이 미량일지라도 음식물을 통해 일생 동안 섭취되기 때문에 안전성에 대한 관심이 높아지고 있다. 에틸카바메이트(ethyl carbamate)는 발효식품 또는 알코올 음료의 저장 및 숙성 과정에서 자연적으로 생성되는 동물성 발암물질이다(KFDA 2010). 알코올 음료 중 포도주, 청주, 위스키 등에서 에틸카바메이트가 높게 검출되었는데, 특히 핵과류(stone fruits: 살구, 매실, 체리 등)로 제조된 브랜디와 증류주에서 매우 높게 검출되었다(Weber & Sharypov 2009). 우리나라의 대형 유통매장에서 95개 주류(탁주, 청주, 약주, 과실주, 소주, 리큐르, 브랜디)를 수집하여 에틸카바메이트 함량을 분석한 결과, 매실주에서 에틸카바메이트 평균 농도가 79.18 ppb로 가장 높았다(Kim et al 2013a).
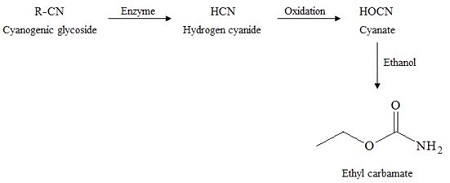
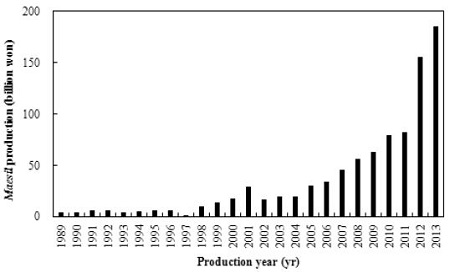
핵과류의 씨 부분에 주로 존재하는 시안배당체가 효소적 가수분해 및 산화에 의해 시안산염(cyanate)으로 전환되는데(Fig. 1), 이 물질이 에탄올과 반응하여 에틸카바메이트가 생성된다고 알려져 있다(Zimmerli & Schlatter 1991). 우리나라의 매실 재배면적은 1982년 156 ha, 1992년 880 ha, 2007년 4,418 ha로 지속적으로 높아지고 있으며(Chung KH 2013), 생산금액도 1989년 45억 원에서 꾸준히 증가하여 2013년에는 1,852억 원으로 크게 증대되었다(Fig. 2) (Statistics Korea 2014). 하지만 매실은 저장성이 좋지 않기 때문에 6월경에 수확된 후 매실주(Maesilju), 소금절임(매실장아찌, 우메보시), 진액(엑기스), 설탕절임 등으로 가공된다(Chung KH 2013). 2011년 국민영양 통계자료에서 섭취자 기준의 매실주 섭취량은 1인 1일 167.41 g이었다(KHIDI 2013). 식약처의 ‘주류 소비 및 섭취 실태조사 결과’에 따르면, 전국 16개 시ㆍ도에 거주하는 만 15세 이상 남녀 1,000명이 1년간 가장 많이 마신 술을 매실주라고 응답한 비율은 21.0%으로 나타났다(KFDA 2011).
캐나다, 프랑스, 독일 등은 알코올 음료를 포도주, 증류주, 과일브랜디 등으로 나누어 에틸카바메이트의 최대 허용기준치를 각각 설정하여 관리하고 있다. 하지만 우리나라는 알코올 함량이 15% 미만인 포도주에 에틸카바메이트의 최대허용치가 30 ppb로 설정되어 있지만, 다른 알코올 음료에 대한 기준함량은 설정되어 있지 않다. 매실주는 제조할 때 사용되는 알코올의 농도, 매실과 씨의 분리 시기, 숙성 기간 등에 의해 에틸카바메이트의 생성이 달라진다고 알려져 있다(Kim et al 2013b; Hwang et al 2009). 특히, 가정에서 직접 매실주를 담그는 경우에는 매실과 알코올의 비율, 발효조건, 침지기간, 숙성기간 등이 다양하기 때문에 에틸카바메이트 생성량이 달라질 가능성이 높다. 또한, 시판되고 있는 상업용 매실주는 표백과 살균효과를 위해 무수아황산 등이 첨가되어 제조되기 때문에, 에틸카바메이트 생성에 미치는 영향을 배제할 수 없다.
따라서 본 연구에서는 에틸카바메이트의 분석 효율을 높이기 위해 내부표준물질 별 회수율을 비교하여 분석법을 개발하고, 상업적으로 제조된 매실주와 가정에서 직접 제조된 매실주의 에틸카바메이트 함량을 분석하여 비교하였다.
재료 및 방법
1. 시약 및 재료
디클로로메탄(dichloromethane)은 J.T.Baker(Center Valley, PA, USA)의 HPLC급을 구입하였고, 에틸카바메이트, 부틸카바메이트, 수산화나트륨은 Sigma-Aldrich(St. Louis, MO, USA)에서, d5-에틸카바메이트는 C/D/N Isotopes(Pointe-Claire, Quebec, Canada)에서 구입하였다. 염화나트륨은 SAMCHUN CHE-MICAL(Pyoungtaek, Gyeonggi-do, Korea)에서 구입하였으며, 정제컬럼(Chem Elut, 50 mL)은 Agilent Technologies(Milwaukee, WI, USA)에서 구입하였다. 각 가정에서 담근 매실주는 경기도, 경상도, 전라도, 충정도 지역에서 총 10개 시료가 수집되었다. 시중에서 판매되고 있는 상업용 매실주 5개는 마트에서 구입되었다.
2. 실험 방법
표준물질인 에틸카바메이트와 내부표준물질 d5-에틸카바메이트를 각각 0.1 g씩 칭량하여 아세톤에 용해시켜 1,000 µg/ mL 농도로 제조한 후, 다시 아세톤으로 희석하여 10 µg/mL의 표준용액과 내부표준용액을 만들어 검량선 작성에 사용하였다. 내부표준용액에 증류수를 첨가하여 400 ng/mL 농도의 내부표준첨가용액을 제조하여 시료 전처리에 사용하였다(KFDA 2008).
분석법의 정확성을 높이기 위해 2가지 내부표준물질을 사용하여 시료를 전처리하였다. 식품의약품안전처(KFDA 2008)에서 에틸카바메이트 시험법에 사용된 부틸카바메이트(butyl carbamate)와 에틸카바메이트의 에틸기 수소 5개가 중수소(deuterium)로 치환된 d5-에틸카바메이트(d5-ethyl carba mate)가 내부표준물질로 각각 이용되었다(Table 1). 회수율(recovery)을 측정하기 위해 매실주의 주 원료인 소주를 사용하였으며, 소주의 에틸카바메이트의 함량을 측정해 그 양을 제외한 후 회수율이 계산되었다. 소주에 첨가한 부틸카바메이트와 에틸카바메이트의 양은 각각 500 ng이었으며, 각 실험은 3회 반복하여 평균과 상대표준편차(relative standard deviation, RSD)를 산출하였다.
에틸카바메이트의 추출방법은 AOAC 방법(AOAC 2000)과 식품의약품안전처의 고시방법(KFDA 2008)에 근거하였다. 1 N 수산화나트륨 용액을 소량씩 첨가하면서 pH meter(3200P, Agilent Technologies, Shanghai, China)를 이용하여 pH를 7∼8정도로 중화시켰다. 중화된 매실주 10 g을 비커에 칭량한 후 내부표준물질 100 ng(250 µL of 400 ng/mL)과 증류수 40 g을 첨가하였다. 혼합액에 염화나트륨 5 g을 넣고 용해시킨 후 고체상 컬럼인 Chem Elut에 옮겼다. 증류수 10 mL로 비커를 헹군 후 Chem Elut으로 옮겨 4분간 정치하여 극성화합물을 흡착시켰다. 디클로로메탄 80 mL로 에틸카바메이트를 2회 용출시킨 후, 용출액을 20℃ water bath에서 2 mL까지 감압농축(SB-1200, EYELA, Shanghai, China)하였다. 농축액을 v-vial로 옮기고 37℃로 설정된 질소농축기(MG-2200, EYELA, Tokyo, Japan)를 이용하여 1 mL로 정확하게 농축하였다. 기체크로마토그래프/질량분석기로 에틸카바메이트를 정성 및 정량 분석하였다. 모든 시료는 3회 반복실험한 후 평균과 상대표준편차를 산출하였다.
소주 10 g에 표준물질 50, 500, 3,000 ng을 첨가하여 시료 전처리와 동일한 방법으로 에틸카바메이트를 분석하였다. 동일한 날에 3가지 농도를 각각 5반복하거나(intra-day), 서로 다른 날짜에 5일 동안 매일 1회씩 반복하여(inter-day) 회수율과 상대표준편차를 %로 산출하였다. 검출한계(limit of detection, LOD)와 정량한계(limit of quantification, LOQ)는 반응의 표준편차와 검량선의 기울기에 근거하여 3.3×σ/S (σ, 반응의 표준편차; S, 검량선의 기울기)와 10×σ/S로 계산하였다.
내부표준용액에 디클로로메탄을 가해 내부표준물질 농도는 100 ng/mL로 하고, 표준물질은 8가지 농도(50, 100, 200, 500, 1,000, 1,500, 2,000, 3,000 ng/mL)로 검량선을 작성하였다. 내부표준물질과 표준물질의 농도비를 X축으로 하고, 면적비를 Y축으로 작성된 검량곡선을 이용하여 에틸카바메이트를 정량하였다.
에틸카바메이트의 정성 및 정량분석을 위해 사용한 기기는 GC/MSD(7820A Gas Chromatograph-5977E Mass Spectrometer, Agilent Technologies, Shanghai, China)였다. 컬럼은 DB-WAX(Agilent Technologies, 30 m×0.25 mm i.d., 0.25 µm film thickness)를 사용하였고, 운반기체는 99.9999%의 헬륨가스를 1 mL/min의 유속으로 하였다. 오븐온도는 60℃에서 90 ℃까지 분당 10℃로 승온하고, 130℃까지 분당 2℃로 승온 후 5분간 유지한 후 220℃까지 분당 20℃로 승온하고, 3분간 유지하여 물질을 분리시켰다. 시료 주입방법은 비분할법(splitless)을 사용하였으며, 주입구와 transfer line 및 ion source 온도는 각각 210, 240, 230℃였다. 시료는 70 eV의 에너지에 의해 전자 충격 이온화법(electron impact ionization)으로 이온화되었으며, 150℃의 사중극자형(quadrupole) 질량분석관을 통해 이온이 분리되었다. 선택 이온질량은 SIM(selected ion monitoring) 방법으로 m/z 62, 74, 89는 에틸카바메이트와 부틸카바메이트의 정량에, m/z 64, 76, 94는 d5-에틸카바메이트의 정량에 사용되었다. 선택성과 감도가 높은 토막이온(fragments)인 m/z 62와 m/z 74의 비율을 이용하여 에틸카바메이트를 정성 분석하였다.
결과 및 고찰
1. 분석법의 유효성 검증(Method Validation)
에틸카바메이트 분석법의 정확성을 높이기 위해 2가지 내부표준물질(Table 1)을 사용하여 회수율을 비교하였다. 에틸카바메이트의 내부표준물질로 프로필카바메이트, 부틸카바메이트, d5-에틸카바메이트가 사용되어 왔다(Kim et al 2010; Lim et al 2011; Huang et al 2013). AOAC 방법(AOAC 2000)에서 사용된 프로필카바메이트(propyl carbamate)는 생산이 중단되었기 때문에 제외되었다. 식품의약품안전청의 고시(KFDA 2008)에서 사용된 부틸카바메이트(butyl carbamate)와 에틸카바메이트의 에틸기 수소 5개가 중수소(deuterium)로 치환된 d5-에틸카바메이트로 전처리하여 회수율을 비교하였다. 소주 시료에서 에틸카바메이트 18.93 ppb가 검출되었기 때문에, 회수율은 시료에 내재되어 있는 에틸카바메이트 함량을 제외한 양으로 계산되었다. 부틸카바메이트와 d5-에틸카바메이트의 회수율은 77.47%와 101.00%이었다(Table 2). 이 결과는 부틸카바메이트의 탄소 수가 2개 더 많아, 극성, 끓는점 등의 화학적 특징이 에틸카바메이트와 차이가 있는 반면에, d5-에틸카바메이트는 에틸기의 수소 5개만 중수소로 치환되어 에틸카바메이트와 물리화학적 성질이 유사하였기 때문으로 생각된다(Table 1). 따라서 d5-에틸카바메이트가 에틸카바메이트 분석의 내부표준물질로 선정되었다.
시료의 전처리 과정에서 매실주를 중화시킨 이유는 알코올 음료의 산도를 중성으로 만들었을 때 반복실험의 표준편차가 크게 낮아지면서 재현성(reproducibility)이 향상되었기 때문이다(Lachenmeier et al 2006). 증류수를 첨가하여 알코올을 희석시킨 것은 알코올 농도가 20% 이상이면 에틸카바메이트의 회수율이 120% 이상으로 크게 높아진다고 보고되었기 때문이다(Xia et al 2014). 정제단계(clean-up)에서는 liquid-liquid extraction보다 solid-phase extraction(SPE)를 이용하는 것이 전처리 시간을 단축시키고, 간섭물질(interfering compounds)의 제거에 효율적이라고 보고되었다(Xia et al 2014). SPE 컬럼의 충전물이 primary-secondary amine 또는 florisil인 경우에는 유기산과 같은 저분자 화합물이 잔존한다는 제한이 있다. 따라서 본 연구에서는 유기산 함량이 높은 매실주의 특성을 고려하여 흡착제(sorbent)가 규조토(diatomite)인 Chem Elut으로 저분자 화합물을 제거하였다.
매실주의 주재료인 소주에 3가지 농도의 에틸카바메이트(50, 500, 3,000 ng)를 첨가하여 분석한 결과, 92.54∼103.59%의 회수율을 나타내었고, 상대표준편차는 0.87∼5.64%로 각 반복 횟수 간 편차가 크지 않음을 확인하였다(Table 3). CODEX에서 제시한 정량분석에 적합한 회수율 범위는 70∼120%, 상대표준편차 범위는 10∼20% 이내이어야 한다. 본 연구의 회수율과 상대표준편차는 CODEX의 분석기준에 부합되었기 때문에 에틸카바메이트 분석법으로 적합하였다. 분석법의 검출한계는 1.20 ppb이고, 정량한계는 3.65 ppb이었다.
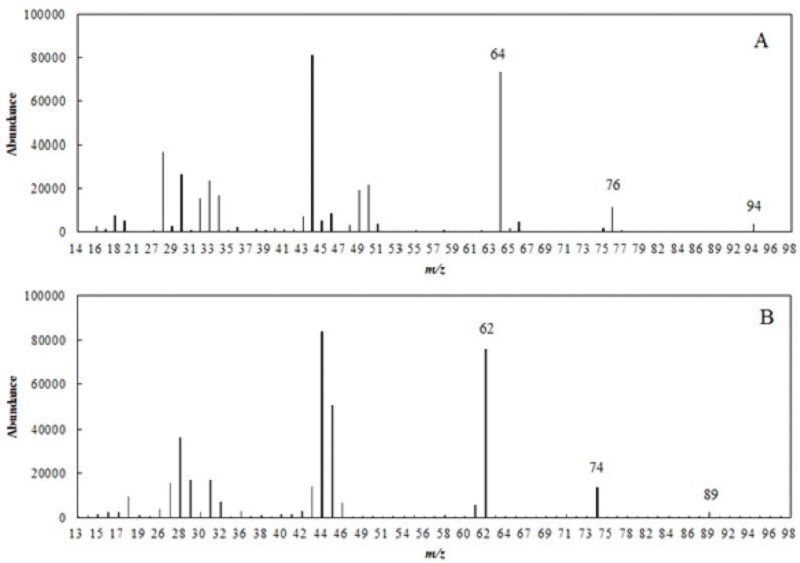
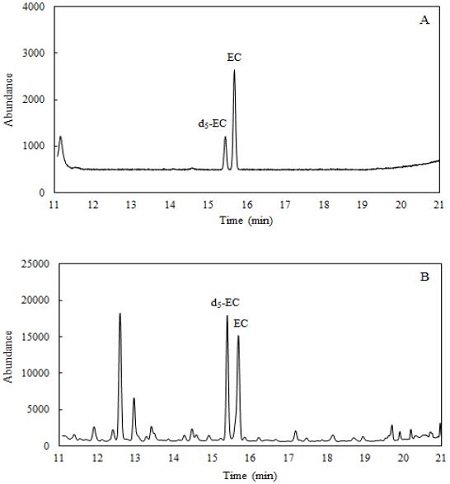
8가지 농도의 에틸카바메이트와 d5-에틸카바메이트의 농도비와 면적비를 통해 검량선을 작성한 결과, 상관계수(R2)의 값이 0.9992로 직선성(linearity)을 나타내었다. 이는 에틸카바메이트와 d5-에틸카바메이트의 회수율과 반복성이 일정하여 농도의존적으로 농도비가 증가함에 따라 면적비 또한 일정하게 증가하였음을 보여준다. 에틸카바메이트와 d5-에틸카바메이트의 질량스펙트럼을 비교한 결과, 분자이온(m/z 89과m/z 94), 메틸기가 제거된 토막이온(m/z 74와 m/z 76), 에틸기가 제거된 후 McLafferty 자리옮김 반응산물(m/z 62와 64)이 공통적으로 나타났다(Fig. 3). 그 중 m/z 62와 64가 주봉우리로 나타나 높은 감도(sensitivity)와 선별성(selectivity)을 고려하여 정량에 이용되었다. 선택이온 모드(SIM mode)에서 감도를 높이기 위해 6개 토막이온(m/z 62, 64, 74, 76, 89, 94)이 수집되었다. 내부표준물질인 d5-에틸카바메이트와 분석물질인 에틸카바메이트는 각각 15.44분, 15.68분에서 검출되어 크로마토그램에서 완벽하게 분리되었다(Fig. 4).
2. 매실주의 에틸카바메이트 함량
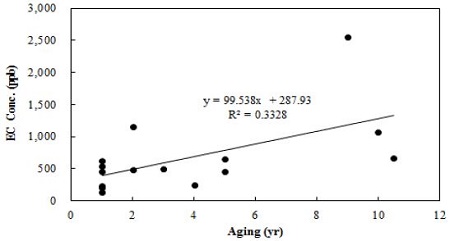
에틸카바메이트가 모든 매실주 시료에서 검출되었고(Fig. 5), 시료 별 3회 반복의 상대표준편차는 20%를 넘지 않았다. 분석된 매실주의 에틸카바메이트 함량 범위는 최소 118.48 ppb부터 최대 2,640.42 ppb이었다. 이는 Kim et al(2013b)의 연구에서 보고된 대형 유통매장에서 구매한 매실주의 에틸카바메이트 평균함량인 79.18 ppb보다 높은 수치이다.
매실주, 와인 등의 알코올 음료를 제조할 때 갈변을 억제하기 위해 무수아황산을 첨가하는데, Hashiguchi et al(2010)은 매실주에 메타중아황산칼륨을 첨가했을 때 hydrogen cyanide가 cyanate로 산화되는 과정을 억제하여 에틸카바메이트 생성이 감소된다고 보고하였다. C1(197.99 ppb) 시료도 갈변, 착색 등을 억제하기 위해 무수아황산(anhydrous sulfur dioxide)이 첨가되었는데(Table 4), 이 화합물은 산화되는 과정을 억제함으로써 에틸카바메이트 전구체인 cyanate의 생성을 지연시킬 수 있다. 따라서 상업용 시료의 에틸카바메이트 함량과 원재료와의 연관성을 살펴보기 위해, 제품 용기에 표기된 원재료 및 함량을 Table 4에 제시하였다. 상업용 매실주 시료에서 가장 낮은 농도는 C1(197.99 ppb)시료였다. 이 시료는 매실 원액이 50%로 다른 시료의 매실 원액이 61∼100%인 것에 비해 상대적으로 낮았기 때문에, 매실원액에 존재하였던 에틸카바메이트가 더 희석된 것으로 생각된다. C3 (233.15 ppb) 시료에서는 C1 시료와 마찬가지로 무수아황산이 0.035% 이하 첨가되었으며, 매실주 원액은 62%로 약간 더 높았으나, 알코올 도수가 10%로 상업용 매실주 중에서 가장 낮아 에틸카바메이트의 생성이 낮았던 것으로 생각된다. 반면에, C4(1,076.82 ppb) 시료는 매실주 원액의 비율이 비교적 낮았지만 10년의 숙성기간 동안 cyanate와 알코올이 반응하여 가장 높은 농도의 에틸카바메이트가 관찰된 것으로 사료 된다. 다른 시료와 달리 제품에 매실이 담겨 판매되는 C2(461.05 ppb) 시료는 진열되어 판매되는 시간까지 cyanate와 알코올이 반응을 할 수 있기 때문에 에틸카바메이트의 농도가 높을 것으로 예상하였다. 실제로 C2 시료는 무수아황산과 알코올 함량이 같은 C1 시료(197.99 ppb)보다 에틸카바메이트가 2.3배 높게 검출되었다. 이러한 결과는 매실 원액의 함량, 첨가물, 침지기간이 에틸카바메이트 생성에 영향을 준다는 것을 보여준다.
집에서 담근 매실주의 에틸카바메이트 함량은 129.19∼2,546.67 ppb로 상업용 매실주의 함량(153.91∼1,193.36 ppb)보다 2배 이상 넓게 분포되었다. Kim et al(2013b)은 매실주를 제조하면서 숙성기간에 따른 에틸카바메이트 농도를 비교한 결과, 알코올 농도 및 매실과 소주의 담금비에 따라 제조 후 15∼90일까지 적게는 15.60 ppb부터 87.40 ppb까지 최대 5배까지 높아졌다고 보고하였다. 본 연구에서 매실이 술에 8년간 침지되었던 것으로 확인된 매실주의 에틸카바메이트 함량은 2,546.67 ppb로 가장 높았다. 반면에, 10년 동안 숙성된 시료의 에틸카바메이트 함량은 666.56 ppb로 오히려 낮았다. 이 시료는 10년 동안 숙성되었지만 일정 기간의 침지 이후에는 매실이 알코올에서 분리되어 저장되었기 때문에, cyanate의 용출이 낮았을 것으로 생각된다. 한편, 1년 동안 숙성시킨 시료 중 477.71 ppb이 검출된 시료는 10년 동안 숙성시킨 시료의 에틸카바메이트의 3/4에 해당되는 양으로 숙성시킨 시간에 비해 비교적 많은 양의 에틸카바메이트가 검출되었다. 일반적으로 3개월 후에 매실을 분리하는 것과 달리, 이 시료는 1년 동안 매실을 분리하지 않고 숙성된 시료였다. 전체적으로 매실주의 숙성 기간은 에틸카바메이트 함량과 양의 상관관계(R2=0.3328)를 나타냈다(Fig. 5). 에틸카바메이트 생성은 매실의 분리 시기 등 다양한 요인의 영향을 받기 때문에 본 실험에서는 숙성기간이 강한 요인으로 작용하지는 않은 것으로 생각된다.
Hwang et al(2009)은 16%와 30% 알코올 농도의 매실주를 45일에서 180일까지 저장기간이 길어질수록 에틸카바메이트 함량이 증가하였다고 보고하였다. 매실의 침출 기간이 길어질수록, 침출 온도가 높을수록 에틸카바메이트 함량도 증가되었다. 매실을 침출할 때 자외선의 양이 많으면 암실이나 냉장고에 보관한 것보다 에틸카바메이트 함량이 높아졌다. 90일 동안 설탕만으로 숙성한 매실엑기스에서는 에틸카바메이트가 검출되지 않은 반면에, 알코올과 숙성하였을 때는 60일부터 에틸카바메이트가 검출되었다(Kim et al 2013b). 매실 과육만으로 매실주를 제조하였을 때는 에틸카바메이트가 생성되지 않은 반면에, 매실씨로 제조된 경우에는 에틸카바메이트가 생성되었다(Hwang et al 2009). 이러한 연구결과를 종합해 보면, 본 연구에서 수집된 매실주는 각기 다른 방법으로 제조되었기 때문에 에틸카바메이트 농도 범위가 큰 것으로 사료된다.
지금까지 발효식품과 알코올 음료에서 에틸카바메이트 생성을 낮추기 위한 다양한 방법이 시도되어 왔다. 아르기닌을 분해하여 요소 또는 시트룰린을 생성하는 효소인 arginase의 gene을 포도주 발효 효모에서 제거하거나, acid urease를 처리하여 요소를 분해하거나, 증류방법을 개선하는 방법 등이 개발되어 적용되었다(Fujinawa et al 1992; Liu et al 1996; KFDA 2011). 미국 FDA와 캘리포니아양조협회는 포도주의 에틸카바메이트 함량을 낮추기 위해 ‘Ethyl Carbamate Preventative Action Manual’을 작성하여 포도주 제조업자들에게 보급하여 에틸카바메이트 생성을 저감화 할 것을 권고하고 있다(Butzke & Bisson 1997). 우리나라에서는 식품의약품안전청이 ‘주류 중 에틸카바메이트(EC) 저감화 매뉴얼’을 배포하여(KFDA 2011) 매실주를 제조할 때 에탄올 함량을 50% 이하로 낮추고, 매실의 침출기간이 길어질수록 매실 씨앗에 포함된 시안화물의 용출이 높아질 수 있으므로 매실의 침출기간을 100일 이내로 할 것을 권고하고 있다. 또한, 핵과류의 침출온도를 낮게 유지하고, 침출기간을 줄여야 하며, 침출액을 저장할 때 상온 이하의 햇빛이 들지 않는 장소에서 숙성시켜 에틸카바메이트 생성량을 최대한 낮출 것을 권고하고 있다.
요 약
에틸카바메이트의 내부표준물질로 d5-에틸카바메이트가 선정되었다. 에틸카바메이트의 일내(intra-day), 일간(inter-day) 정밀도를 측정한 결과, 회수율은 92.54∼103.59%, 상대표준편차는 0.87∼5.64%로 CODEX 기준에 부합하였다. 검출한계와 정량한계는 각각 1.20 ppb와 3.65 ppb였으며, 검량선은 직선성(R2=0.9992)을 나타내었다. 상업용 매실주보다는 가정에서 담근 매실주에서 검출된 에틸카바메이트의 함량이 비교적 높게 나타났다. 또한, 매실주의 숙성기간은 에틸카바메이트 농도와 양의 상관관계를 보였다. 즉, 매실의 침지기간과 매실이 분리된 후 숙성기간이 매실주의 에틸카바메이트 함량에 영향을 미친다는 것을 나타낸다.
REFERENCES
- AOAC, (2000), Official Methods of Analysis, 17th ed, Association of Official Analytical Chemists, Washington DC, p14-15.
- Chung, KH., (2013), Plum, maesil, Rural Development Administration (RDA), Korea, p144-147.
- Butzke, CE., Bisson, LF., (1997), Ethyl Carbamate Preventative Action Manual, UCdavis Cooperative Extension.
- Fujinawa, S., Kodama, S., Todoroki, H., Suzuki, T., (1992), Trace urea determination in red wine and its degradation rate by acid urease, Am J Enol Vitic, 43(4), p362-366.
-
Huang, Z., Pan, XD., Wu, PG., Chen, Q., Han, JL., Shen, XH., (2013), Validation (in-house and collaborator) of the quantification method for ethyl carbamate in alcoholic beverages and soy sauce by GC-MS, Food Chem, 141, p4161-4165.
[https://doi.org/10.1016/j.foodchem.2013.06.128]

-
Hashiguchi, T., Horii, S., Izu, H., Sudo, S., (2010), The concentration of ethyl carbamate in commercial ume (Prunus mume) liqueur products and a method of reducing it, Biosci Biotechnol Biochem, 74(10), p2060-2095.
[https://doi.org/10.1271/bbb.100364]

- Hwang, LH., Kim, AK., Park, KA., Kim, JY., Hwang, IS., Chae, YZ., (2009), The effect of raw material, alcohol content, and transresveratrol on the formation of ethyl carbamate in plum wine, J Fd Hyg Safety, 24(3), p194-199.
- KFDA, (2008), Official Amendment Notice no. 2008-25, Korea Food and Drug Administration.
- KFDA, (2010), Ethyl carbamate: Risk profile, Korea Food and Drug Administration, p1-76.
- KFDA, (2011), Reduction manual of ethyl carbamate in alcohol beverage, Korea Food and Drug Administration, p13-46.
- KFDA, (2011), Alcohol consumption and intake survey, Available from http://www.mfds.go.kr/index.do?mid=675&seq=16616&cmd=v. Accessed Dec 13, 2014.
- KHIDI, (2013), National Food & Nutrition Statistics 2011, Korea Health Industry Development Institute.
-
Kim, DH., Jang, HS., Choi, GI., Kim, HJ., Kim, HJ., Kim, HL., Kim, KS., (2013a), Determination of residue levels of ethyl carbamate in alcoholic beverages by gas chromatography/tandem mass spectrometry, J Fd Hyg Safety, 28(1), p63-68.
[https://doi.org/10.13103/JFHS.2013.28.1.063]

-
Kim, NY., Eom, MN., Do, YS., Kim, JB., Kang, SH., Yoon, MH., Lee, JB., (2013b), Determination of ethyl carbamate in maesil wine by alcohol content and ratio of maesil (Prunus mume) during ripening period, Korean J Food Preserv, 20(3), p429-434.
[https://doi.org/10.11002/kjfp.2013.20.3.429]

-
Kim, YKL., Koh, E., Chung, HJ., Kwon, H., (2010), Determination of ethyl carbamate in some fermented Korean foods and beverages, Food Addit Contam, 17(6), p469-475.
[https://doi.org/10.1080/02652030050034055]

-
Lachenmeier, DW., Nerlich, U., Kuballa, T., (2006), Automated determination of ethyl carbamate in stone-fruit spirits using headspace solid-phase microextraction and gas chromato- graphy-tandem mass spectrometry, J Chromatogr A, 1108, p116-120.
[https://doi.org/10.1016/j.chroma.2005.12.086]

-
Lim, SH., Lee, KG., (2011), Development and validation of analy- tical methods for ethyl carbamate in various fermented foods, FoodChem, 126, p1373-1379.
[https://doi.org/10.1016/j.foodchem.2010.11.110]

-
Liu, SQ., Pritchard, GG., Hardman, MJ., Pilone, GJ., (1996), Arginine catabolism in wine lactic acid bacteria: is it via the arginine deiminase pathway or the arginase-urease pathway, J Appl Bacteriol, 81(5), p486-492.
[https://doi.org/10.1111/j.1365-2672.1996.tb03537.x]

- Statistics Korea, (2014), Agriculture and forestry production index (maesil), Available from http://kosis.kr/statHtml/statHtml.do?orgId=114&tblId=DT_114_2014_S0002&conn_path=I3 Accessed January 27, 2015.
-
Weber, JV., Sharypov, VI., (2009), Ethyl carbamate in foods and beverages: A review, Environ Chem Lett, 7(3), p233-247.
[https://doi.org/10.1007/s10311-008-0168-8]

-
Xia, Q., Yuan, H., Wu, C., Zheng, J., Zhang, S., Shen, C., Yi, B., Zhou, R., (2014), An improved and validated sample cleanup method for analysis of ethyl carbamate in Chinese liquor, J Food Sci, 79, p1854-1860.
[https://doi.org/10.1111/1750-3841.12567]

-
Zimmerli, B., Schlatter, J., (1991), Ethyl carbamate: Analytical methodology, occurrence, formation, biological activity and risk assessment, Mutat Res Genet Toxicol Environ Mutagen, 259, p325-350.
[https://doi.org/10.1016/0165-1218(91)90126-7]