원료에 따른 살균 막걸리의 품질 특성
Abstract
This study was investigated to determine the physicochemical changes in makgeolli in response to heat treatment and their effects on the taste and flavor of makgeolli. The main materials used in makgeolli production were rice and wheat flour. The components that affected the taste of makgeolli (organic acids, free sugars and free nitrogen compounds) were compared. There were no differences in organic acids among makgeollies by heat treatment, although there was significant difference in free sugar content. Alanine, arginine, glutamic acid, leucine, lysine, phenylalanine, proline, tyrosine, valine, and methionine were the main free nitrogen compounds in all makgeollies, and there were no changes in content in response to heat treatment. However, the minor free nitrogen compounds such as ammonia, urea, phenylalanine were confirmed to cause off-flavor get the effect of heat treatment. Therefore, the heat treatment did not affect the taste of makgeolli; however, flavor components of makgeolli were changed by heat treatment. It was confirmed that there is a difference due to the complex change of various compounds rather than the any compound in heat treatment.
Keywords:
Makgeolli, rice, wheat, sterilized, heat treatment서 론
막걸리는 누룩과 물을 혼합한 것에 고두밥을 넣어 발효시킨 다음, 맑은 술을 떠내지 않고 그대로 막 걸러서 만든 혼탁한 술이기 때문에 ‘탁주’라고도 한다(Jeong JW 등 2006). 막걸리에 대한 역사는 삼국유사(三國遺事) 가락국기(駕洛國記)에 수로왕에게 제사를 지내기 위해 요례(醪醴)를 빚었다는 기록이 있는데, 여기에 탁주를 뜻하는 요(醪)자가 들어 있는 것으로 보아 삼국시대에 이미 막걸리를 빚기 시작한 것으로 추측된다(Min JY 등 2015).
최근 저도주를 선호하는 추세에 따라 편하게 즐길 수 있는 막걸리의 2010년 출고량은 국세청에 따르면 2009년보다 58.1% 증가하였으며, 전체 주류의 12%를 차지함으로써 1995년 이후 10%대 점유율을 처음으로 회복하였다. 또한, 삼성경제연구소가 지정한 ‘2009년 10대 히트상품’에 막걸리가 1위로 선정되었으며, 그 인기는 국내뿐 아니라 해외에서도 급증하고 있다(Kim IS 등 2012).
막걸리는 누룩에 있는 효소에 의해 전분질 원료가 포도당으로 되는 당화과정과 포도당이 효모에 의해 알코올로 되는 발효과정이 동시에 일어나는 병행 복발효로 제조된다. 발효 과정 중 원료의 단백질은 단백질 분해효소에 의해 분해되어 아미노산이나 펩타이드를 생성하고, 미생물에 의해 생성되는 유기산의 종류에 따라서도 품질이 달라질 수 있다(Kim 등 2017). 한편, 막걸리는 비열처리 막걸리인 생 막걸리와 열처리 막걸리인 살균 막걸리로 나뉜다. 생 막걸리는 효모와 유산균이 생균 상태로 함유되어 있어 유통 중에도 알코올 발효가 지속적으로 진행되어 특유의 톡 쏘는 청량감을 느낄 수 있으나 유통기한이 짧은 단점이 있고, 살균 막걸리는 열처리를 하여 6개월 이상 보관이 가능하나 고유의 맛과 향을 잃는다는 단점이 있다(Kim YT & Kim MS 2011).
지금까지 막걸리에 대한 연구는 주로 생 막걸리에 대한 연구가 진행되었다. 반면, 시판 살균막걸리의 관능특성과 향기성분 분석(Park CS 2012) 외에는 살균 막걸리에 대한 연구가 부족한 실정이다. 따라서 본 연구에서는 원료에 따른 막걸리의 열처리 특성을 알아보기 위해 쌀과 밀로 직접 막걸리를 담그고, 가열 처리로 인한 변화를 분석하고자 하였다.
재료 및 방법
1. 실험재료
막걸리 제조용 원료는 2015년산 오대미(Dongsong Nonghyup, Cheolwon, Korea)를, 밀가루는 시중에서 판매하는 중력분 밀가루(CJ Cheiljedang Co. Ltd., Yangsan, Korea)를 사용하였다. 발효제는 역가 1,800 SP의 개량누룩(Korea enzyme Co. Ltd., Hwaseong, Korea)을 사용하였다. 효모는 ㈜비전바이오켐(Seongnam, Korea)에서 구매한 라빠리장(S.I. Lesaffre Co., Maroq-en-Baroeul, France)을 사용하였다.
2. 막걸리 담금 방법
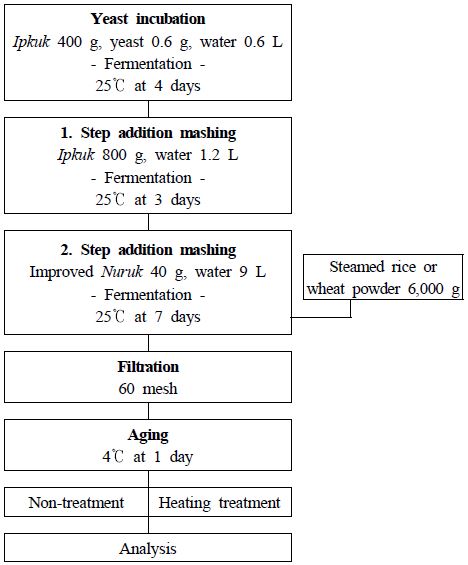
쌀 및 밀 막걸리 모두 2차 담금법으로 제조하였다. 쌀 입국, 효모 및 물을 혼합하여 4일간 25℃에서 발효시킨 밑술에 1차 덧술인 쌀 입국과 물을 추가로 첨가하여 3일간 동일온도에서 발효시켰다. 그리고 쌀 막걸리는 쌀의 증자를 위해 2시간 침지하고, 1시간 탈수하고 1시간 증자시켰다. 밀 막걸리의 밀은 적당량의 수분과 혼합하여 균질화한 후 1시간 증자하였고, 이렇게 만들어진 증자된 쌀 및 밀은 개량누룩과 물을 혼합하여 만든 2차 덧술로써 1차 덧술과 함께 혼합하여 7일간 25℃에서 발효시켰다(Seo MY 등 2005, Kim HR 등 2008).
Park YD(2016) 연구에서 가열 시간과 온도 변화에 따른 미생물의 생존율 변화를 실험하였는데, 55℃에서 25 min, 60℃에서 15 min, 65℃에서 10 min, 70℃에서 3 min, 75℃에서 1 min, 80℃에서 0.3 min 이상 가열처리할 때 생존율 0 %가 되었다. 따라서 본 연구에서는 가열처리 유무에 따른 변화를 극명하게 비교하기 위해 항온수조의 온도를 75℃로 설정하였고, 막걸리의 온도가 75℃가 되는 시점부터 1시간동안 중탕가열 처리하였다.
3. 이화학적 분석 방법
pH는 pH meter(Orion 3 star, Thermo Scientific Co., Singapore)를 이용하여 측정하였다. 총산은 시료 10 mL를 30 mL 비이커에 취하여 0.1 N NaOH 용액으로 pH 8.2로 중화될 때까지 적정하여 소요된 0.1 N NaOH 용액의 소비량을 젖산 함량(%, w/v)으로 표시하였다.
아미노산도는 여과액 10 mL를 0.1 N NaOH 용액으로 중화한 다음 중성 포르말린 용액 5 mL를 가하여 유리된 아미노산을 0.1 N NaOH 용액으로 적정하여 pH 8.2가 될 때까지 소요된 0.1 N NaOH의 mL수로 표시하였다.
가용성 고형분 함량은 굴절당도계(Palette, Atago Co. Ltd., Tokyo, Japan)를 사용하여 측정하였고, 환원당은 DNS(dinitrosalicylic acid)법을 이용하였다. 즉, 희석한 시료용액 0.2 mL에 DNS 시약 0.6 mL를 넣고 끓는 수욕 중에서 5분 동안 끓인 다음 실온에서 냉각하였다. 이후 증류수 4.2 mL를 넣고 혼합한 뒤, 분광광도계(JP/U-2000 spectrophotometer, Hitachi Ltd., Tokyo, Japan)를 사용하여 550 nm에서 흡광도를 측정하였으며, 포도당(glucose) 표준 검량선을 이용하여 환원당 함량(%, w/v)을 계산하였다.
발효기간 중의 술덧의 알코올 함량을 측정하기 위하여 원심분리한 시료를 간이 알코올 분석기(AL-3, Riken Keiki Korea Co. Ltd., Busan, Korea)를 이용해 알코올 함량을 분석하였다. 휘발산 함량은 알코올 분석용 증류액 30 mL를 취하여 삼각플라스크에 넣고 0.01 N NaOH로 pH 8.2가 될 때까지 적정하여 소비된 0.01 N NaOH를 초산(acetic acid)으로 환산하여 표시하였다.
색도는 색차계(Hunterlab Ultra Scan Pro, Reston, VA, USA)를 이용하여 명도(lighteness, L), 적색도(redness, a), 황색도(yellowness, b), 및 △E 값을 측정하여 나타내었다.
유기산은 HPLC(LC-20A, Shimadzu Co., Kyoto, Japan)를 이용하여 post column 방법으로 분석하였다. 유기산 분석용 칼럼(column)은 Shodex Rspack KC-G(6.0 mm × 50.0 mm) 가드 칼럼에 RSpak KC-811(8.0 mm × 300 mm, Showa Denko Co., Tokyo, Japan) 2개를 연결하여 사용하였다. Pump A의 이동상은 3 mM 과염소산(perchloric acid)을 이용하였으며, 유속(flow rate)은 0.8 mL/min, 칼럼 오븐(column oven)의 온도는 63℃로 하였다. 칼럼을 통과해 나온 분리물은 pump B의 이동상(0.2 mM Bromothymol blue, 15 mM Na2HPO4, 2 mM NaOH)과 반응(30℃)한 후 UV 440 nm에서 검출하였다. 이때 pump B의 flow rate는 1.0 mL/min로 하였다. 시료는 여과(0.2 μm, Millipore Co., Cork, Ireland)후 사용하였다.
유리당 분석을 위해서 HPLC(Waters e2695, Massachusetts, USA)를 이용하였으며, post column 방법을 사용하여 분석하였다. 유리당 분석용 column은 supelco sil LC-NH2(25 cm × 4.6 mm, Pennsylvania, USA)를 사용하였으며 RID로 검출하였다. 이동상은 80% acetonitrile(Mallinckrodt Baker Inc., Phillipsburg, USA)을 이용하였으며, flow rate는 1 mL/min, column oven의 온도는 25℃, injection volume 10 μL로 하였다. 시료는 여과(0.2 μm, Millipore Co., Cork, Ireland)후 사용하였다.
유리 질소화합물은 아미노산 자동분석기(L-8900, Hitachi Co., Tokyo, Japan)를 사용하였다. 시료 5 mL에 5% trichloroacetic acid(Junsei Chemical Co., Ltd., Tokyo, Japan) 5 mL를 첨가한 후 원심분리(4℃, 12,000⨉g, 15 min)하였다. 상등액을 회수한 다음 여과(0.2 μm, Millipore Co., Cork, Ireland)한 것을 분석하였으며, 분석조건은 제조사의 매뉴얼을 따랐다(Hitachi high-Technologies Corporation 2014).
모든 데이터는 3회 반복 측정하였으며, 평균±표준편차로 표시하였다. 통계분석은 SPSS(Statistics Package for the Social Science, Ver. 18.0 for window, Seoul, Korea)를 이용하여 대응표본 T 검정으로 유의성을 검증하였다. 유리 질소화합물 데이터 값은 XLSTAT(XLSTAT version 2014, Addinsoft, Paris, France)를 이용하여 주성분분석(Factor analysis)으로 도표화하였다.
결과 및 고찰
1. pH, 총산, 아미노산도, 가용성 고형분, 환원당, 알코올 및 휘발산 함량
막걸리의 가열처리 전과 후의 일반성분에 대한 결과와 대응표본 t검정을 통한 유의성 검토는 Table 1로 나타내었다. 쌀과 밀을 원료로 만든 각각의 막걸리에서 쌀 막걸리의 pH는 살균 전 3.74, 살균 후 3.82로 밀 막걸리 역시 살균 전 pH 4.13에서 살균 후 4.27로 약간 상승하였으며, 두 가지 종류의 막걸리에서 pH가 유의적인 차이를 나타냈다(P<0.01). pH 변화에 영향을 미치는 총산 함량과 비교해 볼 때 쌀 막걸리의 살균 전 0.70%였던 총산이 살균 후 0.67%로, 밀 막걸리는 0.83 %에서 0.71%, 따라서 pH와 총산의 경향이 유사하게 나타나는 것이 확인되었다. 총산은 여러 유기산의 종류 및 기타 산 유래 물질에 의해 함량이 종합적으로 나타난다고 한다(Song JC 등 1997) (Table 1).
막걸리의 아미노산도는 관능적으로 담백한 맛을 부여하는 성분이나, 지나치게 많은 양이 함유되어 있을 때에는 느끼하거나 쓴맛을 주어 주질을 하락시킨다(Yang HS & Eun JB 2011). 따라서 막걸리에 아미노산도가 관능적으로 미치는 영향이 큰데, Table 1에서 쌀 막걸리는 살균 전 4.40, 후 4.17, 밀 막걸리 살균 전 6.41, 후 6.46로 유의적인 차이는 없었다. Lee YJ 등(2012)의 연구에서 담근 막걸리에 아미노산 함량이 본 연구에 비해 다소 낮은데, 이는 알코올을 6%로 희석하여 함량의 차이가 나타났지만, 밀로 만든 막걸리에서 쌀로 만든 막걸리에 비해 더 높은 아미노산 함량을 나타내어 비슷한 경향을 확인할 수 있었다.
가용성 고형분 함량은 Table 1에 나타냈다. 쌀 막걸리는 살균 전, 12.47 °Brix, 후 10.63 °Brix, 밀 막걸리는 살균 전 14.90 °Brix, 후 13.67 °Brix로 밀 막걸리에서만 유의적인 차이를 나타냈다(P<0.001). 가용성 고형물은 용액 속 녹아있는 전분, 알코올, 당 등과 같이 여러 물질에 의해 영향을 받는다고 한다(Son HS 등 2011).
막걸리 중의 환원당은 에탄올 생성과 감미도에 관여하는 성분으로 중요한 성분이다(Lee HS 등 2010). 막걸리의 살균처리 전과 후의 변화는 Table 1에 나타냈다. 쌀 막걸리의 살균 전 환원당 함량은 0.35%, 살균 후 0.37%, 밀 막걸리는 살균 전 0.69%, 후 0.65%로 나타났다.
각 종류별 막걸리의 환원당 함량이 다른 것은 Lee YJ 등(2012)의 연구 결과에서 쌀의 품종, 도정도, 누룩에 따라 막걸리를 만들었을 때 유리당의 구성과 그 함량이 서로 상이한 것을 볼 수 있듯, 본 연구에서도 원료의 특징에 따른 차이인 것으로 판단된다.
각 막걸리의 알코올 함량은 Table 1로 나타냈다. 막걸리의 알코올 함량은 각 막걸리마다 가열처리 전과 후의 함량이 차이가 있는데, 쌀 막걸리는 18.57%에서 17.33%, 밀 막걸리는 19.40%에서 18.73%로 두 처리구에서 동일하게 감소하는 경향을 나타냈다. 알코올은 휘발성이 강한 화합물로 발효주에서의 주요 알코올은 에탄올이며, 발효주의 경우 20% 이하의 에탄올이 물과 섞여 있기 때문에 저온살균처리와 같이 비교적 저온에서는 거의 휘발되지 않는다고 한다(James D & Crum, Ph D 1997). 따라서 가열 전후 달라진 알코올 함량은 휘발성이 강한 메탄올, 에스테르, 휘발산 등의 화합물이 휘발된 것으로 판단된다.
막걸리의 휘발산 함량은 Table 1에 나타냈다. 휘발산 함량은 쌀 막걸리 67.47∼58.53 mg/L, 밀 막걸리 88.20∼60.93 mg/L로 가열처리 후 줄어들었다. 발효주에 있어 휘발산은 주로 초산 등의 휘발성이 높은 산 종류로 휘발산이 높다는 것은 그만큼 발효 중에 휘발산을 생성하는 미생물에 오염이 되었다는 것을 의미하며, 발효주에는 초산을 생성하는 Acetobacter aceti나 Gluconobacter oxydans 등의 균에 의해 발효주 표면에 반투명의 점착성이 있는 막을 형성하여 혼탁해지게 된다고 한다(Graham HF 1993; Joyeux A 등 1984). 따라서 본 연구에서는 오염으로 인한 성분 변화 없이 발효가 정상적으로 이루어진 것을 확인할 수 있었다.
2. 색도
발효주인 막걸리는 아미노산, 유리당, 유기산 등과 같은 영양성분 함량이 높다고 한다(Kim HR 등 2009; Kang JE 등 2015). 따라서 가열에 의한 비효소적 갈변이 일어날 가능성이 높아, 본 실험에서는 색도를 측정하여 갈변 발생을 파악하고자 하였다.
색도 측정에 대한 결과는 Table 2와 같이 정리하였다. 색도의 변화가 유의적인 차이를 나타낸 처리구는 쌀 막걸리의 L값이 0.2만큼의 소폭 상승하였고(P<0.05), 밀 막걸리에서는 a값이 0.1만큼 낮아졌다. L값은 명도에 영향을 주는데 높을수록 밝아지며, a, b 값은 0에 가까울수록 칙칙한 색을 띄게 된다. 그러나 ΔE는 색도의 차이를 나타내는 수치인데, ΔE 값에서 유의적인 차이가 나타나지 않았다. 따라서 본 실험에서는 가열처리에 의한 갈변현상은 발생하지 않은 것으로 유추할 수 있다.
3. 유기산
막걸리의 유기산은 Table 3과 같은 함량을 나타냈다. 원료별로 처리한 막걸리 각각의 유기산 조성과 함량에 차이를 나타냈다. 쌀 막걸리는 주요 유기산으로는 malic acid, citric acid가 나타났고, 밀 막걸리는 citric acid, malic acid로 원료에 따라 주요 유기산에 차이가 있는 것을 알 수 있었다. 그러나 가열에 의한 유기산 총 함량에 변화가 유의적인 차이를 나타나지 않았다. 따라서 가열처리에 따른 신맛의 변화는 없는 것으로 유추할 수 있다.
4. 유리당
유리당 분석 결과는 Table 4와 같이 나타냈다. 유리당은 사용하는 원료와 발효제 종류에 따라 달라지기도 하며, 담금 방법이나 배합비율에 따라서도 차이를 나타낸다고 한다(Lee YJ 등 2012; Jeong JW 등 2006). 따라서 본 연구에서도 처리별로 담근 막걸리의 유리당 함량이 유의적인 차이를 나타냈다(P<0.05). 쌀, 밀을 원료로 담근 막걸리의 유리당 함량은 가열처리 후 증가하였다.
5. 유리 질소화합물
아미노산은 종류에 따라 맛과 향을 갖고 있는데, alanine, glycine, serine, tyrosine 등은 단맛을 갖고, proline, aspartic acid 등은 신맛을 갖는다. 이들은 형태에 따라 쓴맛, 떫은맛을 갖기도 하며, 방향성이 강한 ethanolamine과 같은 경우에는 암모니아 성향을 띄기도 한다(Lee JG 등 2015). 따라서 원료별로 담근 막걸리의 유리 질소화합물 함량은 Table 5로 작성하였다.
원료별로 담금 막걸리의 유리 질소화합물은 공통적으로 alanine, arginine, glutamic acid, leucine, lysine, phenylalanine, proline, tyrosine, valine, methionine이 주요 질소화합물로서 검출되었고, 각각의 함량을 비교해 보았을 때 α-aminobutyric acid, β-aminoisobutyric acid, histidine, isoleucine, leucine, methionine, phenylalanine, proline, serine의 함량이 밀을 원료로 사용한 막걸리가 쌀을 원료로 사용한 막걸리에 비해 유의적으로 더 높았고(P<0.01), alanine, ammonia, anserine, arginine, carnosine, citrulline, cystathionine, ethanol amine, glycine, hydroxylysine, lysine, sarcosine, urea의 함량은 유의적으로 더 낮은 것을 확인할 수 있었다(P<0.05). 이는 원료에 따른 차이로 사료된다.
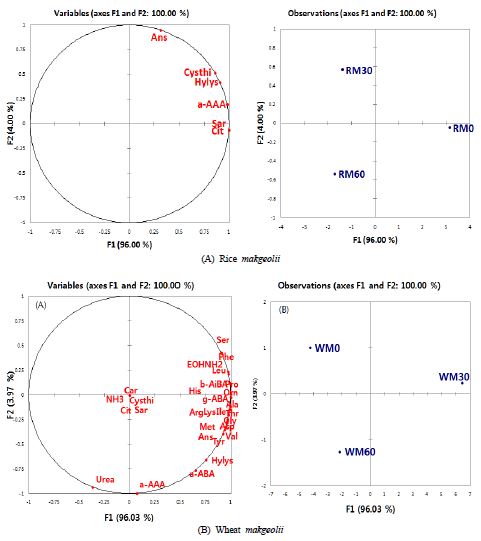
가열처리로 인한 유리 질소화합물의 조성 변화는 쌀 막걸리의 경우 anserine, α-aminoadioic acid, citrulline, cystathionine, hydroxylysine, sarcosine이 유의적으로 감소하였고(P<0.05), 밀 막걸리의 경우 α-aminobutyric acid가 유의적으로 증가한 것을 확인할 수 있었다(P<0.05). 하지만 유리 질소화합물의 총 함량에서는 유의적 차이는 확인할 수 없었다. 가열처리가 원료별로 만든 막걸리의 유리 질소화합물 조성에 영향을 줄 수 있는지를 알아보기 위해 정량한 Table 5 값을 바탕으로 다변량 분석을 통해 상관성이 있는 유리 질소화합물을 선별하여 주성분 분석으로 Fig. 2에 나타내었고, 정량 값과 비교하며 분석하였다. Fig. 2는 쌀 막걸리를 가열처리 전과 30분, 60분 가열처리한 것으로, Fig. 2 (A)에는 쌀 막걸리에 함유된 유리 질소화합물들이 변수에 의해 분포되어 나타나 있고, Fig. 2 (B)는 상관성이 있는 질소화합물 위치에 따라 각 처리구가 분포되어 있다. Fig. 2 (A)에서 x축의 제 1주성분(F1)의 영향력은 96.00%로 y축의 제 2주성분(F2: 4.00%)보다 24배 차이가 나기 때문에 세로축보다 가로축에 의해 분리되는 영향력이 크다. 쌀 막걸리의 경우 anserine, α-aminoadioic acid, citrulline, cystathionine, hydroxylysine, sarcosine 선별되었다. 쌀 막걸리 가열처리 전 제4사분면에 부하되었고, 30분 가열처리 시 α-aminoadioic acid, citrulline, cystathionine, sarcosine의 함량이 유의적으로 감소하여(P<0.05) 제1주성분의 음의 방향으로 이동하여 제2사분면으로 부하되었다. 60분 가열처리 시 anserine, cystathionine, hydroxylysine의 함량이 유의적으로 감소하여(P<0.05) 제2주성분의 음의 방향으로 이동하여 제3사분면으로 부하되었다. 최종적으로 제1주성분의 양의 방향으로 서로 대칭을 이루어 가열처리로 인한 유리 질소화합물의 조성 변화를 확인할 수 있었다. 밀 막걸리의 경우 α-aminobutyric acid가 선별되었지만 변수가 부족하여 다변량 분석을 할 수 없었고, 정량 값과 함께 비교했을 때에도 유리 질소화합물의 조성 변화가 적다는 것을 확인할 수 있었다. 이러한 결과를 통해 가열로 인한 유리 질소화합물들의 성분변화에 원인은 명확히 밝혀진 부분이 없지만, 가열로 인한 구조 변화에 의한 것으로 추론할 수 있다.
요약 및 결론
본 연구에서는 가열처리에 의한 막걸리의 맛과 향에 미치는 영향을 알아보기 위해서 주로 원료로 사용하는 쌀과 밀을 각각 사용하여 막걸리를 담그고 가열처리하여 그 차이점을 분석하였다. 가열처리 전과 후, 맛에 영향을 주는 유기산, 유리당, 유리 질소화합물을 분석한 결과, 유기산에서는 밀이 932.20 mg%였고, 쌀은 839.03 mg%로 차이가 있었으며, 가열처리 전과 후의 유기산 함량은 유의적인 차이가 없었다. 다음으로 단맛에 영향을 주는 유리당 함량은 쌀 0.86∼1.06, 밀 0.91∼1.13으로 가열처리 전과 후에서 유의적인 차이를 나타냈다(P<0.05, P<0.001). 유리 질소화합물 함량을 분석한 결과, 공통적으로 alanine, arginine, glutamic acid, leucine, lysine, phenylalanine, proline, tyrosine, valine, methionine이 주요 질소화합물로서 검출되었고, 원료에 따른 함량은 α-aminobutyric acid, β-aminoisobutyric acid, histidine, isoleucine, leucine, methionine, phenylalanine, proline, serine, alanine, ammonia, anserine, arginine, carnosine, citrulline, cystathionine, ethanol amine, glycine, hydroxylysine, lysine, sarcosine, urea이 유의적으로 차이가 있었다(P<0.05). 가열처리 전과 후의 주요 성분의 변화를 보기 위해 PCA(Principal Component Analysis) 분석한 결과 쌀 막걸리의 경우 가열 후 anserine, α-aminoadioic acid, citrulline, cystathionine, hydroxylysine, sarcosine의 함량이 유의적으로 변화하여 영향을 주었고(P<0.05), 밀 막걸리의 경우 가열 후 α-aminobutyric acid가 유의적으로 차이가 있었지만(P<0.05), 변수의 부족으로 주성분 분석은 못하였으며 가열 처리에 의한 변화가 적다는 것을 알 수 있었다.
따라서 본 연구에서는 막걸리의 가열처리에 따른 성분에 변화가 있었지만, 원료에 따라 성분의 변화가 다른 것을 확인하였으며, 밀로 만든 막걸리보다는 쌀로 만든 막걸리의 유리 질소화합물의 변화가 크다는 것을 확인하였다. 또한 어느 한 물질에 의한 차이보다는 여러 화합물이 복합적인 변화로 가열처리 전과 후에 차이가 있다는 것을 확인할 수 있었으며, 성분 변화가 맛에 영향을 미치는 정도는 향후 더 깊이 있는 연구가 필요하다.
Acknowledgments
본 연구는 국립농업과학원 농업과학기술 연구개발사업(과제번호: PJ011353)의 지원에 의해 이루어진 것으로 지원에 감사드립니다.
REFERENCES
- Graham, HF, (1993), Wine Microbiology and Biotechnology, Harwood Academic Publishers, Langhorne, USA, p400-401.
- Hough, JS, Briggs, DE, Stevens, R, Young, TW, (1982), Metabolism of wort by yeast. Vol Ⅱ, pp 566-611. In: Malting and Brewing Science, Chapman and Hall Press, New York, USA.
- Hitachi High-Technologies Corporation, (2014), L-8900 Amino Acid Analyzer, http://www.hitachi-hitec.com/global/science/lc/18900.html#jump2 Accessed on 17. 10. 2017.
- Joyeux, A, Lafon-Lafourcade, S, Ribereau-Gayon, P, (1984), Evolution of acetic acid bacteria during fermentation and storage of wine, Appl Environ Microbiol, 48(1), p153-156.
- James D, Crum, (1997), Must and wine composition VolⅠ, p19-21, In: Concepts in Wine Chemistry, The Wine Appreciation Guild Ltd, South San Francisco, USA.
- Jeong, JW, Park, KJ, Kim, MH, Kim, DS, (2006), Quality characteristics of takju fermentation by addition of chestnut peel powder, Korean J Food Preserv, 13(3), p329-336.
-
Kang, JE, Kim, JW, Choi, HS, Kim, CW, Yeo, SH, Jeong, ST, (2015), Quality characteristics of rice and rice starch-based yakju, Korean J Food preserv, 22(3), p353-360.
[https://doi.org/10.11002/kjfp.2015.22.3.353]

- Kim, DY, Kwon, DJ, Yang, HC, Yoon, HS, (1985), Vegetable food, Ⅰ, p465-467, In: Food Chemistry, Youngji Publisher, Seoul, Korea.
- Kim, HR, Jo, SJ, Lee, SJ, Ahn, BH, (2008), Physicochemical and sensory characterization of a Korean traditional rice wine prepared from different ingredients, Korean J Food Sci Technol, 40(5), p551-557.
- Kim, HR, Kwon, YH, Jo, SJ, Kim, JH, Ahn, BH, (2009), Characterization and volatile flavor components in glutinous rice wine prepared with different yeasts of nuruks, Korean J Food Sci Technol, 41(3), p296-301.
- Kim, IS, Lee, JS, Cho, MH, (2012), The analysis of the relationships among makgeolli consumers’ purchase motivations, selection attributes and consumer satisfaction, Journal of Tourism Studies, 24(3), p57-81.
- Kim, YS, Shin, KS, Lee, JH, (2017), Comparative study of total acidity content of makgeolli with pre-treatment and analysis methods, J Korean Soc Food Sci Nutr, 46(5), p600-607.
- Kim, YT, Kim, MS, (2011), Makgeolli’s character for the globalization, J Tourism Leisure Res, 23(6), p333-349.
- Lee, CH, Lee, HD, Kim, JY, Kim, KM, (1989), Sensory quality attributes of takju and their changes during pasteurization, Korean J Dietary Cult, 4(4), p405-410.
- Lee, HS, Park, CS, Choi, JY, (2010), Quality characteristics of the mashes of takju prepared using different yeasts, Korean J Food Sci Technol, 42(1), p56-62.
- Lee, JG, Moon, SH, Bea, KH, Kim, JH, Choi, HS, Kim, TW, Jeong, C, (2015), Sensory and component of distilled spirits Vol Ⅰ, pp 365-468. In: Distilled Spirits, Kwangmoonkag Press, Paju, Korea.
-
Lee, YJ, Yi, HC, Hwang, KT, Kim, DH, Kim, HJ, Jung, CM, Choi, YH, (2012), The qualities of makgeolli made with different rice cultivars, milling degrees of rice, and nuruks, J Korean Soc Food Sci Nutr, 41(12), p1785-1791.
[https://doi.org/10.3746/jkfn.2012.41.12.1785]

-
Min, JY, Kim, NY, Kim, US, Han, MJ, (2015), The quality characteristics of pasteurized ginseng makgeolli added with different concentration of ginseng powder, Korean J Food Cult, 30(6), p757-765.
[https://doi.org/10.7318/KJFC/2015.30.6.757]

- Park, CS, (2012), Sensory characteristics and volatile compounds analysis of commercial sterilized makgeolli, Sejong University, Seoul, Korea.
- Seo, MY, Lee, JK, Ahn, BH, Cha, SK, (2005), The changes of microflora during the fermentation of takju and yakju, Korean J Food Sci Technol, 37(3), p61-66.
-
Son, HS, Park, BD, Ko, BK, Lee, CH, (2011), Quality characteristics of takju produced by adding different amount of water, Korean J Food Sci Technol, 43(4), p453-457.
[https://doi.org/10.9721/KJFST.2011.43.4.453]

- Song, JC, Park, HJ, Shin, WC, (1997), Change of takju qualities by addition of cyclodextrin during the brewing and aging, Korean J Food Sci Technol, 29(5), p895-900.
-
Yang, HS, Eun, JB, (2011), Fermentation and sensory characteristics of Korean traditional fermented liquor (Makgeolli) added with citron juice, Korean J Food Sci Technol, 43(4), p438-445.
[https://doi.org/10.9721/KJFST.2011.43.4.438]