
경남 일부지역 폐경 전·후 여성들의 골밀도와 영양소 섭취량 및 신체계측치와의 관련성에 대한 비교
Abstract
This study compared relationships between bone mineral density (BMD), and nutrient intakes and anthropometric indices in pre- and postmenopausal women. The subjects were divided into normal and risk groups according to their bone status as shown by T-score. The height (p<0.01), weight (p<0.01), body fat mass (BFM) (p<0.05), lean body mass (LBM) (p<0.05) and BMI (body mass index) (p<0.05) were significantly higher in the normal group than the risk group in premenopausal women. Additionally, the intakes of total protein, animal protein, vitamin K, thiamin, riboflavin, niacin, vitamin B6, K and Se, and the rate of animal/plant protein intake were significantly higher (p<0.05) in the normal group than the risk group for premenopausal women. In postmenopausal women, the intakes of animal protein, vitamin D, vitamin K and thiamin, as well as the rates of animal/plant protein and Ca/P intakes were significantly higher (p<0.05) in the normal group than the risk group. However, the plant protein intake was significantly higher (p<0.05) in the risk group than the normal group in both pre- and postmenopausal women. In premenopausal women, the lumbar spine BMD was positively correlated with the age, height, weight and LBM, and the intakes of energy, vitamin K, thiamin, riboflavin, niacin, folate, and magnesium, and negatively correlated with the sodium intake. The femur BMD was positively correlated with the age, weight, BFM, BMI and WHR, as well as the intakes niacin and vitamin B6. In postmenopausal women, the femur BMD was positively correlated with the weight, BFM, BMI and WHR, as well as the intakes of vitamin D and magnesium, while it was negatively correlated with the age. In conclusion, the nutrient intakes and anthropometric indices might have bigger effects on BMD in premenopausal women than postmenopausal women. The body weight, vitamin D, vitamin K, thiamin, riboflavin, niacin, vitamin B6, folate and magnesium were important factors influencing BMD in women.
Keywords:
bone mineral density, nutrient intakes, anthropometric indices, premenopausal women, postmenopausal women서론
최근 고령 인구가 늘어남에 따라 골다공증은 많은 국가에서 심각한 건강문제로 인식되고 있다(Holroyd C 등 2008). 골다공증(Osteoporosis)은 골밀도(Bone mineral density; BMD)의 감소로 나타나게 되는 대표적인 대사성 골 질환으로 골을 유약하게 하여 골절의 위험률을 높여 기능적 의존성을 증가시키고, 노인의 질병 발생에 중요한 역할을 한다(Shen CL 등 2013). 또한 이에 대한 사회경제적 비용이 급격히 증가되고 있는 실정이다(Lee JS & Jang SG 2013). 그러므로 골다공증 및 골절의 예방은 삶의 질과 건강문제뿐만 아니라, 경제적인 측면에서도 매우 중요하다.
2012년 국민건강영양조사에 의하면 우리나라 50세 이상 성인의 골다공증 유병률은 평균 21.4%이고, 남자가 7.8%인데 비해 여자는 34.9%(Korea Centers for Disease Control and Prevention 2013)로 여자가 남자에 비해 약 4.5배 정도 높다. 골감소증(Osteopenia)은 골밀도가 정상보다 줄어든 상태를 말하며, 골다공증의 전단계로 간주되나, 골감소증을 갖고 있더라도 모두가 골다공증으로 진행되는 건 아니다(WHO Scientific Group on the Prevention and Management of Osteoporosis 2000). 우리나라 여성들의 골감소증 유병률은 지역이나 연령에 따라 차이를 나타내어 16.0%(Lee JS 등 2006)~43.5%(Koo JO 등 2008) 정도로 보고되어 있다.
골밀도는 골량을 나타내는 대표적인 지수로 골량은 30~35세에 최대치에 도달한 후 골 형성과 골 흡수가 균형을 유지하다가 40세 이후부터 골 흡수가 상대적으로 증가하여 골량이 감소하게 되어 매년 1~2% 정도 골밀도가 감소된다(Chung YJ 등 2001). 특히 여성들인 경우, 폐경이 되면 에스트로겐의 부족으로 골 손실이 증가되어 골밀도가 급격히 감소되는 것으로 알려져 있다(Ilich JZ & Kerstetter JE 2000; Riggs BL 등 1998). 따라서 성인 초기에 골량을 최대로 확보하고 폐경 이후 골량 감소를 최소로 줄이는 것이 골 건강을 위해 매우 중요하다고 볼 수 있다.
골량 형성에는 여러 가지 요인이 복합적으로 관여하는데(Cashman KD 2007), 영양은 골격 발달과 최대 골량 형성에 가장 중요한 요인 중의 하나라고 하였다(Heaney RP 등 2000; Ilich JZ & Kerstetter JE 2000). 특히 칼슘(Andon MB 등 1991)과 비타민 D(Dawson-Hughes B 등 2005)가 골격건강을 유지하는 중요한 영양소로 알려져 있다. 단백질 섭취량과 골밀도와의 관련성에 대해서는 논란의 여지가 큰데, 일부 연구에서 단백질 섭취는 골 건강에 도움이 된다고 하였고(Ilich JZ 등 2003), 또 다른 연구에서는 단백질은 골밀도를 감소시키며, 특히 단백질의 과잉섭취는 요 중 칼슘 배설을 증가시켜 골 건강에 악영향을 준다고 하였다(Thorpe MP & Evans EM 2011). 그리고 비타민 K(Binkley NC & Suttie JW 1995), 칼륨(Macdonald HM 등 2005) 및 마그네슘(Orchard TS 등 2014)은 골밀도 증가에 도움이 되며, 인은 과잉 섭취시 칼슘의 흡수를 방해하고, PTH의 분비를 촉진하여 골 손실을 초래한다고 알려져 있다(Calvo MS 1994). 또한 체중, 체질량지수, 체지방량 및 제지방량 등의 신체계측치는 골밀도와 양의 상관성을 나타낸다고 하였으며(Kim MS & Koo JO 2007; Lim JH 등 2008; Lu LJW 등 2009), 체중 감소는 골량의 감소를 초래하고 골절률의 위험을 증가시킨다고 하였다(Langlois JA 등 2001; Shapes SA & Reidt CS 2006).
이상에서 살펴본 바와 같이 골밀도와 영양소 섭취 및 신체계측치와의 관련성에 대한 연구가 이루어지고 있으나, 폐경 전·후 여성들의 골밀도에 영향을 미치는 요인에 관한 비교 연구는 거의 없는 실정이다. 따라서 본 연구는 폐경 전·후여성들을 대상으로 영양소 섭취량 및 신체계측치와 골밀도와의 관련성을 비교 분석하였다. 이와 같은 분석을 통해 여성들의 골 건강에 미치는 이들 요인이 폐경 전·후 어떻게 다른지 비교하여 폐경 전·후 여성들에게 적합한 골 건강과 골다공증 예방을 위한 영양교육 자료를 제공하고자 하였다.
연구방법
1. 연구대상자 및 기간
본 연구는 건강검진을 목적으로 경상대학교병원을 방문한 22~69세 여성들 중 지원 의사를 밝힌 폐경 전·후 여성들 각각 50명씩 총 100명을 대상으로 하였다. 골밀도에 영향을 미칠 것으로 예상되는 40대 이하의 조기 폐경, 여성호르몬 치료, 난소 및 자궁 적출 여성과 갑상선질환, 신장질환, 고혈압 및 당뇨병 등의 만성질환이 있는 여성을 제외하였으며, 2014년 8월부터 9월까지 시행하였다(IRB 승인; GIRB-A14-Y-0031).
2. 골밀도(Bone Mineral Density; BMD) 측정
조사 대상자들의 골밀도는 이중에너지 방사선 골밀도 측정기(Dual energy X-ray absorptiometry-DEXA: DPX-Bravo, GE)를 이용하여 골다공증의 주요 지표가 되는 부위인 요추와 대퇴골이 측정되었다. 요추(lumbar spine, L2~L4)는 제 2~4 요추까지의 골밀도 평균치, 대퇴골(femur)은 대퇴경부(femoral neck), 와드 삼각부(Ward's triangle) 및 대퇴 전자부(femoral trochanter)의 골밀도 평균치가 각각 사용되었다.
골밀도는 WHO의 기준(WHO 1994)인 T-score(건강한 젊은 성인의 평균 골밀도와의 비교치)를 기준으로 {< -2.5; 골다공증(osteoporosis), -2.5~-1.0; 골감소증(osteopenia), >-1.0; 정상(normal)}에 따라 판단되었다. 대상자들은 선행연구(Kim MS & Koo JO 2008)를 참고하여 요추 및 대퇴골밀도가 모두 정상이면 정상군, 요추와 대퇴부 중 어느 한 부위라도 골감소증 또는 골다공증이 있는 경우 위험군으로 분류하였다.
3. 신체 계측
조사 대상자들의 신장은 신장측정기(주. 삼화계측)로 측정하였으며, 체중, 체지방량(body fat mass; BFM), 제지방량(lean body mass; LBM), 체질량지수(body mass index; BMI), 및 허리-엉덩이 둘레비율(waist to hip circumference rate; WHR)은 정밀체성분분석기(Inbody 720, Biospace, Korea)를 이용하여 측정하였다.
4. 식사섭취 조사 및 영양소 섭취량 분석
식사섭취 조사는 훈련된 조사원들에 의해 직접 면담을 통해 이루어졌으며, 24시간 회상법(24-hour recall method)을 이용하여 주중과 주말 각각 1일씩 총 2일간의 식품섭취량을 조사하여 그 평균을 구하였다. 식품섭취 분량을 보다 정확하게 파악하기 위해 식품 모형을 이용하였다. 영양소 섭취량 및 섭취비율은 조사된 식품 섭취량으로부터 전문가용 CAN Pro 4.0(Computer Aided Nutritional Analysis Program 4.0, 한국영양학회)을 이용하여 분석하였다.
5. 통계분석
모든 자료의 통계분석은 PASW statistics 18.0을 이용하여 각 변인마다 평균과 표준편차를 구하였고, 정상군과 위험군 간의 유의성은 t-test로 검증하였으며, 빈도분석으로 골밀도에 따른 정상군과 위험군의 인원수와 비율을 구하였다. 골밀도와 영양소 섭취량 및 신체계측치와의 상관관계는 Pearson’s correlation coefficient로 분석하였다. 모든 분석의 유의수준은 p<0.05에서 검증하였다.
결과 및 고찰
1. 골밀도
Table 1은 대상자들의 요추 및 대퇴골의 평균 골밀도와 WHO의 골 건강 평가 기준(WHO 1994)에 따른 대상자들의 분류를 나타낸 것이다. 요추골밀도는 폐경 전 여성들(0.42±0.18)이 폐경 후 여성들(-0.08±0.21)에 비해 유의하게 높았다(p<0.05). 대퇴골밀도는 군 간의 유의한 차이는 없었으나, 폐경 후 여성들(0.07±0.16)이 폐경 전 여성들(0.02±0.16)에 비해 오히려 약간 높게 나타났다. 이는 본 조사대상 폐경 후 여성들은 폐경 후 평균 기간이 약 5.2세로 크게 길지 않는 것도 하나의 원인이 될 수 있을 것으로 추측된다. 그리고 폐경 전 여성들의 요추 및 대퇴골밀도는 서울지역 병원에서 건강검진을 받은 평균 연령 45세인 폐경 전 여성들의 요추 및 대퇴골밀도(Park JY 등 2011)에 비해 낮은 수준이었다. 반면에 폐경 후 여성들의 요추 및 대퇴골밀도는 서울지역 병원에서 건강검진을 받은 평균 연령 55세인 폐경 후 여성들(Park JY 등 2011)에 비해 높은 수준을 나타내었다.
요추골밀도는 폐경 전 여성들인 경우, 78.0%가 정상, 22.0%가 골감소증이었고, 폐경 후 여성들인 경우에는 62.0%가 정상, 32.0%가 골감소증, 6.0%가 골다공증으로 나타났다. 대퇴골밀도는 폐경 전 여성들인 경우 76.0%가 정상, 24.0%가 골감소증이었고, 폐경 후 여성들인 경우에는 86.0%가 정상, 12.0%가 골감소증, 2.0%가 골다공증으로 나타났다. 요추 및 대퇴골밀도가 모두 정상이면 정상군, 요추와 대퇴부 중 어느 한 부위라도 골감소증 또는 골다공증이 있는 경우 위험군으로 분류한 결과, 폐경 전·후 여성들 모두 29명(58.0%)은 정상군, 21명(42.0%)은 위험군에 속하였다.
2. 신체계측치 및 생리적 특성
Table 2에서 보는 바와 같이 연령은 폐경 전 여성들인 경우 정상군은 37.0±8.7세, 위험군은 34.1±9.9세, 폐경 후 여성들인 경우 정상군은 55.5±5.1세, 위험군은 55.7±4.1세로 나타났다. 폐경 전 여성들인 경우, 신장(p<0.01), 체중(p<0.01), BFM(p<0.05), LBM(p<0.05) 및 BMI(p<0.05)는 정상군이 위험군에 비해 유의하게 많았다. 본 조사 결과는 체중, BFM, LBM, BMI 및 허리둘레가 클수록 골밀도가 높게 나타난 평균 연령 36.2세인 미국 폐경 전 여성들(Lu LJW 등 2009)과는 일치하였다. 반면에, 신장은 골밀도에 긍정적인 영향을 미치나, 체중과 BMI는 골밀도에 영향을 미치지 않는다는 서울대학교 병원 건강검진센터를 내원한 평균 연령 약 39.2세인 폐경 전 여성들(Oh SI 등 2003)과는 다소 차이가 있었다.
폐경 후 여성들인 경우에는 신장, 체중, BFM, LBM, BMI 및 WHR 등 모든 지수들이 군 간의 유의한 차이가 없었다. 이는 신장, 체중 및 BMI는 골밀도에 유의한 영향을 미치지 않는다는 대구지역 노인 여성들(Choi MJ 등 2007)과는 일치하였다. 하지만 체중은 폐경 여성들의 골밀도에 영향을 미치는 주요 요인이라고 한 Wardlaw GH(1996) 및 WHR은 체중과는 독립적으로 골밀도에 부정적인 영향을 미친다는 Bhupathiraju SN 등(2011)의 보고와는 차이가 있었다. 또한, 폐경 여성들인 경우, 4~13%의 체중 감소는 체중 변화가 거의 없는 여성들에 비해 1~4%의 골 손실이 나타났다고 하였다(Riedt CS 등 2005). 그리고 체중은 폐경 후 여성들의 골밀도에 영향을 미치는 주요 요인이며, BMI가 22 이하인 경우 골다공증의 위험이 높아지는 반면, 26 이상인 경우에는 보호효과가 있다고 보고된 바 있다(Wardlaw GH 1996). 본 조사결과에 의하면 평균 신체계측치는 폐경 전 여성들의 골밀도와는 연관성이 있으나, 폐경 후 여성들의 골밀도와는 연관성을 나타내지 않는 것으로 추측할 수 있었다.
3. 영양섭취 상태
Table 3은 대상자들의 1일 열량 및 영양소 섭취량을 나타낸 것이다. 총단백질 섭취량은 폐경 전 여성들은 정상군이 위험군에 비해 유의하게 많았으나(p<0.05) 폐경 후 여성들은 군 간의 유의한 차이가 없었다. 폐경 전·후 여성들 모두 동물성 단백질 섭취량은 정상군이 위험군에 비해 유의하게 많은 반면 식물성 단백질 섭취량은 위험군이 정상군에 비해 유의하게 많았다(p<0.05). 비타민 D 섭취량은 폐경 전 여성들은 군 간의 유의한 차이가 없었으나 폐경 후 여성들은 정상군이 위험군에 비해 유의하게 많았다(p<0.05). 비타민 K 섭취량은 폐경 전·후 여성들 모두 정상군이 위험군에 비해 유의하게 많았다(p<0.05). 티아민 섭취량도 비타민 K 섭취량과 마찬가지로 폐경 전·후 여성들 모두 정상군이 위험군에 비해 유의하게 많았다(p<0.05). 리보플라빈, 니아신, 비타민 B6, 칼륨 및 셀레늄 섭취량은 폐경 전 여성들인 경우에 정상군이 위험군에 비해 유의하게 많았으나(p<0.05), 폐경 후 여성들인 경우에는 군 간의 유의한 차이가 없었다.
고단백식사는 요 중 칼슘 배설량을 증가시켜 골다공증의 원인이 될 수 있으나(Kerstetter JE & Allen LH 1994), 1일 90g 이내의 단백질 섭취는 체내 칼슘 균형에 영향을 주지 않고 골밀도에 긍정적인 영향을 미친다고 하였다(Koo JO 등 1991). 본 폐경 전 여성들의 1일 단백질 섭취량도 같은 범위에 속할 뿐만 아니라, 적정섭취비율이 1로 권장섭취량을 상회하므로 골 건강에 이로운 효과를 나타낸 것으로 추측된다. 그리고 본 조사 대상자들인 경우 폐경 유무에 상관없이 동물성 또는 식물성 단백질에 따라 골밀도에 상반된 연관성을 나타내었다. 이는 단백질 급원이 골 건강에 대한 단백질의 역할에 영향을 미친다고 한 Beasley JM 등(2014)과 성인인 경우 동물성 단백질 섭취량은 골밀도와 양의 상관성을, 식물성 단백질 섭취량은 골밀도와 음의 상관성을 나타낸다고 한 Promislow J 등(2002)의 결과와 일치하였다. 반면에 동물성 단백질은 여성들의 골밀도에 부정적인 영향을 미친다고 한 Kim JS 등(2011)의 보고와는 상반된 결과였다. 단백질은 골격의 기질 형성과 인슐린유사 성장인자(Insulin-like growth factor-Ⅰ; IGF-Ⅰ)의 증가(Jesudason D & Clifton P 2011) 및 근육량의 유지(Paddon-Jones D & Rasmussen BB 2009) 등에 관여함으로써 골다공증 및 골절을 예방한다고 알려져 있다.
골 건강과 밀접한 관련성이 큰 것으로 알려져 있는 칼슘과 비타민 D 섭취량을 살펴보면 칼슘 섭취량은 폐경 전·후 여성들 모두 군 간의 유의한 차이가 없었고, 비타민 D 섭취량은 폐경 후 여성들인 경우에만 정상군이 위험군에 비해 유의하게 많게 나타났다. 이는 칼슘 섭취는 골밀도에 유의한 영향을 나타내지 않는다는 Sowers MR 등(1992)의 보고 및 폐경 후 여성들인 경우 비타민 D의 결핍은 골다공증을 초래한다고 한 Dawson-Hughes B 등(2005)의 보고와는 같은 경향이었으나, 칼슘 섭취량이 골밀도에 영향을 미치는 주요 인자라고 한 Lee YS 등(2005)의 보고와는 차이가 있었다. 비타민 D의 결핍은 골격 석회화의 부족을 초래하고, 2차적으로 PTH의 과다 분비를 일으켜 골격으로부터 칼슘의 이동을 촉진하여 골밀도를 감소시킨다고 알려져 있다(Dawson-Hughes 등 2005). 비타민 K의 섭취량은 폐경 전·후 여성들 모두 정상군이 위험군에 비해 유의하게 많게 나타나 폐경 유무와 상관없이 여성들의 골 건강에 긍정적인 영향을 주는 것으로 나타났다. 그리고 이는 비타민 K의 섭취 부족은 여성들의 골 손실과 관련성이 크다고 한 Vermeer C 등(1996)의 보고와 같은 경향이었고, 비타민 K의 섭취량은 골밀도에 영향을 나타내지 않았다고 한 Booth SL 등(2003)의 보고와는 차이가 있었다.
비타민 B군 중 티아민 섭취량은 폐경 전·후 여성들 모두 정상군이 위험군에 비해 유의하게 많았고, 리보플라빈, 니아신, 비타민 B6 섭취량은 폐경 전 여성들의 골밀도에만 긍정적인 영향을 주는 것으로 나타났다. Dai Z & Koh WP(2015)는 티아민, 리보플라빈, 비타민 B6, 엽산 및 비타민 B12는 골건강에 도움이 되지만 이들 비타민 보충제 섭취는 골다공증이나 골절 예방에 도움이 되지 않는다고 보고한 바 있다. Abrahamsen B 등(2005)은 영국과 덴마크 폐경 여성들인 경우 리보플라빈 섭취량이 가장 적은 4분위 여성들의 요추 및 대퇴경부 골밀도가 가장 낮았다고 하였다. 그리고 폐경 전 여성들의 니아신 섭취량은 정상군이 위험군에 비해 유의하게 많았는데, 이는 일본의 폐경 전 여성들인 경우 니아신 섭취량은 골밀도에 긍정적인 영향을 나타내었다고 한 Sasaki S & Yanagibori R(2001)의 보고와 같은 경향이었다. 비타민 B6는 콜라겐의 교차결합(Cross- linking) 형성에 필수적인 Lysyloxidase의 Cofactor 및 Alkaline phosphatase의 기질로서 골격형성에 관여한다고 하였다(Masse PG 등 1996). Yazdanpanah N 등(2007)은 비타민 B6의 섭취량이 부족한 노인들은 골밀도가 낮고 골절의 위험이 크다고 보고한 바 있는데, 이는 비타민 B6의 섭취량이 골밀도에 유의한 영향을 나타내지 않았던 본 조사 대상 폐경 여성들과는 차이가 있었다.
이상에서 살펴 본 바와 같이 폐경 전 여성들인 경우 총단백질, 동물성 단백질, 비타민 K, 티아민, 리보플라빈, 니아신, 비타민 B6, 칼륨 및 셀레늄 등의 섭취량은 골밀도에 긍정적인 연관성을 나타내었으나, 식물성 단백질 섭취량은 오히려 부정적인 연관성을 나타내었다. 폐경 후 여성들인 경우에는 동물성 단백질, 비타민 D, 비타민 K 및 티아민 등의 섭취량은 골밀도에 긍정적인 연관성을 나타내었으나, 식물성 단백질 섭취량은 폐경 전 여성들과 마찬가지로 부정적인 연관성을 나타내었다. 폐경 전·후 여성들의 골밀도에 공통적으로 긍정적인 연관성을 나타낸 영양소는 동물성 단백질, 비타민 K 및 티아민이었고, 부정적인 연관성을 나타낸 영양소는 식물성 단백질로 조사되었다. 그리고 본 연구 결과에서 여성들의 골밀도는 폐경 전이 폐경 후에 비해 영양소 섭취량과 연관성이 더 큰 것으로 추측할 수 있었다.
Table 4는 대상자들의 영양소 섭취비율을 나타낸 것이다. 폐경 전·후 여성들 모두 동물성/식물성 단백질 섭취비율은 정상군이 위험군에 비해 유의하게 높았다(p<0.05). 칼슘/인 섭취비율은 폐경 후 여성들에게만 정상군이 위험군에 비해 유의하게 높게 나타났다. Weikert C 등(2005)도 골격 건강을 유지하기 위해서는 동물성/식물성 단백질의 섭취비율이 매우 중요하다고 하였다. 또한 동물성 단백질을 섭취하지 않는 채식주의자는 채식주의자가 아닌 사람들에 비해 대퇴골밀도가 약 4% 감소되었다고 한(Ho-Pham LT 등 2009) 반면, 동물성/식물성 단백질의 높은 섭취비율은 골 건강에 부정적인 영향을 준다고 보고된 바 있다(Massey LK 2003). 칼슘/인의 낮은 섭취비율은 PTH 분비와 골 흡수를 촉진하여 골 건강에 부정적인 영향을 나타내며, 특히 칼슘/인의 섭취비율이 0.5 이하가 되면 골격 건강에 악영향을 가져온다고 하였다(Kim WY 1994). 본 조사대상 여성들인 경우 칼슘/인의 섭취비율은 폐경 유무와 상관없이 위험군은 모두 0.5 이하로 나타나 상당한 문제로 보여진다.
4. 골밀도와 연령, 신체계측치 및 영양소 섭취량과의 상관성
Table 5는 연령 및 신체계측치들과 요추 및 대퇴골밀도와의 상관성을 나타낸 것이다. 먼저 연령과 골밀도와의 상관성을 살펴보면, 연령은 폐경 전 여성들인 경우 요추 및 대퇴골밀도와 유의하게 양의 상관성(p<0.05)을 나타낸 반면, 폐경 후 여성들인 경우에는 대퇴골밀도와 유의하게 음의 상관성(p<0.05)을 나타내었다. 이는 폐경 전 여성들인 경우 연령이 높을수록 골밀도가 높다고 한 Kim MS & Koo JO(2008)의 보고 및 폐경 후 여성들인 경우 연령이 높을수록 골밀도가 낮다고 한 Oh SI 등(2002)의 보고와 같은 경향이었다. 이는 연령이 낮은 20~30대 여성들인 경우 오히려 불규칙적인 식습관과 운동 습관을 갖고 있을 우려가 크기 때문일 것으로 추측된다.
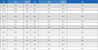
Correlation coefficients between bone mineral density and, age and anthropometric factors of the subjects
신체계측치와 골밀도와의 상관성에 있어 요추골밀도는 폐경 전 여성들인 경우에는 신장(p<0.01), 체중(p<0.05) 및 LBM(p<0.01)과 유의하게 양의 상관성을 나타내었으나, 폐경 후 여성들인 경우는 어떤 지수와도 유의한 상관성을 나타내지 않아 폐경에 따른 현저한 차이를 나타내었다. 대퇴골밀도는 폐경 전 여성들인 경우 체중(p<0.01), BFM(p<0.05), BMI(p<0.05) 및 WHR(p<0.05)과 유의하게 양의 상관성을 나타내었다. 폐경 후 여성들의 대퇴골밀도도 폐경 전 여성들과 마찬가지로 체중(p<0.05), BFM(p<0.05), BMI(p<0.01) 및 WHR(p<0.01)과는 유의하게 양의 상관성을 나타내었다. 이상에서의 결과로 보아 폐경 후 여성들의 요추골밀도는 폐경 전 여성들과는 달리 신체계측치와의 연관성이 없었고, 대퇴골밀도는 폐경 전 여성들에 비해 BMI 및 WHR과의 연관성이 더 큰 것으로 추측된다.
본 조사 결과를 다른 선행 연구들과 비교해 보면 여성들의 요추골밀도와 체중과의 상관성은 폐경 전 여성들이 폐경 후 여성들에 비해 낮았다는 보고(Han JH & Cho KH 2002)와는 상반되었다. 반면, 폐경 전 여성들인 경우 요추골밀도는 신장(Oh SI 등 2003), 신장 및 체중(Kim KR 등 2000), LBM(Wang MC 등 2005) 등과 유의하게 양의 상관성을 나타내었다는 보고들과는 같은 경향이었다. 그리고 폐경 전 여성에게 있어 LBM(Lu LJW 등 2009) 및 BMI(Chan R 등 2009)가 골밀도와 연관성을 나타내는 가장 중요한 인자라고 보고된 바 있다. 한편, 폐경 후 여성들의 요추골밀도는 어떤 신체계측치와도 유의한 상관성을 나타내지 않았는데, 이는 폐경 후 여성들의 요추골밀도는 신장 및 체중(Desimone DP 등 1989), 그리고 신장, 체중 및 BMI(Oh SI 등 2002)와 유의하게 양의 상관성을 나타내었다는 보고들과는 상당한 차이가 있었다. 대퇴골밀도와 신체계측치와의 상관성을 살펴보면 본 조사 여성들의 대퇴골밀도는 폐경 유무와는 상관없이 체중, BFM, BMI 및 WHR과 양의 상관성을 나타내었다. 이는 대퇴 골밀도는 BMI와 유의하게 양의 상관성을 나타내었던 여대생들(Song YJ & Paik HY 2002), 체중 및 BMI와는 양의 상관성을 나타내었던 폐경 후 여성들(Oh SI 등 2002)과 같은 경향이었다. 그리고 신체계측치 중 본 조사 여성들의 골밀도와 상관성이 가장 큰 것은 체중으로 나타났는데, 이는 중국계 미국 여성들(Walker MD 등 2007)과도 같은 결과였다. 체중은 골량을 결정하는 잠재적 요인으로 체중이 많을수록 골조직에 가해지는 무게가 증가하므로 즉, 기계적 부하에 의해 골밀도 유지에 도움이 되며, 체중이 실리는 요추 및 대퇴골밀도에 영향을 미치게 된다고 하였다(Wee J 등 2013). 한편, Reid IR(2002)은 폐경 후 여성에게 있어 지방조직은 에스트로겐을 생성하는 주요 조직이기 때문에 BFM은 골밀도에 영향을 미치는 주요 인자라고 하였는데, 본 폐경 여성들도 BFM은 대퇴골밀도와 유의한 양의 상관성을 나타내었다. 하지만 Zhao LJ 등(2007)은 중국인과 서구인을 대상으로 한 연구에서 같은 체중을 가진 경우 체지방률이 높아질수록 오히려 골밀도가 감소하였다고 보고한 바 있다.
Table 6은 열량 및 영양소 섭취량과 요추 및 대퇴골밀도와의 상관성을 나타낸 것이다. 폐경 전 여성들의 요추골밀도는 열량(p<0.05), 비타민 K(p<0.05), 티아민(p<0.05), 리보플라빈(p<0.05), 니아신(p<0.01), 엽산(p<0.05) 및 마그네슘(p<0.05) 등의 섭취량과 유의하게 양의 상관성을 나타낸 반면 나트륨 섭취량(p<0.05)과는 유의하게 음의 상관성을 나타내었다. 대퇴골밀도는 니아신 및 비타민 B6 섭취량과 유의하게 양의 상관성(p<0.05)을 나타내었다. 폐경 후 여성들인 경우에는 요추골밀도는 어떤 영양소 섭취량과도 유의한 상관성을 나타내지 않았고, 대퇴골밀도는 비타민 D 및 마그네슘 섭취량과 유의하게 양의 상관성을 나타내었다(p<0.05).
영양소 섭취량과 골밀도와의 상관성에 대한 연구는 주로 칼슘과 비타민 D에 관한 것이었다. 특히 칼슘은 골격에 존재하는 가장 풍부한 무기질로 골 건강을 위해서는 필수적인 영양소로 알려져 있다(Almeida SG 등 2011). 하지만 본 연구에서는 폐경 유무와 상관없이 칼슘 섭취량은 여성들의 골밀도와 유의한 상관성을 나타내지 않았는데, 이는 칼슘 섭취량은 골밀도와 유의한 상관성을 나타내지 않았다고 한 Sowers MR 등(1992) 및 Vannucci L 등(2017)의 보고와 일치하였다.
티아민, 리보플라빈, 니아신, 비타민 B6 및 엽산 등의 비타민 B군 섭취량은 폐경 전 여성들의 골밀도와 유의한 양의 상관성을 나타내었다. 비타민 B군과 골밀도와의 상관성에 관한 기전은 아직 명확하게 밝혀진 바가 없으며, 티아민, 리보플라빈 및 니아신은 에너지 대사와 신경계 기능유지에 필요하다고 알려져 있다(Dai Z & Koh WP 2015). 리보플라빈은 골세포의 에너지 생성에 관여하는 효소의 Cofactor로 작용하며, 리보플라빈 섭취량이 가장 적은 여성들의 요추 및 대퇴골밀도가 가장 낮았다고 하였다(Abrahamsen, B 등 2005). 니아신은 골세포의 DNA 합성과 분화, 골세포로의 칼슘 이동에 관여하는 것으로 알려져 있으며, Sasaki S & Yanagibori R(2001)도 일본 폐경 전 여성들의 니아신 섭취량은 골밀도와 유의한 양의 상관성은 나타내었다고 하였다. 비타민 B6는 앞에서 언급하였듯이 콜라겐과 Alkaline phosphatase의 형성에 관여하여 골 건강에 도움이 된다고 알려져 있다. 그리고 엽산은 비타민 B6 및 비타민 B12와 함께 파골세포에서의 골흡수를 자극하는 호모시스테인의 수준을 감소시켜 골 건강에 도움이 되는 것으로 보고되어 있다(Herrmann M 등 2007). 비타민 K 섭취량도 요추골밀도와 유의한 양의 상관성을 나타내었는데, 이는 젊은 여성들의 골밀도는 비타민 K 섭취량과 유의한 양의 상관성을 나타내었다고 한 보고들(Booth SL 등 2003; Kim MS 등 2010)과 같은 경향이었다.
나트륨 섭취량은 골밀도와 유의한 음의 상관성을 나타내었는데, 이는 나트륨 섭취량은 요 중 칼슘 배설량을 증가시켜 여성들의 골밀도와 유의한 음의 상관성을 나타내었다고 한 보고들(Woo J 등 2009; Yoon JS & Lee MJ 2013)과 같은 경향이었다. 반면에 나트륨 섭취량은 여성들의 골밀도와 유의한 상관성이 없었다는 보고 (Carbone L 등 2016)도 있어 짜게 먹는 한국인들의 식습관으로 볼 때 이들 관련성에 대한 연구가 보다 심도 있게 이루어져야 할 것으로 사료된다.
한편, 폐경 후 여성들의 영양소 섭취량과 골밀도와의 상관성에 대한 연구를 살펴보면 총 골밀도 및 요추골밀도는 비타민 D 섭취량과 양의 상관성을 나타내었다는 보고(Kim MY 등 2016)와 더불어 골밀도는 칼륨 및 마그네슘 섭취량과 유의한 양의 상관성을 나타내었다(Sasaki S & Yanagibori R 2001; Booth SL 등 2003)는 보고 등이 있다. 비타민 D는 소장에서 칼슘 결합단백질을 합성해 칼슘 흡수를 증가시키는 역할을 하므로 비타민 D가 부족하면 칼슘 흡수가 저하되고, 그로 인해 이차적으로 PTH의 기능이 항진되어 골밀도 저하의 위험성이 높아진다고 알려져 있다(Adams JS 등 1999). 마그네슘이 많이 함유되어 있는 식품은 칼륨도 많이 함유되어 있을 가능성이 크고, 마그네슘 섭취량은 골밀도와 양의 상관성을 나타내었다고 하였다(Ryder KM 등 2005). New SA 등(2000)도 폐경 후 여성들인 경우 마그네슘 섭취 부족은 급속한 골 손실을 가져와 골밀도를 저하시킨다고 하였다. 이와는 달리 Oh SI 등(2002)은 폐경 후 여성들의 골밀도는 영양소 섭취량과 유의한 상관성이 없었다고 보고한 바 있다. 본 조사 여성들의 영양소 섭취량과 골밀도와의 상관성 또한 폐경 전이 폐경 후에 비해 더 크다는 것을 추측할 수 있었다. 또한 폐경 전 여성들인 경우 골밀도와 다양한 영양소 섭취량과의 관계를 연구할 필요가 있다고 사료된다.
요약 및 결론
폐경 전·후 여성들 각각 50명씩 총100명을 대상으로 골밀도에 따라 정상군과 위험군으로 나누어 신체계측치 및 영양소 섭취량을 분석·비교한 결과는 다음과 같다.
- 1. 요추골밀도의 T-score는 폐경 전 여성들이 폐경 후 여성들에 비해 높았다.
- 2. 신장, 체중, BFM, LBM, BMI 및 BMR은 폐경 전 여성들인 경우 정상군이 위험군에 비해 유의하게 많았다.
- 3. 폐경 전 여성들은 정상군이 위험군에 비해 총단백질, 동물성단백질, 비타민 K, 티아민, 리보플라빈, 나이아신, 비타민 B6, 칼륨 및 셀레늄 섭취량과 동물성/식물성 단백질 섭취비율이 유의하게 많았다. 폐경 후 여성들은 정상군이 위험군에 비해 동물성 단백질, 비타민 D, 비타민 K 및 티아민 섭취량과 동물성/식물성 단백질 및 칼슘/인 섭취비율 등이 유의하게 많았다. 식물성단백질 섭취량은 폐경 전·후 여성들 모두 정상군이 위험군에 비해 유의하게 적었다.
- 4. 폐경 전 여성들인 경우 요추골밀도는 연령, 신장, 체중, LBM 및 TBF와 유의한 양의 상관성을 나타내었으며, 대퇴골밀도는 연령, 체중, BFM, BMI 및 WHR과 유의한 양의 상관성을 나타내었다. 폐경 후 여성들인 경우 요추골밀도는 연령 과 유의한 음의 상관성을 나타내었으며, 대퇴골밀도는 체중, BFM, BMI 및 WHR과 유의한 양의 상관성을 나타내었다.
- 5. 폐경 전 여성들인 경우 요추골밀도는 열량, 비타민 K, 티아민, 리보플라빈, 니아신, 엽산 및 마그네슘 섭취량과는 유의하게 양의 상관성을 나타낸 반면, 나트륨 섭취량과는 유의하게 음의 상관성을 나타내었다. 대퇴골밀도는 니아신 및 비타민 B6 섭취량과 유의하게 양의 상관성을 나타내었다. 폐경 후 여성들인 경우 대퇴골밀도는 비타민 D 및 마그네슘 섭취량과 유의하게 양의 상관성을 나타내었다.
이상에서의 결과로 보아 골밀도에 영향을 미치는 요인으로 신체계측치 및 영양소 섭취량은 폐경 후 여성들에 비해 폐경 전 여성들에게 더 크게 영향을 미치는 것으로 나타났다. 또한 신체계측치 및 영양소 섭취량은 폐경 전 여성들인 경우에는 요추 골밀도에, 폐경 후 여성들인 경우에는 대퇴골밀도에 더 크게 상관성을 나타내었다. 영양소 중 비타민 D, 비타민 K, 티아민, 리보플라빈, 니아신, 비타민 B6, 엽산 및 마그네슘이 골밀도와 상관성이 높은 것으로 나타났다. 따라서 노년기의 골 건강을 위해서 이들 영양소의 충분한 섭취는 폐경 이전부터 중요하며, 체중이 골밀도와 상관성을 나타내는 만큼 적절한 체중유지가 필요하고 나트륨 섭취는 줄여야 할 것으로 추측할 수 있었다.
본 연구에서는 여성들의 골밀도에 영향을 미치는 요인으로 인구사회학적인 특성이 조사에서 제외되어 비교할 수 없었다는 점과 식이요인으로는 영양소 섭취량 조사에만 국한되어 전반적인 식생활과의 관련성, 특히 여성들의 평소 식품섭취패턴과 골밀도와의 관련성을 파악하여 비교하지 못한 것은 큰 제한점으로 생각된다. 따라서 향후에는 식품섭취빈도조사를 통한 식품섭취패턴과 더불어 인구사회학적인 특성이 폐경 전후 여성들의 골밀도에 어떤 영향을 미치는지에 대한 비교연구가 더 필요할 것으로 사료된다.
References
-
Abrahamsen, B, Madsen, JS, Tofteng, CL, Stilgren, L, Bladbjerg, EM, Kristensen, SR, Brixen, K, Mosekilde, L, (2005), Are effects of mthfr (C677T) genotype on BMD confined to women with low folate and riboflavin intake? Analysis of food records from the Danish osteoporosis prevention study, Bone, 36(3), p577-583.
[https://doi.org/10.1016/j.bone.2004.12.014]

-
Adams, JS, Kantorovich, V, Wu, C, Javanbakht, M, Hollis, BW, (1999), Resolution of vitamin D insufficiency in osteopenic patients results in rapid recovery of bone mineral density, J Clin Endocrinol Metab, 84(8), p2729-2730.
[https://doi.org/10.1210/jc.84.8.2729]

- Almeida SG, Monte LM, Garcia PPC (2011) Biodisponibilidade de cálcio numa dieta isenta de leite de vaca ederivados. Ensaios Ciênc 15(3): 147-158.
- Andon, MB, Smith, KT, Bracker, M, Statoris, D, Saltman, P, Strause, L, (1991), Spinal bone density and Ca intake in healthy postmenopausal women, Am J Clin Nutr, 54(5), p927-929.
-
Beasley, JM, Lacroix, AZ, Larson, JC, Huang, Y, Neuhouser, ML, Tinker, LF, Jackson, R, Snetselaar, L, Johnson, KC, Eaton, CB, Prentice, RL, (2014), Biomarker-calibrated protein intake and bone health in the women’s health initiative clinical trials and observational study, Am J Clin Nutr, 99(4), p934-940.
[https://doi.org/10.3945/ajcn.113.076786]

-
Bhupathiraju, SN, Dawson-Hughes, B, Hannan, MT, Lichtenstein, AH, Tucker, KL, (2011), Centrally located body fat is associated with lower bone mineral density in older Puerto Rican adults, Am J Clin Nutr, 94(4), p1063-1070.
[https://doi.org/10.3945/ajcn.111.016030]

-
Binkley, NC, Suttie, JW, (1995), Vitamin K nutrition and osteoporosis, J Nutr, 125(7), p1812-1821.
[https://doi.org/10.1093/jn/125.7.1812]

- Booth, SL, Tucker, KL, Chen, H, Hannan, MT, Gagnon, DR, Cupples, LA, Wilson, PW, Ordovas, J, Schaefer, EJ, Dawson-Hughes, B, Kiel, DP, (2003), Dietary vitamin K intakes are associated with hip fracture but not with bone mineral density in elderly men and women, Am J Clin Nutr, 77(2), p512-516.
- Calvo, MS, (1994), The effect of high phosphorus intake on calcium homeostasis, Adv Nutr Res, 9, p183-207.
-
Carbone, L, Johnson, KC, Huang, Y, Pettinger, M, Thomas, F, Cauley, J, Crandall, C, Tinker, L, LeBoff, MS, Wactawski-Wende, J, Bethel, M, Li, W, Prentice, R, (2016), Sodium intake and osteoporosis; Findings from the women's health nitiative, J Clin Endocrinol Metab, 101(4), p1414-1421.
[https://doi.org/10.1210/jc.2015-4017]

-
Cashman, KD, (2007), Diet, nutrition, and bone health, J Nutr, 137(11 Suppl), p2507S-2512S.
[https://doi.org/10.1093/jn/137.11.2507s]

-
Chan, R, Woo, J, Lau, W, Leung, J, Xu, L, Zhao, X, Yu, W, Lau, E, Pocock, N, (2009), Effects of lifestyle and diet on bone health in young adults Chinese women living in Hong Kong and Beijing, Food and Nutrition Bulletin, 30(4), p370-328.
[https://doi.org/10.1177/156482650903000408]

-
Choi, MJ, Park, EJ, Jo, HJ, (2007), Relationship of nutrient intakes and bone mineral density of elderly women in Daegu, Korea, Nutr Res and Pratice, 1(4), p328-334.
[https://doi.org/10.4162/nrp.2007.1.4.328]

- Chung YJ, Lee KM, Park JW, Chung SP (2001) Factors which are related with BMD in premenopausal women. J Korean Acad Fam Med 22(3): 363-370.
-
Dai, Z, Koh, WP, (2015), B-vitamins and bone health: Review of the current evidence, Nutrients, 7(5), p3332-3346.
[https://doi.org/10.3390/nu7053322]

-
Dawson-Hughes, B, Heaney, RP, Holick, MF, Lips, P, Meunier, PJ, Vieth, R, (2005), Estimates of optimal vitamin D status, Osteoporosis, 16(7), p713-716.
[https://doi.org/10.1007/s00198-005-1867-7]

- Desimone, DP, Stevens, J, Edwards, J, (1989), Influence of body and race on bone mineral density of the mid-radius hip, J Bone Miner Res, 4(6), p827-930.
- Han, JH, Cho, KH, (2002), Correlation between body composition and spinal bone density in young women, J Korean Acad Fam Med, 23(2), p215-223.
- Heaney, RP, Abrams, S, Dawson-Hughes, B, Looker, A, Marcus, R, Matkovic, V, Weaver, C, (2000), Peak bone mass, Osteoporosis, 11(12), p985-1009.
-
Herrmann, M, Schmidt, J, Umanskaya, N, Colaianni, G, Al Marrawi, F, Widmann, T, Zallone, A, Wildemann, B, Herrmann, W, (2007), Stimulation of osteoclast activity by low B-vitamin concentrations, Bone, 41(4), p584-591.
[https://doi.org/10.1016/j.bone.2007.06.005]

- Holroyd, C, Cooper, C, Dennison, E, (2008), Epidemiology of osteoporosis, Best Pract Res Clin Endocrinol Metab, 22(5), p671-685.
-
Ho-Pham, LT, Nguyen, ND, Nguyen, TV, (2009), Effect of vegetarian diets on bone mineral density: A Bayesian meta-analysis, Am J Nutr, 90(4), p943-950.
[https://doi.org/10.3945/ajcn.2009.27521]

-
Ilich, JZ, Brownbill, RA, Tamborini, L, (2003), Bone and nutrition in elderly women: Protein, energy, and calcium as main determinants of bone mineral density, Eur J Clin Nutr, 57(4), p564-565.
[https://doi.org/10.1038/sj.ejcn.1601577]

-
Ilich, JZ, Kerstetter, JE, (2000), Nutrition in bone health revisited: A study beyond calcium, Am J Clin Nutr, 19(6), p715-737.
[https://doi.org/10.1080/07315724.2000.10718070]

-
Jesudason, D, Clifton, P, (2011), The interaction between dietary protein and bone health, J Bone Miner Metab, 29(1), p1-14.
[https://doi.org/10.1007/s00774-010-0225-9]

- Kerstetter, JE, Allen, LH, (1994), Protein intake and calcium homeostasis, Adv Nutr Res, 9, p167-181.
- Kim, JS, Kim, JH, Yoo, JH, Park, JH, (2011), Association of dietary factors with osteoporosis in postmenopausal women, Korean Soc Osteoporosis, 9(1), p80-88.
- Kim, KR, Kim, KH, Lee, EK, (2000), A study on the factors affecting bone mineral density in adult women-based on the mothers of elementary school students, Korean J Nutr, 33(3), p241-249.
-
Kim, MS, Kim, HS, Sohn, CM, (2010), Relationship between vitamin K status, bone mineral density, and hs-CRP in young Korean women, Nutr Res Pract, 4(6), p507-514.
[https://doi.org/10.4162/nrp.2010.4.6.507]

- Kim, MS, Koo, JO, (2007), Analysis of factors affecting bone mineral density with different age among adult women in Seoul area, Korean J Comm Nutr, 12(5), p559-568.
- Kim, MS, Koo, JO, (2008), Comparative analysis of food habits and bone density risk factors between normal and risk women living in the Seoul area, Korean J Comm Nutr, 13(1), p125-133.
-
Kim, MY, Kim, MJ, Ly, SY, (2016), Vitamin D intake, serum 25OHD, and bone mineral density of Korean adults: Based on the Korea National Health and Nutrition Examination Survey (KNHANES, 2011), J Nutr Health, 49(6), p437-446.
[https://doi.org/10.4163/jnh.2016.49.6.437]

- Kim, WY, (1994), Osteoporosis dietary factors, Korean J Nutr, 27(6), p636-645.
- Koo, JO, Ahn, HS, Yoo, SY, (2008), Study of bone mineral density, body composition and dietary habits of 20~30 years old women, Korean J Comm Nutr, 13(4), p489-498.
- Koo, JO, Kwak, CS, Choi, HM, (1991), Effects of dietary protein levels and sources on calcium and phosphorus metabolism in young Korean women, Korean J Nutr, 24(2), p124-131.
- Korea Centers for Disease Control and Prevention, (2013), The Fourth Korea National Health and Nutrition Examination Survey (KNHANES IV-2), Seoul.
-
Langlois, JA, Mussolino, ME, Visser, M, Looker, AC, Harris, T, Madans, J, (2001), Weight loss from maximum body weight among middle-aged and older white women and the risk of hip fracture: The Nhanes I epidemiologic follow-up study, Osteoporosis Int, 12(9), p763-768.
[https://doi.org/10.1007/s001980170053]

- Lee, JS, Yu, CH, Chung, CE, (2006), Relation between milk consumption and bone mineral density of female college students in Korea, Korean J Nutr, 39(5), p451-459.
- Lee, JS, Jang, SG, (2013), A study on reference values and prevalence osteoporosis in Korea: The Korea National Health and Nutrition Examination Survey 2008~2011, J Korean Official Statistics, 18(2), p42-65.
- Lee, YS, Leem, HS, Aha, HS, Jang, NS, (2005), Nutrition throughout the Life Cycle, Kyomunsa, Seoul, Korea, p262-263.
- Lim, JH, Bae, HS, Lee, SM, Ahn, HS, (2008), Dietary and non-dietary factors related to bone mineral density in female college stidents, Korean J Comm Nutr, 13(3), p418-425.
-
Lu, LJW, Nayeem, F, Anderson, KE, Grady, JJ, Nagamani, M, (2009), Lean body mass, not estrogen or progesterone, predicts peak bone mineral density in premenopausal women, J Nutr, 139(2), p250-256.
[https://doi.org/10.3945/jn.108.098954]

- Macdonald, HM, New, SA, Fraser, WD, Campbell, MK, Reid, DM, (2005), Low potassium intakes and high dietary estimates of net endogenous and production are associated with low BMD in premenopausal women and increased markers of bone resorption in postmenopausal women, Am J Clin Nutr, 81(4), p923-933.
-
Masse, PG, Rimnac, CM, Yamauchi, M, Coburn, SP, Rucker, RB, Howell, DS, Boskey, AL, (1996), Pyridoxine deficiency affects biomechanical properties of chick tibial bone, Bone, 18(6), p567-574.
[https://doi.org/10.1016/8756-3282(96)00072-5]

-
Massey, LK, (2003), Dietary animal and plant protein and human bone health: A whole foods approach, J Nutr, 133(3), p862s-865s.
[https://doi.org/10.1093/jn/133.3.862s]

-
New, SA, Robins, SP, Campbell, MK, Martin, JC, Garton, MJ, Bolton-Smith, C, Grubb, DA, Lee, SJ, Reid, DM, (2000), Dietary influences on bone mass and bone metabolism: Further evidence of a positive link between fruit and vegetable consumption and bone health?, Am J Clin Nutr, 71(1), p142-151.
[https://doi.org/10.1093/ajcn/71.1.142]

- Oh, SI, Lee, HS, Lee, MS, Kim, CI, Kwon, IS, Park, SC, (2002), Some Factors affecting bone mineral status of postmenopausal women, Korean J Comm Nutr, 7(1), p121-129.
- Oh, SI, Lee, HS, Lee, MS, Kim, CI, Kwon, IS, Park, SC, (2003), Factors affecting bone mineral status of premenopausal women, Korean J Comm Nutr, 8(6), p927-937.
-
Orchard, TS, Larson, JC, Alghothani, N, Bout-Tabaku, S, Cauley, JA, Chen, Z, LaCroix, AZ, Wactawski-Wende, J, Jackson, RD, (2014), Magnesium intake, bone mineral density and fractures: Results from the Women’s Health Initiative Observational Study, Am J Clin Nutr, 99(4), p926-933.
[https://doi.org/10.3945/ajcn.113.067488]

-
Paddon-Jones, D, Rasmussen, BB, (2009), Dietary protein recommendations and the prevention of sarcopenia, Curr Opin Clin Nutr Metab Care, 12(1), p86-90.
[https://doi.org/10.1097/mco.0b013e32831cef8b]

-
Park, JY, Choi, MY, Lee, SH, Choi, YH, Park, YK, (2011), The association between bone mineral density, bone turnover markers, and nutrient intake in pre- and postmenopausal women, Korean J Nutr, 44(1), p29-40.
[https://doi.org/10.4163/kjn.2011.44.1.29]

-
Promislow, J, Goodman-Gruen, D, Slymen, DJ, Barrett-Connor, E, (2002), Protein consumption and bone mineral density in the elderly: The rancho bernardo study, Am J Epidemiol, 155(7), p636-644.
[https://doi.org/10.1093/aje/155.7.636]

- Reid, IR, (2002), Relationships among body mass, its components, and bone, Bone, 31(5), p547-555.
- Reidt, CS, Cifuentes, M, Stahl, T, Chowdhury, HA, Schlussel, Y, Shapses, SA, (2005), Overweight postmenopausal women lose bone with moderate weight reduction and 1 g/day calcium intake, J Bone Miner Res, 20(3), p455-463.
- Riggs, BL, Khosla, S, Melton, LJ 3rd, (1998), A unitary model for involutional osteoporosis: Estrogen deficiency causes both type Ⅰand type Ⅱ osteoporosis in postmenopausal women and contributes to bone loss in aging men, J Bone Miner Res, 13(5), p763-773.
-
Ryder, KM, Shorr, RI, Bush, AJ, Kritchevsky, SB, Harris, T, Stone, K, Cauley, J, Tylavsky, FA, (2005), Magnesium intake from food and supplements is associated with bone mineral density in healthy older white subjects, J Am Geriatr Soc, 53(11), p1875-1880.
[https://doi.org/10.1111/j.1532-5415.2005.53561.x]

-
Sasaki, S, Yanagibori, R, (2001), Association between current nutrient intakes and bone mineral density at calcaneus in pre- and postmenopausal Japanese women, J Nutr Sci Vitaminol, 47(4), p289-294.
[https://doi.org/10.3177/jnsv.47.289]

- Shapes, SA, Reidt, CS, (2006), Bone, body weight, and weight reduction: What are the concerns?, J Nutr, 136(6), p1453-1456.
-
Shen, CL, Chyu, MC, Wang, JS, (2013), Tea and bone health: Steps forward in translational nutrition, Am J Clin Nutr, 98(suppl), p1694s-1699s.
[https://doi.org/10.3945/ajcn.113.058255]

- Song, YJ, Paik, HY, (2002), Effect of dietary factors on bone mineral density in Korean college women, Korean J Nutr, 35(4), p464-472.
- Sowers, MR, Clark, MK, Hollis, B, (1992), Radial bone mineral density in pre- and postmenopausal women: A prospective study of rates and risk factors for loss, J Bone Mine Res, 7(6), p647-657.
-
Thorpe, MP, Evans, EM, (2011), Dietary protein and bone health: Harmonizing conflicting theories, Nutr Rev, 69(4), p215-230.
[https://doi.org/10.1111/j.1753-4887.2011.00379.x]

-
Vannucci, L, Masi, L, Gronchi, G, Fossi, C, Carossino, AM, Brandi, ML, (2017), Calcium intake, bone mineral density, and fragility fractures: Evidence from an Italian outpatient population, Arch Osteoporos, 12(1), 40.
[https://doi.org/10.1007/s11657-017-0333-4]

- Vermeer, C, Gijsbers, BLMG, Craciun, AM, Groenen-Van Dooren, MMCL, Knapen, MHJ, (1996), Effects of vitamin K on bone mass and bone metabolism, J Nutr, 126(4-suppl), p1187s-1192s.
-
Walker, MD, Babbar, R, Opotowsky, A, McMahon, DJ, Liu, G, Bilezikian, JP, (2007), Determinants of bone mineral density in Chinese-American women, Osteoporosis Int, 18(4), p471-478.
[https://doi.org/10.1007/s00198-006-0258-z]

-
Wang, MC, Bachrach, LK, Van Loan, M, Hudes, M, Flegal, KM, Crawford, PB, (2005), The relative contributions of lean tissue mass and fat mass to bone density in young women, Bone, 37(3), p474-481.
[https://doi.org/10.1016/j.bone.2005.04.038]

-
Wardlaw, GH, (1996), Putting body weight and osteoporosis into perspective, Am J Clin Nutr, 63(suppl), p433s-436s.
[https://doi.org/10.1093/ajcn/63.3.433]

-
Wee, J, Sng, BY, Shen, L, Lim, CT, Singh, G, Das De, S, (2013), The relationship between body mass index and physical activity levels in relation to bone mineral density in premenopausal and postmenopausal women, Arch Osteoporos, 8, 162, accessed on 26. 11. 2013.
[https://doi.org/10.1007/s11657-013-0162-z]

-
Weikert, C, Walter, D, Hoffmann, K, Kroke, A, Bergmann, MM, Boeing, H, (2005), The relation between dietary protein, calcium and bone health in women: Results from the EPIC-Potsdam cohort, Ann Nutr Metab, 49(5), p312-318.
[https://doi.org/10.1159/000087335]

- WHO Scientific Group on the Prevention and Management of Osteoporosis, (2000), Prevention and management of osteoporosis: Report of a WHO Scientific Group 2003, Geneva, Switzerland.
-
Woo, J, Kwok, T, Leung, J, Tang, N, (2009), Dietary intake, blood pressure and osteoporosis, J Hum Hypertens, 23(6), p451-455.
[https://doi.org/10.1038/jhh.2008.156]

- World Health Organization, (1994), Assessment of fracture risk and its application to screening for postmenopausal osteoporosis, WHO Technical Report Series, Geneva 843, p1-129.
-
Yazdanpanah, N, Zillikens, MC, Rivadeneira, F, De Jong, R, Lindemans, J, Uitterlinden, AG, Pols, HA, Van Meurs, JB, (2007), Effect of dietary B vitamins on BMD and risk of fracture in elderly men and women: The Rotterdam Study, Bone, 41(6), p987-994.
[https://doi.org/10.1016/j.bone.2007.08.021]

-
Yoon, JS, Lee, MJ, (2013), Calcium status and bone mineral density by the level of sodium intake in young women, Korean J Comm Nutr, 18(2), p125-133.
[https://doi.org/10.5720/kjcn.2013.18.2.125]

- Zhao, LJ, Liu, YJ, Liu, PY, Hamilton, J, Recker, RR, Deng, HW, (2007), Relationship of obesity with osteoporosis, J Clin Endocrinol Metab, 92(5), p1640-1646.
