
Aflatoxin 저감화 종균으로 제조한 고상종국의 품질특성
Abstract
We investigated the occurrence of aflatoxin B1 and the amylolytic and proteolytic activities of Aspergillus sp. (A. turbengensis OF5-8, A. oryzae OF5-18, A. oryzae IF18-2, and A. oryzae IF20-25) isolated from a Korean traditional Nuruk for preparation of solid fermented koji. The aflatoxin production of isolated Aspergillus sp. was 7 to 20-fold lower than that of the control A. flavus KACC 41862. The enzymatic activities of each fungal strain under each temperature condition (23℃, 25℃, and 28℃) were also measured. Higher α-amylase activities were observed for A. turbengensis OF5-8 and A. oryzae IF18-2 at 23℃ and 25℃, respectively. For the A. oryzae IF18-2 starter, the glucoamylase activity was maintained at a higher level at all fermentation temperatures. Enzyme activities in the solid fermented koji were also observed after treatment with varied inoculation rates (3%, 6%, and 10%) of liquid starter and the activities of α-amylase (825.3 units/g) and glucoamylase (2,107.3 units/g) in A. oryzae IF18-2 were found to be higher at the 3% inoculation rate. Finally, the enzymatic productivity of solid fermented koji made with A. oryzae IF18-2 was maintained at a higher level; therefore, it is expected to be useful as a fermentation agent or fermentation starter for Makgeolli in the future.
Keywords:
starter, enzymatic activity, Nuruk, aflatoxin, Makgeolli서 론
우리나라의 대표적 서민 주류인 막걸리는 2000년대에 후반을 기점으로 효모의 유산균 생존, 낮은 알코올 농도 등의 특성과 쌀을 주식으로 하는 유사한 문화 등으로 일본을 포함한 동남아시아 지역을 중심으로 각광받는 주류로서 재조명 되었다(Lee JH 등 2012). 그러나 최근 다양한 프리미엄급 주류의 등장과 소비형태의 변화로 급격히 감소하고 있는 것이 현실이다. 우리나라 전통 주류인 막걸리는 전분이 주성분인 곡류에 물과 누룩을 넣어 전분분해와 알코올 발효가 동시에 일어나는 전형적인 병행복발효로 빚는 술이다(So MH & Lee JW 1996). 누룩에는 다양한 종류의 미생물들이 있어 이들이 생산하는 전분질 및 단백질 분해효소, 알코올 발효능 및 유기산 생산 등의 차이가 있어 막걸리의 맛, 향, 색 등의 품질에도 차이가 나타난다(Woo SM 등 2010). 우리나라의 전통누룩에는 Aspergillus oryzae, Rhizopus oryzae, Monascus purpureus, Saccharomyces sp., lactic acid bacteria, Bacillus sp. 등의 다양한 미생물이 생육하고 있다. 특히, 이들 누룩에는 Aspergillus 속, Lichtheimia 속 및 Rhizopus 속 곰팡이가 많이 분포하고 있는 것이 우리 누룩의 가장 큰 특징이다 (Kim CJ 등 1990).
누룩에 생육하는 주요 곰팡이 중 발효과정에 핵심적인 역할을 하는 것은 Rhizopus sp., Aspergillus sp.가 있으며, 이들 곰팡이는 α-amylase, glucoamylase 등 전분을 분해하는 효소를 분비하여 곡류에 저장된 전분을 당화하는 역할을 한다(Kim CJ & Lee JS 1985). 곰팡이의 전분 당화능에 의해 생성된 당류는 효모에 의한 알코올 생산에 사용된다. 따라서 전분 분해능이 우수한 균주의 확보는 막걸리 및 전통주 생산에 매우 중요하다고 할 수 있다. 최근, 우리나라는 탁․약주 및 과실주 생산을 위해 외국에서 개발한 종균을 수입하는데 많은 비용을 지불하고 있다. 특히 국내 종균시장의 60%를 일본에서 수입하며, 연간 로열티는 120억 원 정도이다(Mun JY 등 2016). 따라서 수입 종균을 대체하기 위해 국산 토착 발효종균 발굴과 자원화와 더불어 종균제조기술 개발 또한 무엇보다도 절실히 필요하다(Jeon CO 2014). 최근까지 누룩 관련 연구는 주로 누룩에 서식하는 유용 곰팡이 및 효모 등의 균주 분리․동정에 관한 연구(Jo GY & Lee CW 1997; Lee SH 등 2004)와 시판누룩을 이용한 막걸리의 품질특성에 관한 연구(Woo SM 등 2010)로서 누룩의 전분질 원료에 대한 연구가 보고되었다. 실제로 누룩의 상용화를 목적으로 유용 발효종균을 이용한 새로운 발효제 제조 개발에 관한 연구는 거의 미비한 실정이다.
본 연구에서는 국내 전통누룩에서 분리한 곰팡이 A. turbengensis OF5-8 및 A. oryzae OF5-18, A. oryzae IF18-2, A. oryzae IF20-25를 이용하여 고상종국을 제조하였다. 이들의 당화력은 524.20±13.99∼2,107.32±88.30 units/g으로 Baek SY 등(2010)이 충청지역에서 수집한 누룩의 당화력 760∼1,400 units/g에 비하여 효소활성이 우수함을 보여줬다. 이러한 결과는 막걸리용 전분 분해력이 뛰어난 유용 발효 곰팡이 발굴과 이를 이용한 종균 및 종국 제조기술 개발로 나고야의정서 발효에 따른 국산 토착 발효종균 자원의 산업적 활용 가치를 높이고자 하였다.
재료 및 방법
1. 사용균주 및 원료
본 연구에 사용한 곰팡이 균주는 전통누룩에서 분리하여 농촌진흥청 발효가공식품과에서 보관 중인 4종류의 곰팡이(A. turbengensis OF5-8, A. oryzae OF5-18, A. oryzae IF18-2, A. oryzae IF20-25)를 사용하였다. 고상종국 제조에 사용된 원료는 2015년 경기도에서 생산된 추청미를 광천유통(Suwon, Korea)에서 구입하여 사용하였다.
2. Aflatoxin 정량분석
Aflatoxin(B1) 독성의 정량적인 분석을 진행하기 위하여 ELISA 분석을 진행하였다. 각각의 시료 5 g을 확보하기 위해, 밀기울(100 g), 물(30 mL)을 혼합하여 각각 동량의 곰팡이 포자수(106 cells/mL)를 접종한 뒤, 28℃로 조정된 정치 배양기 (H200-H-E, Benchmark Scientific, NJ, USA)에서 7일간 배양 하였다. ELISA 분석은 AOAC 인증을 받은 Veratox Aflatoxin total kit(Neogen, Lansing, USA)를 사용하였으며, 제조사가 제시한 조건으로 반응시킨 후, 650 nm의 흡광도(UV-2450, Shimadzu Co., Kyoto, Japan)에서 시료를 측정한 뒤, 4PL(Four parameter logistic curve-fit) 분석법을 이용해 검량선을 작성하여 정량적 분석을 진행하였다(Roman BE 등 2017).
3. 곰팡이 균주의 배양액
선발된 곰팡이 균주들은 YEPS(yeast extract 1%(v/w), peptone 2%(w/v), soluble starch 1%(w/v)) 배지에 동일한 포자수(106 cells/mL)로 접종하여 각각 온도별(23℃, 25℃, 28℃)로 조정된 진탕 배양기(VS-1203PF, Vision, Incheon, Korea)에 3일간 120 rpm으로 배양하였다. 배양액은 원심분리기(CR22GⅢ, Hitachi Co., Tokyo, Japan)를 이용하여 3,000 rpm, 10min, 4℃에서 침전물과 분리된 상등액을 회수하였다. 각각의 회수한 상등액은 효소활성 측정의 조효소액으로 사용하였다.
4. 액체종균제조
액체종균은 증류수 100 mL에 대한 무게 비율로 분쇄된 밀기울 5%(w/v)되게 첨가하여 121℃에서 20분간 고압멸균(DS-100A, Dasol, Gyeongi Korea)하였다. 선정한 4종류 곰팡이(A. turbengensis OF5-8 및 A. oryzae OF5-18, A. oryzae IF18-2, A. oryzae IF20-25)를 각각 동일한 포자수(108 cells/mL)로 접종하여 5일간, 28℃에서 배양하고 여과한 것을 액체종균으로 사용하였다.
5. 고상종국 제조
4종류의 곰팡이를 이용한 고상종국 제조는 위해 미생물등 잡균 오염을 방지하기 위하여 소형 제국기(Mini-15, Yaegaki Food Co., Hyogo, Japan)를 사용하였다. 먼저 쌀을 씻어 3시간 동안 침지한 후, 1시간 물 빼기를 하고, 110℃에서 50분간 증자한 후, 40℃가 되도록 냉각시켰다. 각각의 액체종균을 농도별로 접종하고, 40℃에서 제국하여 20시간 후에 1차 뒤집기를 하고, 배양 25시간째 뒤섞기를 하여 24시간 간격으로 확인하면서 곰팡이 포자를 충분히 형성한 후, 제국 8일에 출국하여 50℃에서 18시간 건조(DS-80-3, Dasol, Gyeongi Korea)하였다. 이때 액체종균을 쌀 중량(dry base)에 대하여 3, 6, 10%(v/w) 농도별로 접종하여 고상종국을 제조한 후, 이들의 품질특성을 비교하였다.
6. 효소활성 분석
효소활성은 시료 10 g에 0.5% NaCl, 10 mM 초산완충액 50 mL를 가하여 상온(25℃)에서 3시간 추출하고, 원심분리후, 0.45 μm 실린지 필터로 여과하여 각각의 효소활성(α-amylase 및 glucoamylase, acid carboxy peptidase)을 양조 분석용 Kit(Kikkoman Corp. Nod, Japan)로 측정하였다.
α-Amylase 활성은 시험관에 0.5 mL 기질용액(N3-G5-β-CNP)과 0.5 mL 효소용액(glucoamylase, β-glucosidase)을 분주하고, 37℃에서 약 5분간 예열하였다. 0.1 mL 시료를 넣고 잘 혼합한 후, 10분간 반응하였다. 반응 정지액(sodium carbonate)을 2 mL 넣고 반응을 종료한 후, 400 nm에서 흡광도(UV-2450, Shimadzu Co., Kyoto, Japan)를 측정하였다(Es). 공시험은 0.5mL 기질용액과 0.5 mL 효소 용액을 15분간 37℃에서 반응시킨 후, 반응 정지액(sodium carbonate)을 2 mL 첨가하여 잘혼합하고, 0.1 mL 측정시료를 첨가한 용액으로 400 nm에서 흡광도를 측정하였다(Eb). α-Amylase 활성은 다음과 같은 식에 의하여 계산되었다.
U(units/g) = (Es—Eb) × 0.179 × Df × 22.2 × 추출율
Es: 시료의 흡광도, Eb: 공시험 흡광도, Df: 시료 희석 배율.
Glucoamylase 활성은 시험관에 0.5 mL 기질용액(G2-β-PNP)과 0.5 mL 효소용액(β-glucosidase)을 분주하고, 37℃에서 약 5분간 예열하였다. 0.1 mL 시료를 혼합하여 10분간 반응시킨 후, 반응 정지액(sodium carbonate)을 2.0 mL 넣고 반응을 정지시킨 후, 흡광도 400 nm에서 측정하였다(Es). 공시험의 측정은 0.5 mL 기질용액(G2-β-PNP)과 0.5 mL 효소용액(β-glucosidase)을 37℃에서 약 15분간 예열 후, 반응 정지액 2.0 mL을 첨가하여 잘 혼합하고, 0.1 mL 측정시료를 첨가하여 다시 혼합하였다. 이 반응액을 400 nm에서 흡광도를 측정하였다(Eb). Glucoamylase 활성은 다음과 같은 식에 의하여 계산되었다.
U(units/g) = (Es—Eb) × 0.171 × Df × 144.6
Es: 시료의 흡광도, Eb: 공시험 흡광도, Df: 시료 희석 배율.
Acidic protease 활성은 시험관에 1.0 mL 기질용액(Cbz-Tyr-Ala + NAD + 초산 완충액)을 넣고 37℃에서 약 5분간 예열하였다. 0.1 mL의 시료를 혼합하여 10분간 반응시킨 후, 반응 정지액 2.0 mL를 첨가하여 5분간 예열한 후, 정량 효소액 0.1 mL을 넣고 37℃에서 20분간 정량반응을 실시하였다. 여기에 0.1 mL 정량 발색액(PMS)을 혼합하여 다시 10분간 반응을 계속하였다. 이 반응액을 흡광도(460 nm)에서 측정하였다(Es). 공시험 값의 측정은 상기 기질 용액을 37℃에서 15분간 반응 후, 반응 정지액 2.0 mL와 0.1 mL 시료를 넣고 이후의 반응은 효소 반응액과 동일하게 처리하여 반응액을 흡광도(460 nm)에서 측정하였다(Eb). 표준 값의 측정은 시료 대신 양조 분석 Kit의 표준액을 사용하고, 측정 절차는 공시험과 같이 실시하였다(Estd). 발색 공시험의 측정은 측정 시료 대신 증류수를 사용하고, 분석은 측정시료와 같이 실시하였다(Ec). Acidic protease 활성은 다음과 같은 식에 의하여 계산되었다.
U(units/g) = (Es—Eb) ÷ (Estd-Ec) × 0.1 × 희석배수 × 2,877.5 × 추출율
Es: 시료의 흡광도, Eb: 공시험 흡광도, Estd: 표준액의 흡광도, Ec: 발색 공시험의 흡광도, df: 시료 희석 배율.
1 U은 제시된 측정조건에서 1분간에 Cbz-Tyr-Ala에서 1μmol의 L-alanine을 분해하는 역가를 나타내었다.
7. 통계분석
모든 시료의 품질 특성 분석은 실험군의 오차를 줄이기 위해, 3회 반복하여 평균과 표준편차(IBM SPSS Statistics, USA)로 나타내었다. 통계처리는 분산분석(ANOVA)에 의해 검증하였으며, 유의성 비교는 Ducan’s multiple range test로 p<0.05 수준에서 검증하였다.
결과 및 고찰
1. Aflatoxin 생산능
분리한 4종류 곰팡이를 주류용 발효종균으로 사용하기 위한 안전성 평가는 각 곰팡이의 aflatoxin(B1) 생산능으로 평가하였다. 분리된 4종류 곰팡이들의 aflatoxin 생산 농도는 대조구로 사용한 aflatoxin 생산균인 A. flavus(KACC 41862)에 비해 7∼20배 낮은 유의적 차이(p<0.05)를 보였다(Fig. 1). 식품에서 허용하는 aflatoxin 농도는 5 ppb 이하로 규정(식약처 2016)되어 있으므로 4종류의 곰팡이는 식품에서 허용되는 범위 이내이므로 막걸리용 종균 및 발효제로 사용하여도 될 것이다. 특히, A. oryzae OF5-18는 1.0 ppb 이하의 아플라톡신을 생성함으로 식약처 기준치 이하로 주류제조의 안전성에 문제가 없는 것으로 확인되었다.
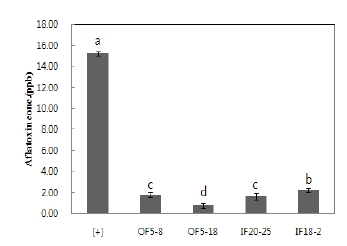
The quantitative concentration of aflatioxin.Data are presented as the mean for 3 independent experiments. Error bars indicate SD. Significance comparison was performed at Duncan’s multiple range test at p<0.05 level. Different letters were indicated with the statistical analysis according to fermentation temperature of each fungal strain. OF5-8, Nuruk of A. turbingensis KACC 93270P; OF5-18, Nuruk of A. oryzae KACC 93284P; IF20-25, nuruk of A. oryzae KACC 93286P; IF18-2, nuruk of A. oryzae KACC 93289P; (+), A. flavus KACC 41862.
2. 발효온도에 따른 효소활성
분리한 곰팡이 균주별 효소활성의 최적온도를 선정하기 위하여 서로 다른 발효 온도(23℃, 25℃, 및 28℃)에서 곰팡이 각각의 효소활성을 측정하였다(Fig. 2). A. oryzae OF5-8 균주의 α-amylase은 23℃에서 1.56±0.54(U/g protein)로 가장 높은 효소활성을 보였고, A. oryzae IF18-2 균주는 25℃에서 가장 높은 1.27±0.20(U/g protein)의 효소활성을 보였다(Fig. 2(A)). 한편, 28℃에서는 4종류 곰팡이들이 평균적으로 0.91±0.18(U/g protein)의 α-amylase 효소활성을 나타내었다. 전분분해능에서 단당류인 glucose를 생산하는데 직접적으로 작용하는 glucoamylase 효소활성은 Fig. 2(B)에 나타내었다. A. oryzae IF18-2 곰팡이 종균은 다른 균주들에 비해 모든 온도(23℃, 25℃, 및 28℃)영역에서 월등히 높은 효소활성 값(6.99±0.57 U/g protein)을 나타내기 때문에 A. oryzae OF5-8, A. oryzae OF5-18 및 A. oryzae IF20-25 종균들에 비해 산업적 가치가 높다고 여겨진다. 한편, A. oryzae IF20-25는 28℃에서 3.03±1.02 U/g protein의 당화력을 보임으로써 온도가 증가할수록 효소활성이 증가되기 때문에 다른 종균들에 비해 내열성이 우수한 균주로 판단된다. Fig. 2(C)에 나타낸 protease activity는 각각의 균주들의 온도에 따른 효소활성 값들에 큰 유의적 차이가 없었지만, A. oryzae IF18-2 균주의 28℃에서의 protease activity가 0.95±0.14 U/g protein으로 가장 낮았다. 주류 제조에 있어 높은 protease 효소활성 결과 값(Fig. 2(C))은 오히려 잡미, 텁텁함에 관여하는 부분이기 때문에(Park CS & Lee TS 2002; Jeong JH 등 2015) 단순히 효소활성이 높은 종균보다 α-amylase와 glucoamylase 효소활성이 우수한 반면 protease 활성이 낮은 황국균이 주류제조를 위한 종균으로 더 적합하다. 결과적으로 α-amylase와 glucoamylase 효소활성이 우수하고 protease 활성이 낮은 A. oryzae IF18-2 종균의 발효 특성을 잘 나타내주는 발효온도는 28℃로 판단되었다. 이를 바탕으로 고상종국을 제조하기 위해 접종할 액체종균은 28℃에서 배양되었다.
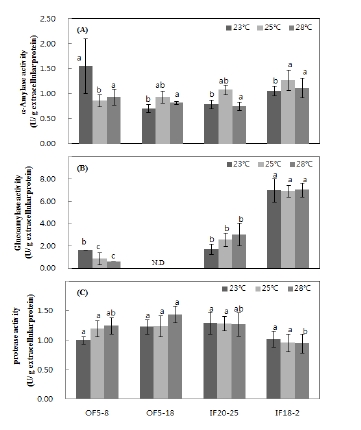
Enzyme activity of fungal strain isolated from nuruk.A shows the enzyme activity of α-amylase. B shows the enzyme activity of glucoamylase. C shows the enzyme activity of acidic protease. Data are presented as the mean for 3 independent experiments. Error bars indicate SD(p<0.05). Significance comparison was performed at Duncan’s multiple range test at p<0.05 level. Different letters were indicated with the statistical analysis according to fermentation temperature of each fungal strain. OF5-8, nuruk of A. turbingensis KACC 93270P; OF5-18, nuruk of A. oryzae KACC 93284P; IF20-25, nuruk of A. oryzae KACC 93286P; IF18-2, nuruk of A. oryzae KACC 93289P; ND, not detected.
3. 고상종국의 α-amylase 효소활성
곰팡이 종균별 고상종국을 제조하기 위해, 밀기울 배지에 배양한 액체종균을 농도별(3%, 6%, 및 10%)로 접종하여 고상종국을 제조한 후, 이들의 효소활성을 분석하였다. 곰팡이 종균별 고상종국의 α-amylase 활성 결과를 Fig. 3에 나타내었다. 전분의 액화제로 작용하는 α-amylase 활성은 곰팡이 종류에 따라 다른 양상을 나타내었다. A. oryzae IF20-25 액체종균을 농도별(3%, 6%, 및 10%)로 배양한 결과, 463.4±4.92 units/g, 526.0±73.76 units/g, 562.7±95.54 units/g으로 곰팡이 종균의 접종량이 증가할수록 높은 활성을 나타냈다. 이러한 결과는 각각의 곰팡이가 액체종균 배양기간 중 포자가 발아하여 균사체가 많이 생장(Oh KC 등 1988)하여 접종량에 비례하여 효소활성이 높아진 것이다. 그 외 대부분의 곰팡이 고상종국에서는 저농도 액체종균에서 α-amylase 효소활성이 높았다. Kim IH 등(1996)의 연구에서 단일배양에 따른 액화력은 100∼735 units/g의 효소활성 보고로 본 연구 결과와 유사하였다. 특히, A. oryzae OF5-18 고상종균은 액체종균 3%(v/w)로 접종한 것이 10%보다 2배 정도 높은 효소활성을 나타내었다. A. oryzae IF18-2는 3% 액체종균을 접종한 고상종국에서 805.3±12.64 units/g의 높은 효소활성을 나타냈고, A. turbengensis OF5-8보다 10배 정도 α-amylase 활성이 높았다. 일반적으로 국내외 시판하는 상업용 종균은 야생균주보다 유전적으로 안정되고 착생능력이 우수하여 생육이 왕성하다는 Noh JM 등(2013)의 보고처럼, 본 연구에서 액체종균의 접종량에 반비례하게 효소활성이 나타난 종균(A. oryzae OF5-18)은 착생능력과 생육이 우수하여 균체량이 많아 적은양의 접종이 오히려 접한 곰팡이 면적 확보에 따른 생육속도의 증가로 효소활성에 영향을 미친 것으로 생각된다. 한편, A. oryzae IF18-2의 효소 생성능 차이는 다른 종균보다 월등히 높게 나타나는데, 향후, 추가적인 연구를 통하여 각 곰팡이들의 생리적인 특징들을 더 검토할 필요가 있다.
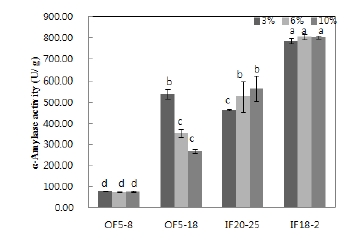
The α-amylase activity of each solid fermented starter by amount of inoculation.Data are presented as the mean for 3 independent experiments. Error bars indicate SD(p<0.05). Significance comparison was performed at Duncan’s multiple range test at p<0.05 level. Different letters were indicated with the statistical analysis according to fermentation temperature of each fungal strain. OF5-8, nuruk of A. turbingensis KACC 93270P; OF5-18, nuruk of A. oryzae KACC 93284P; IF20-25, nuruk of A. oryzae KACC 93286P; IF18-2, nuruk of A. oryzae KACC 93289P.
4. 고상종국의 glucoamylase 효소활성
고상종균 제조시 액체종균의 접종량에 대한 최적조건을 선정하기 위해서 곰팡이 종균별 고상종균의 glucoamylase 활성 결과를 Fig. 4에 나타내었다. 액체종균 3%(v/w)로 접종한 경우, A. oryzae IF18-2 고상종국이 2,107.32±88.30 units/g으로 높은 glucoamylase 활성을 나타냈고, A. turbengensis OF5-8, A. oryzae OF5-18 및 A. oryzae IF20-25로 제조한 고상종국은 1,618.36±159.11 units/g, 986.59±17.48 units/g 및 807.32±19.23units/g의 순으로 높은 당화력을 보였다. A. turbengensis OF5-8 고상종국은 α-amylase와 상반되게 높은 glucoamylase 효소활성을 나타내었다. Aspergillus 속 균주는 증자한 쌀에서 성장이 용이하며, 강력한 전분 당화효소를 생산하는 것으로 알려져 있다(Huh CK 등 2014). 이처럼 모든 고상종국의 당화력이 우수한 것으로 보아 다양한 발효제를 개발하는데 적합한 것으로 여겨진다. A. oryzae OF5-18과 A. oryzae IF18-2 고상종국에서는 액체종균을 3%(v/w) 접종하였을 때 glucoamylase 효소활성이 높았다. A. turbengensis OF5-8와 A. oryzae IF20-25는 종균 접종량이 증가할수록 높은 효소활성을 나타내지만, 고상종국 제조에 사용되는 시간과 노력, 인건비, 전기료 등 제반 경비 등 경제성을 고려하면(Choi JS 등 2011) 종균에 따라 약간의 차이는 있지만 액체종균의 최적 접종량은 3%(v/w)가 가장 적합한 것으로 여겨진다.
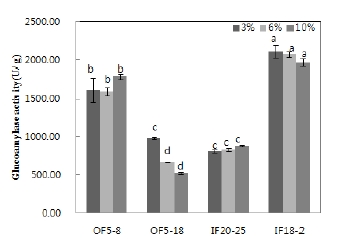
The glucoamylase activity of each solid fermented starter by amount of inoculation.Data are presented as the mean for 3 independent experiments. Error bars indicate SD(p<0.05). Significance comparison was performed at Duncan’s multiple range test at p<0.05 level. Different letters were indicated with the statistical analysis according to fermentation temperature of each fungal strain. OF5-8, nuruk of A. turbingensis KACC 93270P; OF5-18, nuruk of A. oryzae KACC 93284P; IF20-25, nuruk of A. oryzae KACC 93286P; IF18-2, nuruk of A. oryzae KACC 93289P.
5. 고상종국의 acidic protease 효소활성
분리한 4종류 곰팡이(A. turbengensis OF5-8 및 A. oryzae OF5-18, A. oryzae IF20-25, A. oryzae IF18-2) 액체종균의 접종량에 대한 최적조건을 선정하기 위한 단백질 분해력 결과는 Fig. 5에 나타내었다. 고상종국을 제조하기 위해 배양한 액체종균을 농도별(3%, 6%, 및 10%)로 접종하여 고상종국을 제조한 후, 효소활성을 분석한 결과, A. turbengensis OF5-8은 31,118.5±125.56 units/g의 높은 활성을 나타내고, 농도별 3∼10%(v/w)로 접종한 모든 영역에서 효소활성이 높았다. A. oryzae OF5-18, A. oryzae IF20-25 및 A. oryzae IF18-2의 단백질 분해력은 A. turbengensis OF5-8보다 2.5∼4배 낮은 활성을 보였고, 액체종균 농도별 접종에 따른 효소활성 차이는 크지 않았다. 결론적으로 A. turbengensis OF5-8는 다른 고상종국과 달리 산성 단백질 분해력이 가장 우수하여 주류제조보다는 장류제조에 사용하면 대두의 단백질을 잘 분해 할 것으로 여겨진다.
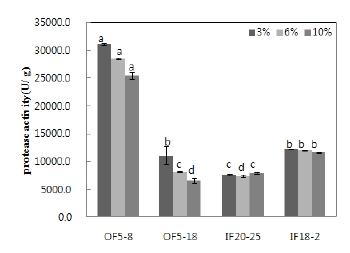
The acidic protease activity of each solid fermented starter by amount of inoculation.Data are presented as the mean for 3 independent experiments. Error bars indicate SD(p<0.05). Significance comparison was performed at Duncan’s multiple range test at p<0.05 level. Different letters were indicated with the statistical analysis according to fermentation temperature of each fungal strain. OF5-8, nuruk of A. turbingensis KACC 93270P; OF5-18, nuruk of A. oryzae KACC 93284P; IF20-25, nuruk of A. oryzae KACC 93286P; IF18-2, nuruk of A. oryzae KACC 93289P.
요 약
본 연구에서 전통누룩에서 분리한 Aspergillus sp.(A. turbengensis OF5-8 및 A. oryzae OF5-18, A. oryzae IF18-2, A. oryzae IF20-25) 종균을 주류용 발효제로 사용하기 위한 aflatoxin B1 생산능과 전분 분해력과 단백질 분해력을 확인 하였다. 분리된 Aspergillus sp.의 aflatoxin 생산은 대조구인 A. flavus KACC 41862에 비해 7∼20배 낮은 농도로 측정되었다. 각각의 곰팡이 종균들을 온도별(23℃, 25℃ 및 28℃)로 효소활성을 측정한 결과. A. turbengensis OF5-8과 A. oryzae IF18-2 종균의 α-amylase 효소활성은 각각 23℃와 25℃에서 높은 효소활성을 보였다. A. oryzae IF18-2 종균은 다른 균주들에 비해 glucoamylase 활성이 모든 배양 온도에서 우수한 효소활성을 나타냈다. 종균별 제조한 고상종국은 액체종균의 접종량(3%(v/w), 6%(v/w), 10%(v/w))에 따라 효소활성이 검정되었다. A. oryzae IF18-2의 액화력(825.3 units/g)과 당화력(2107.3 units/g)은 액체종균 3%(v/w)로 접종하였을 때, 높은 활성을 보였다. 본 연구 결과는 A. oryzae IF18-2로 제조한 종국의 효소활성이 가장 우수한 것으로 생각되고, 향후 막걸리용 종균 및 발효제의 상용화 과정에 활용될 것으로 사료된다.
감사의 글
이 논문은 농촌진흥청 농업과학기술개발사업(과제번호:PJ01242501)의 지원에 의해 이루어진 것이며, 연구비 지원에 감사드립니다.
References
- Baek, SY, Yun, HJ, Chio, HS, Jeong, ST, Hong, SB, Koo, BS, Yeo, SH, (2010), Screening and characteristics of useful fungi for brewing from commercial Nuruk in Chungcheong provinces, Korean J Microbiol Biotechnol, 38(4), p373-378.
- Baek, SY, Kim, JY, Yun, HJ, Chio, JH, Jeong, ST, Yeo, SH, (2011), Quality characteristics of Makgeolli and nuruk grain inoculated with Aspergillusoryzae N041, J East Asian Soc Diet Life, 21(6), p877-811.
- Choi, JS, Jeong, ST, Kim, JY, Choi, JH, Choi, HS, Yeo, SH, (2011), Quality characteristics of wheat nuruk and optimum condition of liquid starters of Aspergillus sp, Korean J Microbiol Biotechnol, 39(4), p357-363.
-
Huh, CK, Kim, SM, Kim, YD, (2014), Comparison for enzymic activity of nuruk and quality properties of Yakju by different fungi, Korean J Food Preservation, 21(4), p573-580.
[https://doi.org/10.11002/kjfp.2014.21.4.573]

-
Im, SY, Baek, SY, Park, HY, Choi, HS, Choi, JH, Jeong, ST, Shin, WC, Park, HD, Yeo, SH, (2014), Quality characteristics of Takju according to different rice varieties and mixing ratio of nuruk, Korean J Food Preservation, 21(6), p892-902.
[https://doi.org/10.11002/kjfp.2014.21.6.892]

- Jo, GY, Lee, CW, (1997), Isolation and identification of the fungi from nuruk, J Korean Soc Food Sci Nutr, 26(5), p759-766.
- Jeon, CO, (2014), Industrial application and starter development for traditional fermentation food using lab evolution method, E-Bioindustry, 27(6), p1-4.
- Jeong, JH, Chai, HS, Lee, YH, Kim, Jm, Lee, JH, (2015), Quality characteristics of Takju, Yakju, Spirit made by cereal nuruks, Korean J Culinary Research, 21(1), p267-280.
- Kim, CJ, Oh, MJ, Lee, JS, (1985), Studies on digestion of raw starch by Rhizopus oryzae, Korean J Appl Microbiol Bioeng, 13(4), p329-337.
- Kim, CJ, Kim, KC, Kim, DY, Oh, MJ, Lee, SK, Lee, SO, Chung, ST, Chung, JH, (1990), Fermentation Technology, Sunjinmunhasa, Seoul, p79-103.
- Kim, IH, Park, WS, Koo, YJ, (1996), Comparison of fermentation characteristics of Korean traditional alcoholic beverage with different input step and treatment of rice and nuruk Korean-style bran koji, Korean J Dietary Culture, 11(3), p339-348.
- Kim, HS, Hyun, JS, KIm, J, Ha, HP, Yu, TS, (1997), Characteristics of useful fungi isolated from traditional Korean nuruk, J Korean Soc Food Sci Nutr, 26(5), p767-774.
- Kim, HS, Hyun, JS, Kim, J, Ha, HP, Yu, TS, (1998), Enzymological characteristics and identification of useful fungi isolated from traditional Korea nuruk, Korean J Microbiol Biotechnol, 26(5), p456-464.
-
Kim, MS, Kim, SN, Ha, BS, Park, HY, Baek, SY, Yeo, SH, Ro, HS, (2014), Diversity, saccharification capacity, and toxigenicity analyses of fungal isolates in nuruk, Korean J Mycol, 42(3), p191-200.
[https://doi.org/10.4489/kjm.2014.42.3.191]

- Lee, SH, Jung, HJ, Yeo, SH, Kim, HS, Kim, HS, Yu, TS, (2004), Characteristics of α-amylase of a new species Aspergillus coreanus NR 15-1, Korea J Biotechnol Bioeng, 19(4), p301-307.
- Lee, JH, Kwon, YJ, Song, HG, (2012), Relationships between consumers well-being recognition and Korea traditional liquor selection properties, J Food Serv Manage Soc Kor, 15(5), p163-183.
-
Mun, JY, Baek, SY, Park, HY, RO, HS, (2016), Cultural characteristics of fungi strains isolated from Korean nuruk, J East Asian Soc Diet Life, 26(2), p125-140.
[https://doi.org/10.17495/easdl.2016.4.26.2.125]

- National Institute of Food and Drug Safety Evaluation, (2016), Risk Assessment of Mycotoxins, KOSEF 11-1471057-000206-01.
- Noh, JM, Choi, JH, Jung, ST, Yeo, SH, Park, JW, Lee, JW, Choi, HS, (2013), Mycelial production and amylase activity of fungi gor brewing in different submerged culture conditions, J East Asian Soc Dietary Life, 23(6), p833-838.
- Oh, KC, Yu, TJ, Kim, TY, (1988), Studies on degree of kojic mycelial penetration and some characteristics of kojic enzyme in moromi, Kor J Mycol, 16(3), p175-184.
- Park, CS, Lee, TS, (2002), Quality characteristics of Takju prepared by wheat flour nuruk, Korean J Food Sci Technol, 34(2), p296-302.
-
Roman, BE, Driksna, D, Abouzied, MM, Klein, F, Rice, J, (2010), Validation of max aqueous extraction on veratox for total aflatoxin ELISA test kit, J AOAC Int, 100(4), p1131-1133.
[https://doi.org/10.5740/jaoacint.17-0034]

- So, MH, Lee, JW, (1996), Takju brewing by combined use of Rhizopusjaponicus-nuruk and Aspergillus oryzae-nuruk, J Korean Soc Food Nutr, 25(1), p157-162.
- So, MH, Lee, YS, (2003), Takju making by rice koji of Rhizopus sp. and Aspergilluskawachii, Research Note of Zymbio Institute, p5-10.
- Shin, DH, (2010), Globalization trends and prospect of Korean traditional fermented foods, Food Science and Industry, 43(3), p69-82.
-
Woo, SM, Shin, JS, Seong, JH, Yeo, SH, Choi, JH, Kim, TY, Jeong, YJ, (2010), Quality characteristics of brown rice Takju by different nuruk, J Korean Soc Food Sci Nutr, 39(2), p301-307.
[https://doi.org/10.3746/jkfn.2010.39.2.301]

